8 Minuten
Außergewöhnliche Lebensdauer und was sie uns lehren kann
Es gibt kein Entkommen vor dem Altern, doch eine kleine Gruppe von Menschen — Supercentenarians, die 110 Jahre und mehr erreichen — scheint viele altersbedingte Erkrankungen zu verzögern oder abzuschwächen. Eine umfassende molekulare und klinische Analyse von Maria Branyas, die 117 Jahre alt wurde, eröffnet ein seltenes Fenster auf biologische Merkmale, die extreme menschliche Langlebigkeit unterstützen könnten. Der vorliegende Fall verknüpft klinische Messungen, Multi‑Omics‑Profile und genetische Analysen, um Biomarker zu identifizieren, die mit gesundem Altern, robuster Immunfunktion und kardiovaskulärer Widerstandsfähigkeit assoziiert sind.

Maria Branyas im Jahr 1925
Die Studie, geleitet von Teams des Josep Carreras Leukaemia Research Institute in Barcelona und veröffentlicht in Cell Reports Medicine, nutzte Blut, Speichel, Urin und Stuhlproben, die vor Branyas' Tod im Jahr 2024 entnommen wurden. Die Forschenden — unter anderem die Epigenetiker Eloy Santos‑Pujol und Aleix Noguera‑Castells — berichten, dass einige Zelltypen und molekulare Signaturen bei Branyas so „wirkten“, als stammten sie von deutlich jüngeren Personen. Ihr Profil vereint vorteilhafte genetische Varianten, einen niedrigen Entzündungszustand, ein charakteristisches Darmmikrobiom und kardiovaskuläre Marker, die mit reduziertem Erkrankungsrisiko einhergehen.
Studiendesign und Methoden: Proben, Analysen und Vergleichsrahmen
Um die biologischen Grundlagen extremer Lebensdauer zu untersuchen, führten die Forschenden eine multimodale Analyse durch: Ganzgenomsequenzierung, Schätzungen des epigenetischen Alters (Methylierungsuhren), Lipidprofile, Immunzellphänotypisierung und Sequenzierung des Darmmikrobioms. Diese Messgrößen wurden mit Referenzdaten jüngerer Kohorten sowie anderer älterer Individuen verglichen, um Abweichungen zu identifizieren, die eher mit Widerstandskraft als mit funktionalem Abbau zusammenhängen.
Probenarten und Laborverfahren
- Blut: genomische DNA, Immunzellzahlen, Entzündungsmarker und Lipidprofile.
- Speichel: ergänzende DNA für Sequenzierung und Validierung keimbahnvererbter Varianten.
- Urin: metabolische Nebenprodukte und Biomarker der Nierenfunktion.
- Stuhl: Zusammensetzung und Diversität des Mikrobioms mittels 16S‑rRNA‑Sequenzierung und Shotgun‑Metagenomik.

Epigenetische Uhren schätzen das biologische Alter, indem sie DNA‑Methylierungsmuster über das Genom hinweg messen; zusätzlich wurden kürzere Telomere — die schützenden Kappen an Chromosomenenden — analysiert, um zelluläre Alterungsdynamiken zu bewerten. Zusammengenommen liefern diese molekularen Messungen eine mehrschichtige Sicht auf die Biologie des Alterns: genetische Prädisposition, epigenetische Regulation, Immungesundheit und Wechselwirkungen mit dem Mikrobiom. Solche kombinierten Ansätze erhöhen die Aussagekraft im Vergleich zu Einzelmethoden und helfen, komplexe Beziehungen zwischen Faktoren sichtbar zu machen.
Wesentliche Ergebnisse: jung wirkendes molekulares Profil, günstige Lipide und geringe Entzündlichkeit
Aus der Analyse traten mehrere konsistente Signale hervor. Erstens zeigten viele von Branyas' zellulären und molekularen Markern trotz ihres hohen Alters Profile, die denen deutlich jüngerer Personen ähneln. Ihre epigenetischen Altersabschätzungen waren in bestimmten Geweben niedriger als ihr chronologisches Alter, was auf eine verlangsamte epigenetische Alterung in ausgewählten Zelltypen hinweist. Solche Diskrepanzen zwischen Chrono‑ und Biologiealter liefern Hinweise auf zelltypspezifische Schutzmechanismen.
Zweitens wies sie außergewöhnlich niedrige systemische Entzündungswerte auf — ein bekannter Prädiktor für bessere Gesundheit im Alter. Niedrige Werte für entzündungsfördernde Zytokine und akute‑Phase‑Proteine korrelieren häufig mit geringerer Gebrechlichkeit und besserer Immunantwort. Ein dauerhaft niedriger Entzündungszustand kann langfristig Gewebe‑ und Organfunktionen erhalten.
Kardiometabolische Marker fielen ebenfalls auf: Branyas hatte sehr niedrige Werte an Low‑Density‑Lipoprotein (LDL) und Triglyzeriden und zugleich ungewöhnlich hohe Werte an High‑Density‑Lipoprotein (HDL). Dieses Lipidprofil steht im Einklang mit einem reduzierten kardiovaskulären Risiko und könnte zu ihrer verlängerten Gesundheitsspanne beigetragen haben. Lipidstoffwechsel und entzündliche Prozesse sind eng verknüpft; günstige Lipidfraktionen können entzündungsfördernde Pfade dämpfen und die Endothelfunktion stabilisieren.
Ihr Darmmikrobiom ähnelte in Schlüsseldimensionen jenem jüngerer Kohorten, etwa in puncto mikrobieller Diversität und Vorkommen taxonomischer Gruppen, die mit anti‑entzündlichen Metaboliten verbunden sind. Beispiele sind erhöhte Anteile von Butyrat‑produzierenden Bakterien, die die Darmbarriere stärken und systemische Entzündungsreaktionen reduzieren können. Zudem identifizierten die Forschenden seltene genetische Varianten in Branyas' Genom, die mit Langlebigkeit, Immunfunktion und Neuroprotektion assoziiert sind, was auf einen genetischen Beitrag zu ihrer Widerstandsfähigkeit hindeutet.
Paradoxerweise beobachtete das Team eine "massive Erosion" der Telomere bei Branyas. Während kürzere Telomere häufig mit erhöhtem Sterblichkeitsrisiko verbunden werden, deuten neuere Befunde darauf hin, dass die Telomerlänge bei Hochbetagten nicht immer prognostisch ist. Eine mögliche Interpretation ist, dass besonders kurze Telomere in Zelllinien mit hoher Teilungsaktivität die Chance für die Expansion maligner Klone verringern könnten — ein Mechanismus, der das Krebsrisiko reduziert. Diese Hypothese bleibt jedoch spekulativ und erfordert weitere funktionelle Untersuchungen.
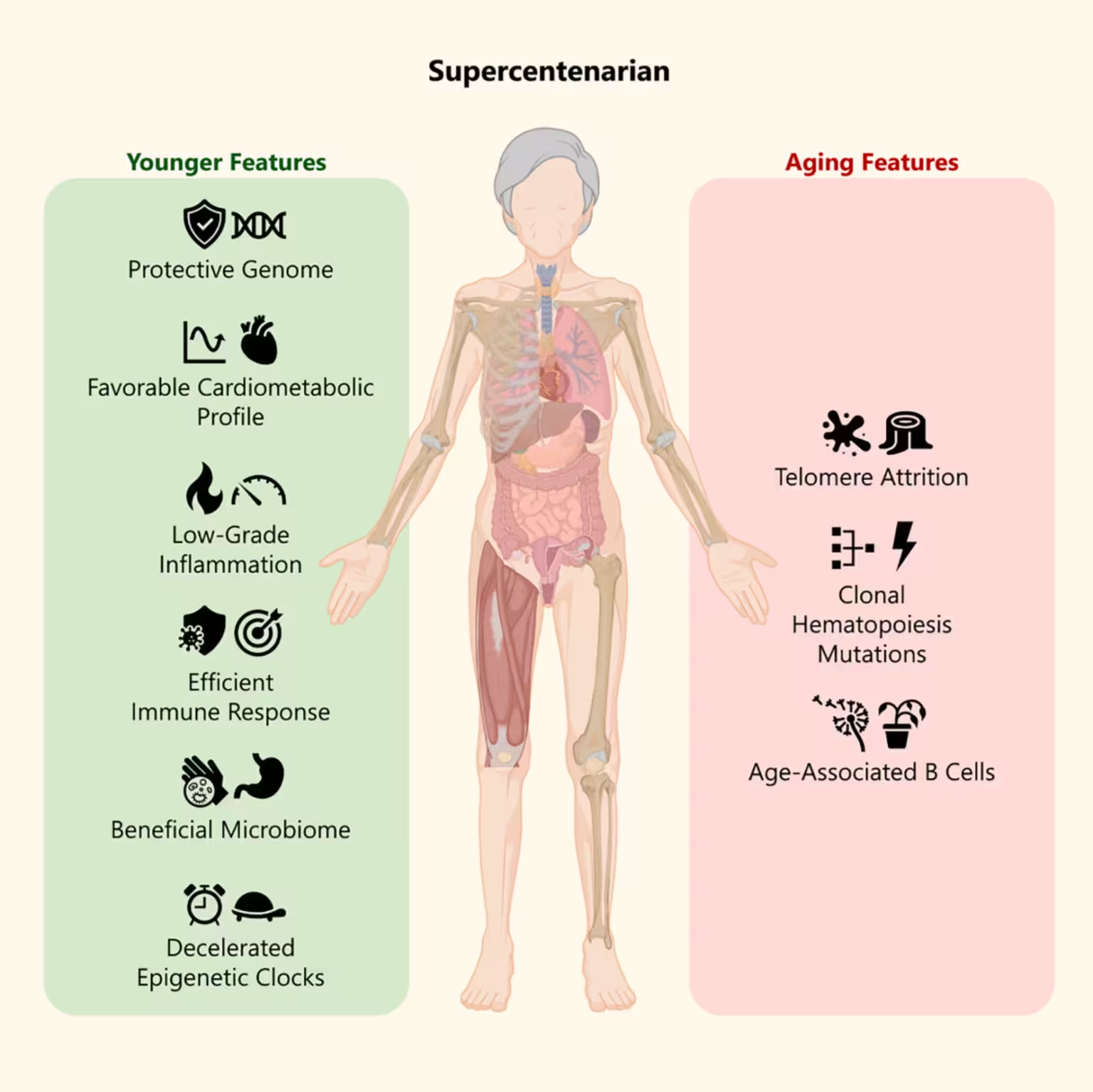
Jüngere Merkmale und Alterungsaspekte bei Maria Branyas
In der Summe ergibt sich ein Bild gemischter Alterungssignale: molekulare Jugendlichkeit in Immun‑ und epigenetischen Uhren, günstige Lipid‑ und Entzündungsprofile, ein Mikrobiom, das mit Gesundheit übereinstimmt, und paradoxerweise sehr kurze Telomere. Ein solches Muster könnte erklären, wie Branyas die durchschnittliche Lebenserwartung von Frauen in Katalonien um mehr als drei Jahrzehnte übertraf. Es illustriert außerdem, wie unterschiedliche Ebenen biologischer Regulation zusammenwirken können, um Resilienz zu erzeugen.
Wissenschaftlicher Kontext und Implikationen für die Alternsforschung
Diese Fallstudie trägt zu mehreren zentralen Themen der Langlebigkeitsforschung bei. Erstens ist extreme Langlebigkeit multifaktoriell: eine Mischung aus schützenden genetischen Faktoren, Lebensstil (etwa einer mediterranen Ernährung mit höheren Anteilen fermentierter Milchprodukte wie Joghurt), niedriger chronischer Entzündung und widerstandsfähiger Immunfunktion. Zweitens erfasst kein einzelner Biomarker das Altern vollständig; Telomerlänge, epigenetisches Alter und Mikrobiomzusammensetzung liefern jeweils nur Teilinformationen und können teils widersprüchliche Signale senden.
Forschende mahnen zur Vorsicht bei Verallgemeinerungen aus nur einer Person. Einzelfälle generieren Hypothesen, sind aber keine endgültigen Beweise. Größere Kohorten von Hundertjährigen und Supercentenarians sind notwendig, um reproduzierbare Biomarker und kausale Mechanismen zu identifizieren, die sich in Interventionen übersetzen lassen, um die Gesundheitsspanne der Allgemeinbevölkerung zu verbessern.
Die Studienautoren schlagen explizit vor, dass ihre Erkenntnisse "einen neuen Blick auf die Biologie des menschlichen Alterns bieten, Biomarker für gesundes Altern aufzeigen und potenzielle Strategien zur Erhöhung der Lebenserwartung liefern". Zukünftige Arbeiten müssen die identifizierten genetischen Varianten und molekularen Signaturen in unabhängigen Stichproben validieren und untersuchen, ob eine Modulation des Mikrobioms, der Entzündungsantwort oder epigenetischer Zustände klinisch messbare Verlängerungen der gesunden Lebensjahre bewirken kann — idealerweise in gut konzipierten Interventionsstudien.
Experteneinschätzung
Dr. Ana Cortes, eine fiktive Geroscience‑Forscherin und Wissenschaftskommunikatorin, kommentierte die größere Bedeutung der Studie: "Einzelfallstudien wie die von Maria Branyas sind immens wertvoll, weil sie uns zwingen, zu ergründen, warum manche Menschen sich den typischen Alterungspfaden entziehen. Diese Arbeit verknüpft Genomik, Epigenetik und Mikrobiomforschung auf eine Weise, die auf integrierte Resilienzmodelle hinweist. Zwar lassen sich aus einer Person keine allgemeinen Schlüsse ziehen, aber die molekularen Signaturen liefern konkrete Ziele für größere Studien — insbesondere Signalwege, die Entzündung und Immunüberwachung regulieren."
Diese Perspektive spiegelt die vorsichtige Zuversicht des Forschungsteams wider: Die Biologie extremer Langlebigkeit ist komplex, doch messbare Merkmale — von Lipidstoffwechsel über mikrobielle Metabolite bis zur epigenetischen Regulation — können künftige translationale Forschungsansätze leiten.
Praktische Erkenntnisse und Ausblick
Für Kliniker und Forschende hebt die Studie Kandidaten‑Biomarker hervor, die in Kohortenstudien langlebiger Menschen Priorität haben sollten: epigenetische Uhrenmaße, Profile entzündlicher Zytokine, Lipidfraktionen und Metriken zur Mikrobiomdiversität. Solche Zielgrößen erleichtern das Monitoring von Interventionen und die Vergleichbarkeit zwischen Studienzentren.
Für die Allgemeinbevölkerung bestätigen die Ergebnisse etablierte Empfehlungen für gesundes Altern: soziale und kognitive Aktivität beibehalten, regelmäßige körperliche Betätigung, eine ausgewogene Ernährung (die mediterrane Diät wird wiederholt mit kardiovaskulärer Gesundheit in Verbindung gebracht) und das Management chronischer Entzündung sowie metabolischer Risikofaktoren. Diese Maßnahmen sind pragmatisch, evidenzbasiert und übertragbar auf breite Bevölkerungsgruppen.
Technologisch demonstriert die Studie den Wert integrierter Multi‑Omics‑Ansätze — die Kombination von Genomik, Epigenomik, Metabolomik und Mikrobiomik — um ein Systemniveauverständnis des Alterns zu entwickeln. Fortschritte in Single‑Cell‑Profiling, longitudinalen Kohortenabfolgen und kontrollierten Interventionsstudien (etwa gezielte Mikrobiommodulation oder anti‑entzündliche Therapien) werden entscheidend sein, um von beobachtenden Befunden zu wirksamen, evidenzbasierten Therapien zu gelangen.
Schlussfolgerung
Das molekulare Porträt von Maria Branyas zeigt, dass extremes Alter und erhaltene Gesundheit koexistieren können. Ihr Fall unterstreicht die Komplexität des Alterns: vorteilhafte genetische Varianten, in einigen Zelltypen jung erscheinendes Epigenom, niedrige Entzündungswerte, ein resilient wirkendes Mikrobiom und günstige Lipidprofile zeichnen zusammen ein Bild biologischer Widerstandskraft. Obwohl ein Einzelfall keine Kausalität beweist oder auf alle Populationen übertragbar ist, liefert er eine wertvolle Roadmap für künftige Studien mit dem Ziel, Biomarker zu identifizieren und Interventionen zu entwickeln, die gesundes Altern fördern und die menschliche Gesundheitsspanne verlängern.
Die wachsende Zahl Hundertjähriger weltweit macht diese Untersuchungen zunehmend dringlich. Mit sorgfältiger Replikation und erweiterten Kohorten könnten die molekularen Hinweise aus außergewöhnlichen Individuen in Strategien münden, die mehr Menschen ein längeres, gesünderes Leben ermöglichen.
Quelle: sciencealert

.webp)
Kommentar hinterlassen