3 Minuten
Fonas: kodėl tai svarbu 1 tipo diabetui
1 tipo cukrinis diabetas yra autoimuninė liga, kurioje organizmo imuninė sistema sunaikina kasos insulino gamybai atsakingas saleles. Standartinis gydymas reikalauja viso gyvenimo trukmės insulino injekcijų ir atidžios gliukozės kontrolės. Pakeisti pažeistas saleles funkcionuojančiomis donoro ląstelėmis — vadinama salelių transplantacija — ilgą laiką buvo tyrimų objektas, siekiant atkurti fiziologinį insulino išsiskyrimą. Tačiau transplantacijos metu donoro ląstelės dažnai atpažįstamos kaip svetimos, todėl paprastai reikia sisteminės imunosupresijos, kuri didina infekcijų ir navikų riziką.
Pirmosios žmogaus transplantacijos įrodymas su genų redaguotomis salelėmis
Revoliuciniame įrodymo koncepcijos tyrime 42 metų vyras, sergantis 1 tipo diabetu nuo penkerių metų, gavo donoro kasos saleles, genetiškai išredaguotas taip, kad jas būtų sunkiau atpažinti imuninei sistemai. Salelės buvo suleistos keliomis injekcijomis į priežasties raumenų audinį. Per pirmąsias 12 savaičių persodintos salelės pradėjo reaguoti į gliukozės padidėjimą — pavyzdžiui po valgio — ir, svarbiausia, pacientui nebuvo taikyta sisteminė imunosupresinė terapija.
Genų redagavimo strategija
Tyrėjai panaudojo CRISPR genų redagavimą ir atliko tris modifikacijas donoro salelėse prieš transplantaciją. Dvi redakcijos sumažino specifinių antigenų išraišką, kuriuos adaptacinė T ląstelių sistema naudoja atpažinti svetimas ląsteles, o trečioji padidino CD47 baltymo, esančio ant ląstelių paviršiaus, gamybą — tai slopina įgimtą imuninį atsaką. Triguba redagavimo strategija buvo sukurta taip, kad susilpnintų tiek adaptacinę (T ląstelių), tiek įgimtą (natūralių žudikų ir makrofagų) imuninę reakciją, neapsunkinant viso organizmo imuniteto.
Ne visos grafto ląstelės turėjo sėkmingas modifikacijas. Ši įvairovė veikė kaip vidinis kontrolės mechanizmas: neredaguotos ląstelės greitai pašalintos T ląstelių, ląstelės su vien tik antigenų mažinimo pakeitimais vis tiek buvo atakuotos natūralių žudikų ir makrofagų, o tik visiškai trigubai redaguotos ląstelės išgyveno pakankamai ilgai, kad išliktų funkcingos. Didesnis trigubai redaguotų salelių kiekis grafte užtikrino insulino gamybą stebėjimo laikotarpiu.
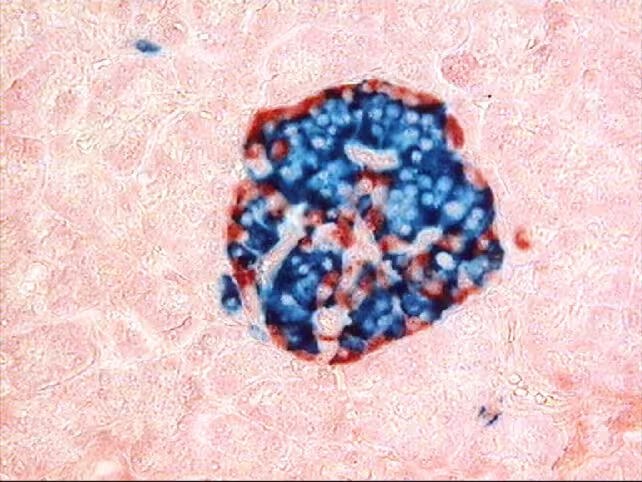
Pagrindiniai rezultatai ir pasekmės
Tai pirmasis praneštas žmogaus atvejis, kuriame genetiškai redaguotos salelės veikė recipiento organizme be sisteminių imunosupresantų. Išankstiniai ne žmogaus primatų ir graužikų tyrimai rodė, kad metodas gali veikti, tačiau ankstesnės sėkmingos žmogaus salelių transplantacijos dažniausiai reikalavo imunosupresijos. Išvengti viso gyvenimo trukmės imunosupresinių vaistų reikštų reikšmingą ilgalaikių sveikatos rizikų sumažėjimą pacientams ir praplėstų ląstelių terapijos klinikinį taikymą.
Už diabeto ribų ši technika siūlo bendrinamą platformą, kaip sumažinti donorinių ląstelių ir audinių matomumą šeimininko imuninei sistemai. Jei metodas bus pakartojamas ir saugus didesniuose tyrimuose, CRISPR pagrįsta imuninio „slėpimo“ inžinerija galėtų mažinti arba eliminuoti poreikį imunosupresijai įvairių alogeninių transplantacijų atvejais.
Susijusios naujovės ir kontekstas
Lygiagrečios pažangos kryptys apima autologinius sprendimus, kurie visiškai eliminuoja imunologinį neatitikimą: pavyzdžiui, neseniai Kinijoje pranešta apie jaunos moters atvejį, kai ji gavo iš savo kamieninių ląstelių išvestas insuliną gaminančias ląsteles ir pasiekė ilgalaikį gliukozės valdymą be donorinio imuninio atsako. Tiek autologinės ląstelių terapijos, tiek imuninio „naišinimo“ alogeniniai graftai yra aktyvios tyrimų sritys, kiekviena su savo privalumais ir techniniais iššūkiais.
Ekspertų įžvalga
Dr. Elena Martín, dirbanti transplantologijos ir imunologijos srityje, teigia, kad tai yra kertinis įrodymas: kombinacija, kuri mažina antigenų išraišką ir didina CD47, sprendžia tiek adaptacinę, tiek įgimtą imuninę reakciją — tai pagrindinė naujovė. Vis dėlto reikia didesnių, kontroliuojamų tyrimų, kad būtų patvirtintas ilgalaikis efektas, atmesti nepageidaujamos redagavimo pasekmės ir įvertinta sauga. Ekspertai pabrėžia būtinybę atidžiai stebėti galimas nenumatytas pasekmes, pavyzdžiui grafto elgsenos pokyčius ar retas imuninės komplikacijas.
Išvada
Praneštas atvejis žymi svarbų žingsnį link ląstelinės terapijos sprendimų 1 tipo diabetui, parodydamas, kad CRISPR redaguotos kasos salelės gali veikti žmogaus organizme be sisteminės imunosupresijos. Nors tai preliminarūs duomenys, rezultatas atveria naujas galimybes saugesnėms ir plačiau taikomoms ląstelių terapijoms ir pabrėžia tolesnių klinikinių tyrimų būtinybę siekiant įvertinti efektyvumą, saugumą ir ilgalaikius rezultatus.
Quelle: nejm


Kommentar hinterlassen