8 Minuten
Stellen Sie sich vor, man könnte in einer einzigen öffentlichen Gesundheitsmaßnahme mehr als ein Drittel der Typhusfälle bei Kindern verhindern. Genau dieses Ausmaß legt Forschung aus Indien nahe: Durch routinemäßige Impfungen in städtischen Gebieten könnten bis zu 36 Prozent der Typhusinfektionen und der damit verbundenen Todesfälle bei Kindern verhindert werden. Kurz, prägnant und keineswegs hypothetisch.
Impfstoffe verändern bereits die Lage. Pakistan war das erste Land, das eine routinemäßige Immunisierung gegen Typhus eingeführt hat, und eine Handvoll anderer Länder zieht nach oder prüft ähnliche Schritte. Die Centers for Disease Control and Prevention (CDC) weist darauf hin, dass die Weltgesundheitsorganisation (WHO) bis April 2025 vier Typhus-Konjugatimpfstoffe vorkqualifiziert hatte – Instrumente, die nun in die Kinderschutzprogramme in Regionen eingeführt werden, in denen Typhus endemisch ist.
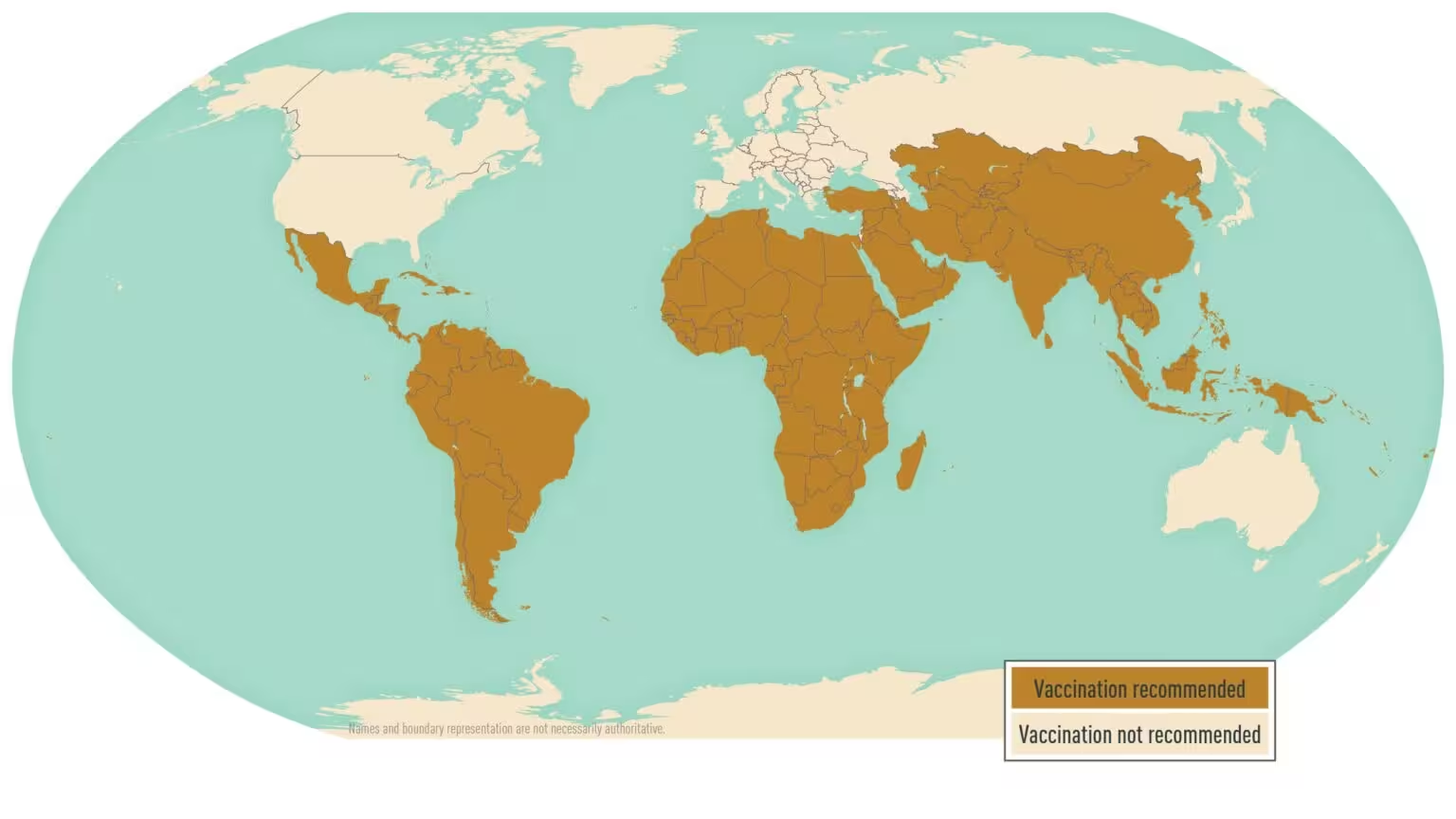
Warum das jetzt wichtig ist
Antibiotikaresistenz ist nicht länger ein Problem der Zukunft. Sie fordert jährlich mehr Todesopfer als manche bekannte Infektionskrankheiten, und resistente Typhuserreger machen die Behandlung schwieriger, teurer und zeitaufwändiger. Impfungen verändern die Rechnung: Wenn Infektionen von vornherein verhindert werden, verringert sich der Selektionsdruck, der die Entstehung und Ausbreitung resistenter Stämme antreibt. Kurz gesagt: Impfstoffe gehören zu den wenigen skalierbaren, nachgewiesenen Abwehrmaßnahmen gegen eine Zukunft, in der gewöhnliche bakterielle Infektionen wieder lebensbedrohlich werden könnten.
Die Evidenz wächst stetig. Eine Studie, veröffentlicht in The Lancet Microbe, analysierte städtische Immunisierungsszenarien und fand erhebliche Rückgänge von Fällen und Todesfällen, wenn Kinder Typhus-Konjugatimpfstoffe erhielten. Die praktische Einführung in Ländern wie Pakistan liefert frühe Erkenntnisse zu Logistik, Versorgungslücken und Einbindung der Gemeinschaft – Lehren, die andere Staaten adaptieren können, ohne das Rad neu zu erfinden.
„Wo Impfstoffe Kinder erreichen, sehen wir unmittelbare gesundheitliche Erträge“, sagt Dr. Anita Rao, eine Epidemiologin für Infektionskrankheiten, die an regionalen Impfprogrammen beteiligt ist. „Aber Versorgung, politischer Wille und Finanzierung bestimmen, ob sich diese Erträge skalieren lassen.“ Ihr Punkt ist klar: Die Wissenschaft ist eindeutig; die Umsetzung ist das Nadelöhr.
Investitionen in neue Antibiotika bleiben unerlässlich. Genauso wichtig ist der Ausbau des Impfstoffzugangs, die Stärkung der Surveillance für resistente Stämme und die Unterstützung von Gesundheitssystemen, die routinemäßige Kinderimmunisierungen bereitstellen. Die Teile passen zusammen; die Frage ist, ob Regierungen und globale Gesundheitspartner sie zusammensetzen, bevor die Resistenzlage sich weiter zuspitzt.
Wir haben keine Zeit zu verschwenden.
Aus epidemiologischer Sicht erklärt sich der hohe Nutzen durch mehrere Wirkmechanismen: Erstens reduziert die direkte Schutzwirkung des Impfstoffs die Inzidenz bei Geimpften und damit die Gesamtübertragungsrate (R0) innerhalb urbaner Populationen. Zweitens verringert ein niedrigerer Krankheitsdruck die Antibiotikaanwendung in der Gemeinde – sowohl die rechtmäßige Behandlung als auch die ungerechtfertigte Selbstmedikation – und drittens begrenzt dies die Chance für Selektionsvorteile resistenter Mutanten. Kombiniert ergeben diese Effekte eine messbare Abnahme von Krankheitslast und Sterblichkeit, was Studien aus Modellierungen und frühen Programmdaten bestätigen.
Die Implementierung der Typhusimpfung ist jedoch nicht nur eine wissenschaftliche Aufgabe, sondern auch logistisch komplex. Sie erfordert:
- eine verlässliche Lieferkette für Kühllogistik (Cold Chain),
- integrierte Daten- und Erfassungsmechanismen zur Überwachung von Durchimpfungsraten und Nebenwirkungen,
- Schulungen für Gesundheitspersonal und Aufklärungskampagnen, die kulturelle und sprachliche Barrieren berücksichtigen,
- sowie Finanzierungspläne, die sowohl Anschub- als auch langfristige Kosten abdecken.
Ohne diese Komponenten bleibt die reine Verfügbarkeit eines vorkqualifizierten Impfstoffs ungenutzt.
Die Frage der Kostenwirksamkeit ist für politische Entscheidungsträger zentral. Ökonomische Modellierungen, die Impfkosten, Behandlungskosten, Produktivitätsverluste und langfristige Effekte durch vermiedene Resistenzen berücksichtigen, zeigen häufig, dass die Einführung von Typhus-Konjugatimpfstoffen in endemischen städtischen Gebieten langfristig kostensparend sein kann. Diese Modellrechnungen variieren je nach Annahmen zur Übertragungsdynamik, Impfstoffwirksamkeit und Programmdurchführung, doch die Tendenz ist konsistent: Frühzeitige Impfprogramme können hohe direkte und indirekte Kosten vermeiden.
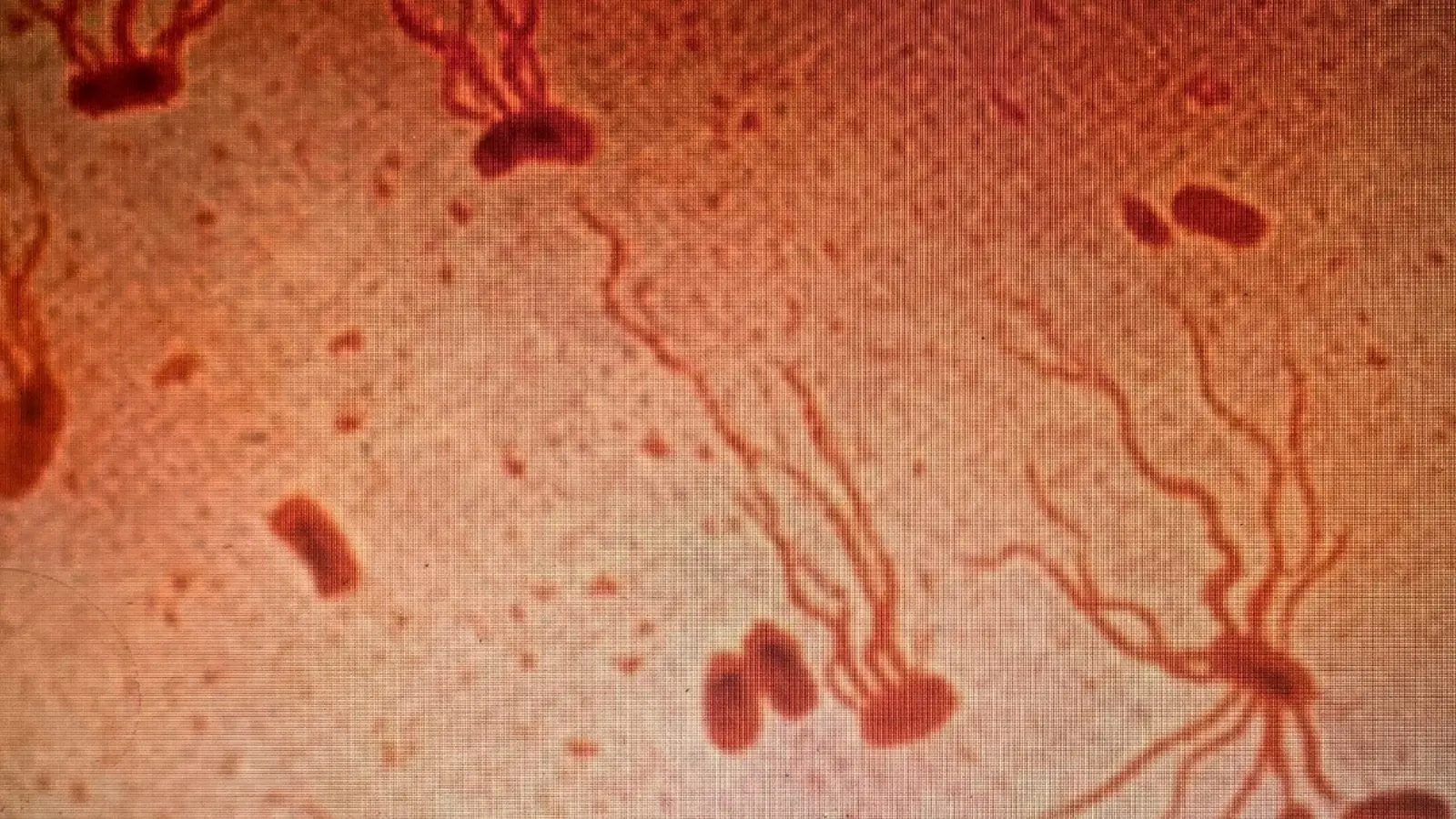
Technische Aspekte der Impfstoffe selbst verdienen besondere Beachtung. Typhus-Konjugatimpfstoffe (TCVs) koppeln Vi-Kapselantigene an Trägerproteine, wodurch sie bei Kleinkindern robuste und langlebigere Immunantworten induzieren können als frühere Polysaccharid-Impfstoffe. Die Immunität umfasst sowohl humorale als auch zelluläre Komponenten und reduziert die Kolonisationsdichte und damit die Übertragungswahrscheinlichkeit.
Wissenschaftliche Studien zeigen, dass TCVs bei Kindern ab 6 Monaten wirksam sind. Die Dauer des Schutzes wird weiterhin überwacht, aber Daten legen nahe, dass eine Einzeldosis bei Kleinkindern mehrere Jahre Schutz bieten kann, was sie für die Aufnahme in Routine-Kinderschutzprogramme attraktiv macht. Ergänzende Kampagnen, die zunächst eine breite Alterskohorte abdecken, können die kurzfristige Immunität in der Bevölkerung schnell erhöhen und so die Auswirkungen auf die Übertragung beschleunigen.
Ein weiterer zentraler Punkt ist die Überwachung resistenter Salmonella Typhi-Stämme. Fortschrittliche molekulare Surveillance-Methoden – einschließlich Ganzgenom-Sequenzierung – ermöglichen die frühe Erkennung von Ausbreitungen multiresistenter oder sogar extrem resistenter Klone. Wenn Impfprogramme mit robusten Surveillance-Systemen gekoppelt sind, lassen sich nicht nur kurzfristige Erfolge messen, sondern auch Hinweise auf veränderte Resistenzmuster erkennen, die eventuell adaptierte Therapieleitlinien erforderlich machen.
Praktische Erfahrungen aus Pakistan und anderen Programmen liefern wertvolle operative Erkenntnisse. Beispiele umfassen:
- Zielgerichtete Kommunikation: Lokale Meinungsbildner, Gesundheitsfachkräfte und Elternnetzwerke sind entscheidend, um Vertrauen zu schaffen und Fehlinformationen zu begegnen.
- Priorisierung urbaner Hotspots: Da die Modellierung in Indien besonders hohe Effekte in städtischen Gebieten zeigte, empfiehlt sich eine strategische Priorisierung dort, wo Übertragungsdichte und Gesundheitsbelastung am höchsten sind.
- Integration in bestehende Routinen: Die Verknüpfung mit etablierten Kindesimpfprogrammen reduziert Marginalkosten und verbessert die Akzeptanz.
Diese Elemente zeigen: Es geht nicht nur darum, Impfstoffdosen bereitzustellen, sondern Programme so zu designen, dass sie nachhaltig, nachvollziehbar und anpassungsfähig sind.
Auf globaler Ebene spielen multilaterale Akteure und Finanzierungseinrichtungen eine Schlüsselrolle. Organisationen wie die WHO, Gavi (die Impfallianz) und regionale Gesundheitsnetzwerke können Anschubfinanzierung, technische Unterstützung und Mechanismen zur Preisverhandlung bereitstellen. Solche Unterstützung ist besonders wichtig für Länder mit begrenzten Ressourcen, die sonst Schwierigkeiten hätten, Impfprogramme zu starten oder aufrechtzuerhalten.
Politische Entscheidungsträger müssen zudem die Balance finden zwischen kurzfristigen Budgetzwängen und langfristigen Gesundheitsgewinnen. Ein Beispiel: Die anfänglichen Ausgaben für Impfstoffbeschaffung und Kampagnenlogistik können durch vermiedene Behandlungskosten, reduzierte Krankenhausaufenthalte und niedrigere Langzeitfolgekosten für Familien und Gesundheitssysteme mehr als ausgeglichen werden. Klar quantifizierbare Budget-Impact-Analysen helfen dabei, Vorbehalte abzubauen und Investitionen zu rechtfertigen.
Es gibt auch ethische Überlegungen: In Regionen mit hoher Typhuslast sind die gesundheitlichen Vorteile von Impfprogrammen oft ungleich verteilt – arme, dicht besiedelte städtische Gemeinden tragen die Hauptlast. Prioritäre Impfprogramme in diesen Gebieten sind daher nicht nur epidemiologisch sinnvoll, sondern auch gesellschaftlich gerecht.
Forschungslücken bestehen weiterhin. Offene Fragen umfassen die optimale Altersstruktur für Routine- und Auffrischimpfungen, die langfristige Persistenz des Impfschutzes in verschiedenen Endemizitätskontexten und die Wechselwirkung zwischen Impfprogrammen und Antibiotikaverbrauch auf Gemeindeebene. Solche Fragen lassen sich durch engmaschige Datensammlung, Kohortenstudien und adaptive Programmgestaltung beantworten.
Technologie und Innovation können zusätzliche Hebel bieten: digitale Registrierungs- und Erinnerungssysteme erhöhen die Durchimpfung, mobile Gesundheitslösungen erlauben flexible Kampagnen in informellen Siedlungen, und kosteneffiziente Labornetzwerke unterstützen lokale Surveillance. All diese Elemente zusammen verbessern die Effizienz und Messbarkeit von Programmen.
Schließlich ist die gesellschaftliche Dimension nicht zu unterschätzen. Vertrauen in Impfstoffe ist fragil und von lokalen Erfahrungen, historischen Ereignissen und der Wahrnehmung des Gesundheitssystems geprägt. Transparente Kommunikation, partizipative Planung und die Einbindung lokaler Gesundheitsarbeiter sind deshalb entscheidend, um hohe Impfquoten zu erreichen und langfristig aufrechtzuerhalten.
Die Strategie ist klar: Wir brauchen ein kombiniertes Maßnahmenpaket aus Impfstoffeinführung, Überwachung resistenter Stämme, Investitionen in neue Antibiotika, Stärkung der Gesundheitssysteme und gezielter Kommunikation. Jedes Element verstärkt die anderen; zusammen schaffen sie Resilienz gegenüber einer sich verschärfenden Resistenzlage.
Die Zeit drängt. Länder, Gesundheitsorganisationen und Förderer müssen jetzt handeln, um die Chance zu nutzen, die Typhus-Konjugatimpfstoffe bieten: einen unmittelbaren Schutz für Kinder, eine Reduktion des Antibiotikaverbrauchs und damit ein wirksames Mittel im Kampf gegen Antibiotikaresistenz.
Wer jetzt investiert, schützt nicht nur die Gesundheit der nächsten Generationen, sondern bewahrt auch die Wirksamkeit lebenswichtiger Antibiotika für die Zukunft.
Quelle: sciencealert

Kommentar hinterlassen