7 Minuten
Atradimo santrauka: paslėptas receptorius, reguliuojantis kaulų tvirtumą
Leipcigo universiteto tyrėjai identifikavo iki šiol mažiau vertintą receptorių — GPR133 — veikiančią kaip molekulinį „kaulų jungiklį“, kontroliuojantį skeleto tvirtumą. Laboratoriniuose tyrimuose su pelėmis aktyvavus GPR133 nauju mažu molekuliu vadinamu AP503 padidėjo kaulų tankis ir buvo atstatyti pokyčiai, panašūs į osteoporozę. Šis tyrimas nurodo naują biologinį taikinį terapijoms, galinčioms tiek išsaugoti, tiek atstatyti kaulus — svarbų poreikį senstančiose populiacijose.
Kodėl naujos osteoporozės gydymo priemonės yra skubiai reikalingos
Osteoporozė yra lėtinė būklė, kuriai būdingas palaipsnis kaulų masės praradimas ir mikroarchitektūros blogėjimas, didinantis lūžių riziką. Vien Vokietijoje šia liga serga maždaug šeši milijonai žmonių, daugiausia moterys, ypač po menopauzės. Dabartiniai gydymo būdai, tokie kaip bisfosfonatai, denosumabas ar anaboliniai agentai (teriparatidas, romosozumabas), gali sumažinti lūžių riziką, tačiau turi apribojimų — šalutiniai poveikiai, ribota vartojimo trukmė ir nevisiškas kaulo kokybės atstatymas. Reikia saugesnių, ilgalaikių strategijų, kurios tiek apsaugotų nuo kaulų netekimo, tiek atkurtų skeleto integralumą.
Siekiant rasti alternatyvų su geresniu saugumo ir efektyvumo profiliu, mokslininkai tiria naujus molekulinius taikinius kaulų biologijoje. Vienas perspektyvus taikinys yra GPR133, adhezijos G baltymų receptorių (adhesion GPCR) klasės narys, iki šiol santykinai mažai tirtas kaulų remodeliavimo kontekste.
Mechanizmas: kaip GPR133 aktyvavimas pertvarko kaulus
GPR133 priklauso membraninių baltymų klasei, vadinamai adhezijos G baltymų receptoriais. Šios molekulės aktyvuojamos mechaniniais signalais ir ląstelių tarpusavio kontaktais bei perduoda signalus viduje per G baltymus. Kaulų audinyje GPR133 aktyvavimas sukelia kaskadą, kuri didina osteoblastų — naują kaulą formuojančių ląstelių — aktyvumą, tuo pačiu slopindama osteoklastų — kaulų rezorbciją vykdančių ląstelių — veiklą. Nukreipdamas pusiausvyrą link kaulo formavimo, GPR133 signalizavimas stiprina kaulų struktūrą ir didina jos patvarumą.
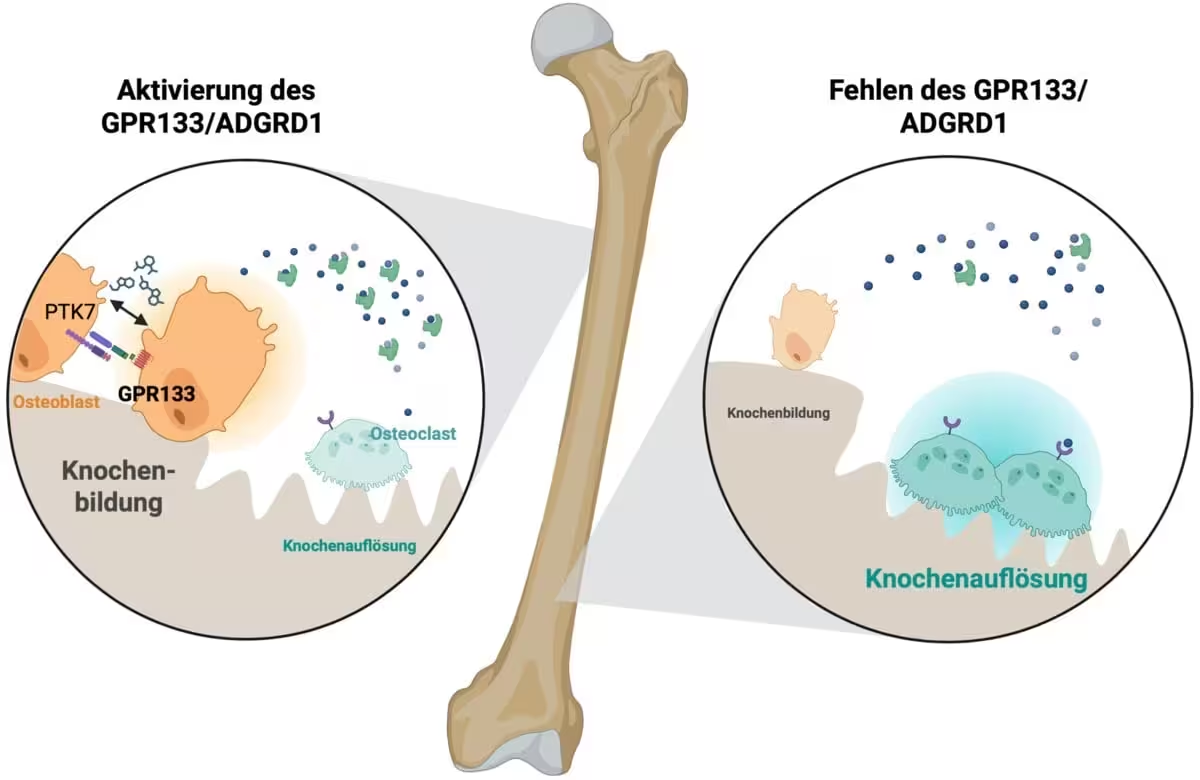
Aktyvavus GPR133 kaulų audinyje, generuojamas signalas, kuris skatina kaulą formuojančias ląsteles (osteoblastus) ir slopina kaulą rezorbuojančias ląsteles (osteoklastus). Šaltinis: Biorender, Ines Liebscher
Rudolfo Schönheimerio biochemijos institute atlikti laboratoriniai eksperimentai parodė, kad GPR133 genetinis sutrikimas pelėse sukelia ankstyvą kaulų tankio sumažėjimą — fenotipą, atspindintį tam tikras žmogaus osteoporozės ypatybes. Priešingai, farmacologinis receptoriaus stimuliavimas naudojant AP503 — atrastą skaičiavimo paieškos būdu — lėmė reikšmingą kaulų masės padidėjimą ir pagerino skeleto mechanines savybes tiek sveikuose, tiek osteoporoziniuose gyvūnų modeliuose.
Aktyvavimo būdai: mechaninis įtempis ir ląstelių sąveikos
GPR133 reaguoja į mechaninį įtempį ir į signalus, kylančius iš tiesioginių kaulų ląstelių sąveikų. Ši dviguba jautrumo savybė rodo, kad receptorius veikia kaip fiziologinis integratorius, apjungiantis fizinę apkrovą (manipuliaciją, svorio laikymą) ir vietinį tarp ląstelių signalizavimą, paverčiant šiuos signalus anaboliniais (kaulą kuriamaisiais) atsakais.
Tyrimo rezultatai ir eksperimentiniai duomenys
Leipcigo tyrime mokslininkai derino molekulinės genetikos, ląstelių biologijos ir in vivo farmakologijos metodus. Pagrindinės išvados:
- Pelės su sumažinta GPR133 funkcija jauname amžiuje išsivystė su mažesne kaulų mase, kas rodo, kad receptorius reikalingas normaliam kaulų kaupimuisi ir palaikymui.
- AP503, mažos molekulės agonistas, atrastas aukšto pralaidumo skaičiavimo ekranu, selektyviai stimuliavo GPR133 ir atkartojo jo natūralų anabolinį signalą kauluose.
- Gydymas AP503 padidino kaulų mineralinį tankį, pagerino mikroarchitektūrą ir atstatė osteoporozę primenančius pokyčius gydytose pelėse.
Šie priešklinikiniai rezultatai remia idėją, kad taikant GPR133 galima tiek užkirsti kelią su amžiumi susijusiam kaulų netekimui, tiek aktyviai atstatyti prarastą kaulą. Be to, ankstesni tos pačios grupės darbai parodė, kad AP503 taip pat stiprina skeletinį raumenį, kas numato koordinuotą naudą raumenų ir kaulų sveikatai — pageidautina savybė intervencijoms, skirtoms silpniems vyresnio amžiaus pacientams.
Klinikinės implikacijos ir plėtros iššūkiai
GPR133 ir AP503 identifikacija atveria vertimo kelią, tačiau kartu kelia ir įprastus iššūkius:
- Saugumas ir specifiškumas: būtina išsamiai įvertinti AP503 selektyvumą GPR133 atžvilgiu ir galimų šalutinių taikinių profilį. Ilgalaikė GPCR signalizavimo moduliacija reikalauja kruopščių toksikologinių tyrimų.
- Farmakokinetika ir pristatymas: gali prireikti cheminio optimizavimo, kad būtų užtikrintas geras geriamasis prieinamumas, metabolinis stabilumas ir tinkamas dozavimo režimas žmonėms.
- Efektyvumas didesniuose žinduoliuose ir žmonėse: pelių modeliai yra informatyvūs, bet nevisiškai atspindi žmogaus kaulų remodeliavimo dinamiką. Reikės tyrimų su didesniais gyvūnais ir galiausiai etapinių klinikinių tyrimų, kad būtų įvertintas lūžių rizikos sumažėjimas ir funkciniai rezultatai.
Kadangi dabartiniai standartiniai vaistai jau mažina lūžių riziką, bet koks naujas gydymas turi parodyti arba pranašesnį efektyvumą, arba geresnį saugumo profilį ilgalaikiam vartojimui, arba unikalią naudą, pvz., vienu metu stiprinant raumenis. Galimybė tiek apsaugoti nuo kaulų netekimo, tiek regeneruoti prarastą kaulą daro GPR133 labai patraukliu farmacinės plėtros taikiniu.
Fonas ir tyrimų kontekstas: dešimtmetis GPCR studijų Leipcige
Leipcigo universitetas daugiau nei dešimtmetį investuoja į adhezijos GPCR struktūros ir funkcijos tyrimus per Bendradarbiavimo tyrimų centrą 1423 „GPCR aktyvacijos ir signalizacijos struktūrinė dinamika“. Šis ilgalaikis, kryptingas darbas padarė universitetą tarptautiniu adhezijos GPCR tyrimų centru ir sudarė sąlygas daugiadisciplininiams metodams, kurie atskleidė GPR133 vaidmenį kaulų biologijoje.
„Jei šis receptorius yra pažeistas dėl genetinių pokyčių, pelės ankstyvame amžiuje rodo kaulų tankio sumažėjimą – panašų į osteoporozę žmonėms. Naudodami medžiagą AP503, kuri tik neseniai buvo identifikuota kompiuterinio ekrano būdu kaip GPR133 stimuliatorius, mums pavyko žymiai padidinti kaulų tvirtumą tiek sveikose, tiek osteoporozinėse pelėse“, — paaiškina profesorė Ines Liebscher, pagrindinė tyrimo vadovė iš Rudolfo Schönheimerio biochemijos instituto Medicinos fakultete.
Ekspertų įžvalga
Dr. Martin Keller, fiktyvus translacinis farmacologas ir vyresnysis R&D patarėjas, turintis patirties raumenų ir kaulų vaistų kūrime, komentuoja: „Taikyti adhezijos GPCR, tokius kaip GPR133, yra protinga strategija, nes šie receptoriai stovi sąsajoje tarp mechaninių stimulusų ir ląstelinės reakcijos. Junginys, galintis saugiai imituoti fizinio krūvio signalizavimą ir pasukti remodeliavimą link kaulo formavimo, galėtų pakeisti ilgalaikį osteoporozės gydymą — ypač pacientams, kurie negali toleruoti dabartinių terapijų. Kelias nuo pelės prie rinkos yra ilgas, tačiau dviguba raumenų ir kaulų nauda, aprašyta šiame darbe, yra ypač patraukli geriatrijos priežiūrai.“
Kiti žingsniai ir ateities perspektyvos
Leipcigo komanda vykdo kelis tarpinio etapo projektus, kad detaliau apibrėžtų AP503 mechanizmą ir ištirtų receptoriaus vaidmenį kituose ligų modeliuose. Svarbūs tolesni žingsniai:
- Dozės–atsako ir lėtinio vartojimo tyrimai, siekiant įvertinti ilgalaikį poveikį ir saugumą.
- Struktūriniai tyrimai, kad suprastų, kaip AP503 prisijungia ir aktyvuoja GPR133, palengvinant racionalų vaistų optimizavimą.
- Tyrimai didesniuose gyvūnuose, geriau prognozuojant žmonėms taikytiną farmakologiją.
- Ankstyvos fazės klinikinė plėtra, jei priešklinikinis saugumas ir efektyvumas bus patvirtinti.
Jei šie planai bus sėkmingai įgyvendinti, GPR133 agonistai galėtų tapti kitos kartos osteoporozės terapijos dalimi, ypač po menopauzės moterims ir vyresnio amžiaus žmonėms, kuriems gresia trapuminių lūžių rizika.
Išvados
GPR133 atradimas kaip kaulų stiprumą reguliuojančio veiksnio ir mažos molekulės aktyvatoriaus AP503 parodymas, kad jis gali padidinti kaulų tankį ir atstatyti osteoporozę primenančius pokyčius pelėse, yra perspektyvus žingsnis kaulų biologijos srityje. Remiantis dešimtmečiu adhezijos GPCR tyrimų Leipcigo universitete, šis darbas suteikia naują terapinį taikinį ir koncepcinę bazę intervencijoms, integruojančioms mechaninius ir ląstelių signalus, siekiant atstatyti ir išsaugoti skeleto sveikatą. Nors vertimas į žmogaus gydymus reikalauja išsamių tolesnių tyrimų, gebėjimas stiprinti tiek kaulus, tiek raumenis kelia GPR133 moduliavimą kaip prioritetinį kelią kovojant su amžiaus nulemtu raumenų ir kaulų silpnumu.
Mokslininkai rado „kaulų jungiklį“, kuris galėtų sustabdyti osteoporozę ir išlaikyti kaulus stiprius senstant. Šaltinis: Shutterstock
Aktyvavus GPR133 kaulų audinyje, generuojamas signalas, kuris skatina kaulą formuojančias ląsteles (osteoblastus) ir slopina kaulą rezorbuojančias ląsteles (osteoklastus). Šaltinis: Biorender, Ines Liebscher
Quelle: scitechdaily

Kommentar hinterlassen