8 Minuten
Forscher haben einen Stamm von Darmbakterien aus dem Japanischen Laubfrosch identifiziert, der bei Mäusen einen dramatischen Tumorrückgang auslösen kann und damit auf eine überraschende neue Richtung in der Krebsforschung hinweist. Ein Bakterienstamm, Ewingella americana, verringerte nicht nur die Tumorgröße, sondern löschte die Tumore bei behandelten Tieren vollständig aus und löste gleichzeitig eine anhaltende Immunantwort aus. Diese Beobachtung eröffnet zugleich Fragen zur Wirkungsweise, zu Sicherheitsaspekten und zum Potenzial mikrobieller Therapeutika in der Onkologie.
Von Teich‑Mikrobiomen zu Anti‑Krebs‑Kandidaten
Amphibien und Reptilien fallen durch eine vergleichsweise niedrige Krebshäufigkeit auf, ein Umstand, der Wissenschaftlerinnen und Wissenschaftler am Japan Advanced Institute of Science and Technology dazu veranlasste, das Darmmikrobiom dieser Tiere gezielt nach therapeutischen Hinweisen zu durchsuchen. Das Team isolierte Bakterien aus dem Darm von Fröschen, Molchen und Eidechsen und wählte 45 Stämme zur weiterführenden Laborprüfung aus. Neun dieser Stämme zeigten in Mausmodellen messbare tumorsuppressive Effekte — doch ein Kandidat hob sich deutlich hervor: Ewingella americana, isoliert aus dem Japanischen Laubfrosch (Dryophytes japonicus).
Im Gegensatz zu vielen experimentellen Wirkstoffen, die ausschließlich das Tumorwachstum verlangsamen, führte bereits eine einmalige Applikation von E. americana zum vollständigen Verschwinden etablierter Tumore bei behandelten Mäusen. Als die Forschenden 30 Tage später Krebszellen erneut in diese Tiere einbrachten, entwickelten sich für mindestens einen weiteren Monat keine Tumore, was auf einen anhaltenden schützenden Effekt und nicht bloß auf eine vorübergehende Hemmung hindeutet. Diese Ergebnisse deuten nicht nur auf unmittelbare antitumorale Effekte hin, sondern auch auf eine mögliche Bildung einer immunologischen Erinnerung gegen die Tumorzellen.
Die Auswahl von Amphibien und Reptilien als Quelle war bewusst: Diese Organismen leben oft in mikrobiellen und ökologischen Nischen mit hoher Selektionsdrucksrate, in denen Mikroben Überlebensstrategien gegen Umwelteinflüsse entwickelt haben. Solche Anpassungen können Eigenschaften hervorbringen, die in der Tumorforschung wertvoll sind, zum Beispiel die Fähigkeit, in sauerstoffarmen (hypoxischen) Umgebungen zu persistieren oder spezifische immunmodulierende Moleküle zu produzieren. Das gezielte Screening von Biodiversität — hier des Amphibien‑Mikrobioms — stellt damit eine vielversprechende Ergänzung zu klassischen Wirkstoffforschungspipelines dar.
Wie die Bakterien Tumore angreifen und die Immunantwort stärken
Nachfolgende Analysen deuten darauf hin, dass E. americana eine zweigleisige Strategie verfolgt. Zum einen scheint der Stamm direkt Tumorgewebe unter den niedrigen Sauerstoffbedingungen anzusprechen, die in vielen soliden Tumoren herrschen. Zum anderen stimuliert er das Wirtsimmunsystem. Bei den behandelten Tieren wurde eine erhöhte Aktivität zentraler Immunzelltypen beobachtet — insbesondere T‑Zellen, B‑Zellen und Neutrophile — die eine Schlüsselrolle in antitumoralen Immunantworten spielen. Zusammengefasst schwächt das Bakterium offenbar sowohl das Tumormikroumfeld als auch rekrutiert und aktiviert Immunzellen, die das Tumorgewebe endgültig eliminieren können.
Detailliertere Immunanalysen zeigten Veränderungen in der Zellzusammensetzung des Tumormikroumfelds und erhöhte Expression entzündungsfördernder Zytokine, die auf eine Verschiebung hin zu einer immunaktivierenden Umgebung hindeuten. Solche Veränderungen können eine zuvor immunsuppressive Tumorumgebung umformen, sodass adaptive Immunantworten effektiver Tumorzellen erkennen und zerstören können. Darüber hinaus legen In-vitro‑Experimente nahe, dass E. americana auch direkte zytotoxische Effekte auf Tumorzellen haben könnte, möglicherweise durch sekretion von bakteriellen Faktoren oder durch Modulation metabolischer Bedingungen im lokalen Gewebe.
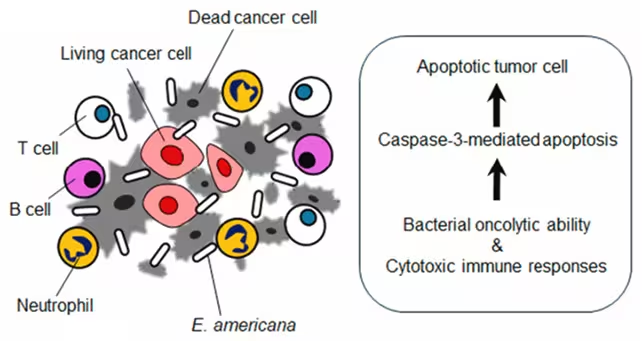
Die Bakterien scheinen die Hilfe von Immunzellen zu gewinnen, um Krebs zu bekämpfen.
Die Forschenden vermuten, dass E. americana Anpassungen an sauerstoffarme Umgebungen entwickelt hat — eine Eigenschaft, die ihm erlaubt, in Tumoren zu persistieren und dort aktiv zu werden, wo Immunfunktionen und die Wirkung von Chemotherapien häufig eingeschränkt sind. Diese ökologische Einsicht — aus Organismen zu lernen, die an extreme Mikroumgebungen angepasst sind — unterstreicht das bislang wenig genutzte Potenzial der Biodiversität für die Wirkstoffentdeckung und die Entwicklung neuartiger Krebstherapien.
Technische Untersuchungen zur Genomik und zum Sekretom des Stammes sind bereits geplant oder im Gange. Durch Genomsequenzierung, Transkriptomanalysen und Proteomstudien wollen die Wissenschaftlerinnen und Wissenschaftler die molekularen Determinanten identifizieren, die für die Tumorzielgerichtetheit und die Immunaktivierung verantwortlich sind. Insbesondere interessieren Fragen wie: Welche bakteriellen Gene werden in hypoxischen Bedingungen hochreguliert? Welche sekretorischen Effekte modulieren Immunzellen? Und lassen sich diese Faktoren isolieren oder synthetisch nachbauen, um Sicherheitsrisiken zu minimieren?
Sicherheitsdaten aus den vorläufigen Tierversuchen sind ermutigend. Der Bakterienstamm wurde schnell aus dem Blutkreislauf eliminiert, erzeugte keine anhaltende Organtoxizität in den behandelten Mäusen und übertraf in Tumorverkleinerungsassays mehrere Standardoptionen, einschließlich des Chemotherapeutikums Doxorubicin. Trotzdem warnen die Autorinnen und Autoren, dass E. americana unter bestimmten Bedingungen Infektionen beim Menschen verursachen kann; deshalb wird die Sicherheit zentrale Bedeutung haben, wenn ein Weg zu klinischen Studien eingeschlagen werden soll. Dies umfasst sowohl die Kontrolle der Bakterienlast als auch mögliche genetische Modifikationen zur Attenuierung von Pathogenitätsfaktoren.
Folgen, nächste Schritte und Herausforderungen
Das Team plant ergänzende Experimente, um E. americana in verschiedenen Krebsarten und in Kombination mit anderen Therapien zu testen sowie die Methoden der Verabreichung zu optimieren. Wesentliche offene Fragen bleiben: Lässt sich die bakterielle Wirkung in größeren Tiermodellen und letztlich beim Menschen reproduzieren? Welche molekularen Faktoren von E. americana treiben die Immunaktivierung und die direkten Tumoreffekte an? Können diese Faktoren isoliert, standardisiert oder gentechnisch so modifiziert werden, dass sie in sicheren, regulierbaren therapeutischen Produkten genutzt werden können?
Bei der Übertragung mikrobieller Therapien in die klinische Anwendung stehen Forscherinnen und Forscher vor mehreren Hürden: regulatorische Vorgaben für lebende mikrobiologische Therapeutika, Anforderungen an die Qualitätskontrolle, die Notwendigkeit robuster Sicherheitsdaten und die Entwicklung geeigneter Formulierungen und Liefervehikel. Live‑Bakterientherapien sind jedoch kein rein hypothetisches Konzept — bereits heute wird eine lebende Bakterientherapie zur Behandlung bestimmter Blasenkrebse eingesetzt. Die aktuellen Ergebnisse aus der Studie in Gut Microbes (Iwata et al., 2025) zeigen sowohl das Potenzial als auch den Vorsichtsbedarf, der beim Übergang von Laborversuchen zu klinischen Anwendungen notwendig ist.
Wichtig ist auch die Frage nach der Standardisierung und Reproduzierbarkeit: Natürliche Bakterienstämme variieren je nach Isolat und Umweltbedingungen, daher müssen Protokolle entwickelt werden, die gleichbleibende Wirkungen gewährleisten. Dies kann durch die Auswahl einer definierten Produktcharge, durch Genotypisierung und durch Validierung unter GMP‑Bedingungen (Good Manufacturing Practice) erreicht werden. Parallel dazu sind robuste präklinische Modelle erforderlich, um Dosis‑Wirkungsbeziehungen, Pharmakokinetik und -dynamik sowie potenzielle Nebenwirkungen umfassend zu charakterisieren.
Weiterhin wird die Interaktion mit bestehenden Krebstherapien untersucht: Könnte eine Kombination aus E. americana und Checkpoint‑Inhibitoren, Strahlentherapie oder konventioneller Chemotherapie synergetische Effekte hervorbringen? Erste Hypothesen gehen davon aus, dass eine bakterielle Umformung des Tumormikroumfelds die Empfindlichkeit gegenüber immunbasierten Therapien erhöhen könnte. Solche Kombinationen müssten jedoch sorgfältig auf Verträglichkeit und mögliche unerwünschte Wechselwirkungen geprüft werden.
Experteneinschätzung
„Einen Bakterienstamm zu finden, der sowohl Tumore angreift als auch die adaptive Immunität verstärkt, ist selten und sehr vielversprechend“, sagt Dr. Elena Park, eine Krebsimmunologin, die an der Studie nicht beteiligt war. „Die ökologische Strategie von Organismen, die an hypoxische Nischen angepasst sind — etwa einige Darmmikroben amphibischer Wirte — bietet eine neue Perspektive für therapeutische Konzepte. Gleichzeitig erfordert das Arbeiten mit lebenden Bakterien eine sorgfältige Abwägung von Wirksamkeit und Sicherheit. Eine mögliche Alternative ist die Identifikation und Isolierung aktiver Moleküle für die Entwicklung klassischer Arzneimittel, um das Infektionsrisiko zu minimieren.“
Weitere Stimmen aus der Fachwelt betonen die Bedeutung interdisziplinärer Zusammenarbeit: Mikrobiologen, Immunologen, Onkologen und regulatorische Experten müssen gemeinsam Strategien entwickeln, die sowohl die wissenschaftliche Validität als auch die patientenspezifische Sicherheit berücksichtigen. Zudem wird hervorgehoben, dass die Erforschung natürlicher Mikrobiome die Tür zu bislang unbekannten Wirkmechanismen öffnen kann, die mit synthetischen Ansätzen allein schwer zu identifizieren wären.
Fazit
Die Entdeckung der anti‑tumoralen Aktivität von Ewingella americana bei Mäusen unterstreicht den Wert, vielfältige mikrobielle Ökosysteme nach neuen Therapiekandidaten zu durchsuchen. Obwohl die Überführung in die Humanmedizin noch weitreichend und komplex ist, eröffnet die Studie eine neue Richtung für Immuntherapien und zielgerichtete Tumoransätze — eine Richtung, die das Instrumentarium zur Behandlung hartnäckiger Krebserkrankungen langfristig erweitern könnte. Die Erhaltung von Biodiversität, so betonen die Autorinnen und Autoren, ist dabei nicht nur eine ökologische Verpflichtung, sondern auch eine Strategie zur Bewahrung potenzieller medizinischer Entdeckungen der Zukunft.
Insgesamt zeigt diese Forschung, wie wichtig es ist, ökologische Prinzipien und moderne biomedizinische Methoden zu verbinden. Weitere Untersuchungen — von Genomanalysen bis zu präklinischen Sicherheitsstudien — werden klären müssen, ob und wie sich ein Frosch‑Darmbakterium sicher und effektiv in der Onkologie anwenden lässt. Bis dahin bleibt die Studie ein Beispiel dafür, wie unerwartete Quellen und interdisziplinäre Forschung neue Wege in der Krebstherapie aufzeigen können.
Quelle: sciencealert


Kommentar hinterlassen