8 Minuten
Neue Forschungsergebnisse der McGill University stellen eine zentrale Annahme über Dopamin und Bewegung in Frage. Anstatt als momentane Steuerungseinheit dafür zu fungieren, wie schnell oder kraftvoll eine Bewegung ausgeführt wird, könnte Dopamin die stabilen Hintergrundbedingungen liefern, die Bewegungen überhaupt ermöglichen — eine Erkenntnis mit direkten Folgen für die Behandlung der Parkinson-Krankheit.
Ein Umdenken zur motorischen Vitalität
Jahrzehntelang haben Neurowissenschaftler Dopamin mit motorischer Vitalität in Verbindung gebracht — also mit Geschwindigkeit und Kraft freiwilliger Bewegungen. Bei der Parkinson-Krankheit geht der fortschreitende Verlust dopaminerger Neurone mit verlangsamten Bewegungen, Zittern und Gleichgewichtsstörungen einher. Klinisch hat diese Verbindung Therapien angetrieben, die auf die Wiederherstellung der Dopamin-Signalübertragung abzielen, allen voran Levodopa, das weiterhin die wirksamste symptomatische Behandlung darstellt.
Die neue Studie, veröffentlicht in Nature Neuroscience und geleitet von Nicolas Tritsch am Douglas Research Centre der McGill University, deutet jedoch auf eine andere Rolle hin. Anstatt als Echtzeit-"Gashebel" zu wirken, der bei jeder einzelnen Bewegung die Ausführungsgeschwindigkeit festlegt, könnte Dopamin eher wie Motoröl funktionieren: unverzichtbar für das Gesamtsystem, ohne das unmittelbar zeitlich getaktete Signal zu sein, das die Vitalität einzelner Aktionen bestimmt. "Unsere Ergebnisse legen nahe, dass wir die Rolle des Dopamins bei Bewegung neu denken sollten", sagte Tritsch. "Das Wiederherstellen eines normalen Dopaminspiegels könnte ausreichen, um die Beweglichkeit zu verbessern. Das würde die Perspektive auf Parkinson-Therapien vereinfachen." Diese Interpretation verändert die Diskussion von einer primär phasischen zu einer tonischen Sichtweise und eröffnet neue Fragen zur Biologie der Bewegungssteuerung und zur klinischen Behandlung.
Wie das Experiment die Rolle von Dopamin testete
Das Team maß die Dopamindynamik in Echtzeit, während Mäuse eine einfache motorische Aufgabe ausführten: das Drücken eines gewichteten Hebels. Für diese Messungen kombinierten die Forschenden hochsensible Aufnahmetechniken zur Darstellung von Neurotransmittern mit der Optogenetik, einer lichtgesteuerten Methode, die dopaminproduzierende Zellen in genau definierten Momenten während einer Aktion an- oder ausschalten kann. Solche experimentellen Werkzeuge erlauben es, phasische und tonische Komponenten der Dopaminantwort separiert zu untersuchen und so Ursache-Wirkungs-Beziehungen näher zu spezifizieren.
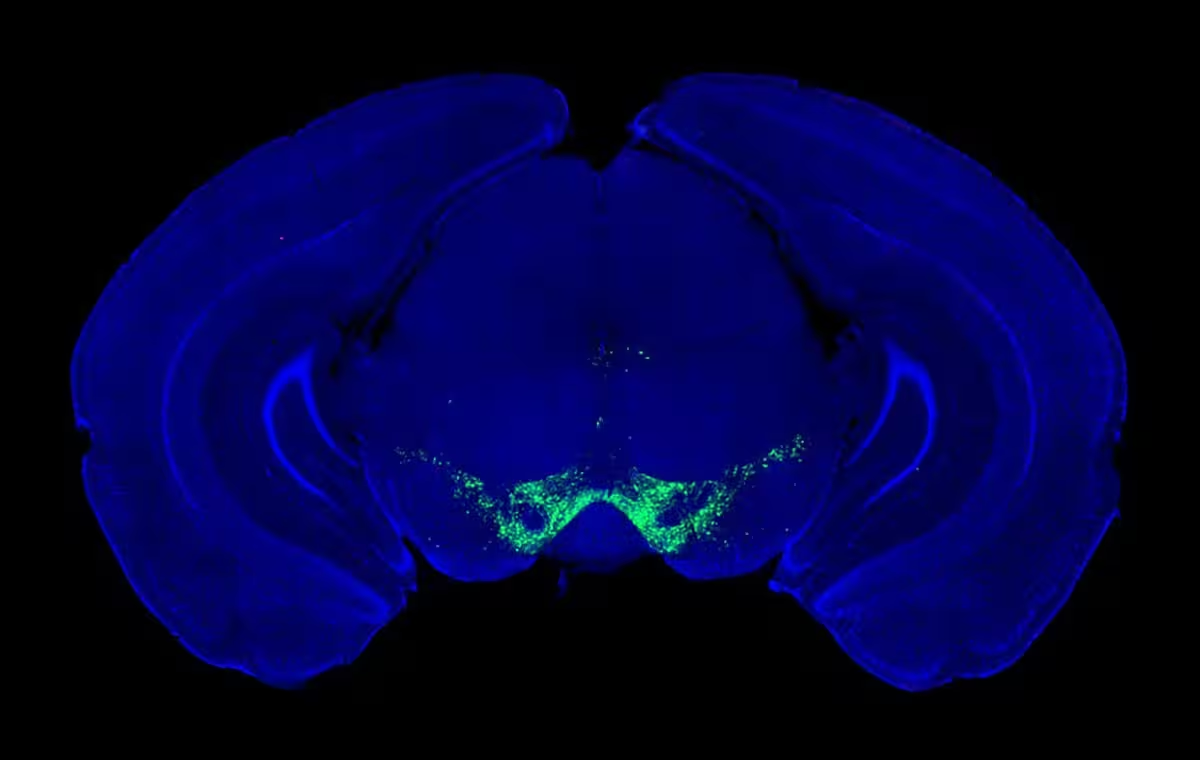
Fluoreszenzmikroskopie-Aufnahme dopaminproduzierender Neurone (grün) im Mittelhirn einer Maus.
Wäre es so, dass schnelle Dopamin-Ausbrüche (phasische Peaks) direkt die Bewegungsintensität steuerten, dann müsste das künstliche Verstärken oder Unterdrücken dieser Ausbrüche genau im Moment der Bewegung die Geschwindigkeit oder Kraft verändern. Überraschenderweise zeigten die kurzzeitigen Manipulationen keinen konsistenten Effekt auf die Vitalität einzelner Hebel-Drücke. Stattdessen beobachteten die Forschenden, dass Levodopa die Bewegung verbesserte, indem es das basale Dopamin-Niveau im Gehirn anhob — das sogenannte steady-state-Signal — ohne notwendigerweise die schnellen, bewegungsgebundenen Spitzen vollständig wiederherzustellen. Diese Befunde deuten darauf hin, dass ein ausreichender tonischer Dopaminspiegel eine permissive Bedingung für normale Bewegungen ist.
Methodisch verwendete das Team verschiedene Ansätze zur Kontrolle und Messung: neben Optogenetik und Sensoren für schnell wirkende Dopamin-Signale wurden Kalzium-Imaging und elektrophysiologische Aufzeichnungen eingesetzt, um Aktivitätsmuster in den beteiligten Schaltkreisen zu korrelieren. Solche multimodalen Datensätze erhöhen die Robustheit der Interpretation, weil sie sowohl die Neurochemie als auch die Netzwerkdynamik berücksichtigen. Zudem berücksichtigten die Forschenden Verhaltenseinflüsse wie Motivation, Anstrengung und Lernzustand der Tiere, da Dopamin auch mit Belohnungsprozessen verknüpft ist und Motivation die Bewegungsparameter modulieren kann.
Folgen für Parkinson-Therapie und Forschung
Diese Neuinterpretation wirft mehrere offene Fragen in der Parkinson-Forschung in ein neues Licht. Wenn die Verfügbarkeit von basalem Dopamin die entscheidende permissive Größe für Bewegung ist, dann könnten Therapien, die den tonischen Dopaminspiegel stabilisieren, genauso wichtig oder sogar wichtiger sein als Interventionen, die versuchen, phasische Dopaminspitzen zu imitieren. Dieses Verständnis könnte erklären, warum Levodopa, das die Gesamtverfügbarkeit von Dopamin erhöht, weiterhin so effektiv die Mobilität verbessert, auch wenn es nicht die komplexe zeitliche Struktur natürlicher Dopaminfreisetzung exakt nachbildet.
Ein therapeutischer Fokus auf die Erhaltung oder Wiederherstellung eines passenden basalen Dopaminpegels könnte mehrere Vorteile bringen. Zum einen könnte er die Notwendigkeit reduzieren, ständig phasisch zu intervenieren, was komplexe und potenziell störende Manipulationen der Hirnsignale erfordert. Zum anderen eröffnet er klarere Zielkriterien für die Medikamentenentwicklung: statt breit wirkender Dopamin-Agonisten, die global über viele Hirnkreise hinweg aktiv sind und deshalb Nebenwirkungen verursachen, wären präzisere Strategien denkbar, die tonisches Dopamin speziell in motorischen Bahnen fördern.
In der Vergangenheit wurden Dopaminrezeptor-Agonisten erprobt, doch sie riefen häufig Nebenwirkungen hervor, weil sie weitreichend auf Rezeptoren in unterschiedlichen Schaltkreisen wirkten, einschließlich solcher, die an Motivation, Kognition oder Belohnung beteiligt sind. Die Herausforderung besteht nun darin, Wirkstoffe oder Interventionen zu entwickeln, die die Basalverfügbarkeit von Dopamin modulieren, ohne unerwünschte Effekte in nicht-motorischen Netzwerken auszulösen. Mögliche Ansätze reichen von verbesserten pharmakologischen Formulierungen und gezielten Abgabesystemen bis hin zu neuartigen biologischen oder neuromodulatorischen Verfahren, die regional spezifisch wirken.
Was Forscher als Nächstes tun sollten
Weitere Forschung muss prüfen, ob die gleichen Prinzipien auch bei Primaten und Menschen gelten und wie das basale Dopamin mit anderen Neuromodulatoren sowie mit circuit-level-Veränderungen bei der Parkinson-Krankheit interagiert. Zum Beispiel könnten Serotonin, Noradrenalin oder Acetylcholin modulieren, wie ein gegebener tonischer Dopaminspiegel sich auf die Netzwerkexzitabilität und damit auf Bewegungen auswirkt. Ebenso wichtig ist die Frage, wie degenerative Prozesse, Entzündungsreaktionen und kompensatorische Plastizität in den betroffenen Schaltkreisen die Beziehung zwischen basalem Dopamin und motorischer Funktion verändern.
Für Kliniker und Wirkstoffentwickler motiviert die Studie eine erneute Konzentration auf Therapien, die den tonischen Dopamin-Tonus erhalten, sowie auf Biomarker, die den basalen — nicht nur den phasischen — Dopaminstoffwechsel widerspiegeln. Solche Biomarker könnten bildgebende Verfahren, cerebrospinale Flüssigkeitsanalysen oder neue molekulare Sensoren umfassen, die empfindlich genug sind, um stabile Konzentrationen über längere Zeiträume zu erfassen. In klinischen Studien müssten Endpunkte definiert werden, die Änderungen in baseline-orientierten Parametern validieren und mit funktionellen Verbesserungen der Motorik korrelieren.
Experimentell sind mehrere Richtungen sinnvoll: Langzeitmessungen von Dopamin in frei bewegenden Tiermodellen, Vergleiche zwischen akuten und chronischen Therapien, sowie Tests an nicht-menschlichen Primaten, um translational relevante Befunde zu gewinnen. Wichtig ist auch die Untersuchung individuell unterschiedlicher Reaktionen: Patienten mit Parkinson zeigen heterogene Verläufe und Nebenwirkungsprofile bei dopaminerg wirksamen Medikamenten, sodass passgenaue, personalisierte Ansätze zur Stabilisierung des basalen Dopaminspiegels vielversprechend erscheinen.
Technische und konzeptionelle Details
Das Konzept von tonischem versus phasischem Dopamin ist zentral für das Verständnis der Ergebnisse. Tonisches Dopamin beschreibt einen relativ stabilen Hintergrundspiegel im Extrazellulärraum, der die Erregbarkeit von Zielneuronen und die Grundbereitschaft zu handeln moduliert. Phasisches Dopamin dagegen sind kurze, zeitlich präzise freigesetzte Spitzen, die häufig mit Belohnungssignalen oder kranialen Ereignissen assoziiert werden. Die Studie legt nahe, dass das tonische Signal die Grundbedingungen setzt, unter denen phasische Signale überhaupt sinnvoll in Verhaltensänderungen umgesetzt werden können.
Auf zellulärer Ebene beeinflusst Dopamin über verschiedene Rezeptortypen (D1-ähnliche und D2-ähnliche Familien) die Aktivität von Striatumneuronen und deren Einfluss auf unmittelbare Bewegungsoutput-Kanäle. Eine angemessene tonische Dopaminpräsenz kann die Balance zwischen direkten und indirekten Bahnen der Basalganglien stabilisieren und damit die Fähigkeit des Systems unterstützen, angemessene motorische Befehle zu bilden und umzusetzen. Eine reduzierte Basalverfügbarkeit könnte diese Balance stören, was zu Hypokinese (Bewegungsverlangsamung) und anderen Parkinson-Symptomen führt.
Methodisch untermauern die kombinierten Messungen in der Studie die These, weil sie nicht nur kurzzeitige Fluktuationen aufzeichnen, sondern auch zeigen, wie sich ein über längere Zeit erhöhtes Dopaminniveau funktional auswirkt. Solche Daten sind wichtig, um pharmakologische Effekte korrekt zu interpretieren: Ein Mittel, das transient phasische Peaks nachahmt, wird sich anders auswirken als ein Mittel, das den Grundspiegel über Stunden stabil anhebt.
Potenzielle Limitationen und offene Fragen
Wie jede Untersuchung hat auch diese Studie Grenzen. Ergebnisse aus Tiermodellen lassen sich nicht uneingeschränkt auf Menschen übertragen; Unterschiede in Schaltkreisarchitektur, Lebensdauer und Komplexität des Bewegungsverhaltens können die Translation erschweren. Zudem bleibt unklar, in welchem Ausmaß motivational-affektive Effekte von Dopamin die beobachteten motorischen Veränderungen mitverursachen. Dopamin ist sowohl an Belohnung als auch an Bewegungssteuerung beteiligt, sodass disentanglieren, welche Effekte primär motorisch sind und welche sekundär über Motivation wirken, eine Herausforderung darstellt.
Auch die langfristigen Effekte einer konstant erhöhten tonischen Dopaminverfügbarkeit sind noch nicht umfassend untersucht. Chronische Dopaminmodulation kann adaptive Reaktionen in Rezeptorexpression, Signaltransduktion und neuronaler Plastizität hervorrufen. Daher sind Langzeitstudien notwendig, um Vorteile gegen mögliche Anpassungseffekte und Nebenwirkungen abzuwägen. Schließlich bleibt die Frage offen, welche patientenspezifischen Faktoren — etwa Alter, Krankheitsstadium, genetische Disposition — am stärksten darüber entscheiden, ob eine tonische oder phasische Therapie besser geeignet ist.
Schlussfolgerung
Indem der Fokus von schnellen Dopaminspitzen auf die unterstützende Rolle des basalen Dopamins verschoben wird, liefert diese Studie ein neues Rahmenmodell für das Verständnis motorischer Kontrolle und schlägt gezieltere Strategien zur Behandlung der Parkinson-Krankheit vor. Das Ergebnis ist ein klareres mechanistisches Bild, das die Bedeutung stabiler neurotransmittereller Grundlagen betont und potenziell einen einfacheren und sichereren Weg zu effektiveren Therapien eröffnet. Für Forscher, Klinik und Wirkstoffentwicklung bedeutet dies eine Verschiebung der Prioritäten hin zu Interventionen und Biomarkern, die tonische Dopaminverfügbarkeit messen und erhalten.
Quelle: scitechdaily

Kommentar hinterlassen