8 Minuten
Stellen Sie sich einen einfachen Ton vor, gespielt mit 40 Schwingungen pro Sekunde, der klebrige Gehirnproteine sanft anstößt, sodass sie dorthin wandern, wo Ärztinnen und Ärzte erreichbar sind. Die Vorstellung klingt beinahe poetisch. Doch eine aktuelle Primatenstudie legt nahe, dass ein kurzer Kurs rhythmischer Klänge genau das bewirken könnte: Beta‑Amyloid aus dem Gehirngewebe in die Cerebrospinalflüssigkeit (Liquor) zu verschieben — ein Ergebnis, das häufig als Hinweis auf verbesserte Clearance interpretiert wird.
Könnte dies ein kostengünstiges, nicht‑invasives Ergänzungsverfahren zu bestehenden Alzheimer‑Behandlungen darstellen? Forschende des Kunming Institute of Zoology (Chinese Academy of Sciences) haben genau das an Tieren untersucht, deren Gehirne in Alterungsprozessen unserem ähnlich sind. Die Untersuchung zielt auf zentrale Fragen der Alzheimer‑Forschung: Kann auditive Stimulation bei 40 Hz die Amyloiddynamik beeinflussen, die neuronale Netzwerkaktivität modulieren und damit die Mechanismen der Proteinentsorgung aktivieren? Diese Fragen sind nicht nur methodisch, sondern auch klinisch relevant, wenn es darum geht, risikoärmere und zugänglichere Interventionen zu entwickeln.

Könnte eine kostengünstige, klangbasierte Therapie eine sicherere Alternative zu aktuellen Alzheimer‑Behandlungen bieten? In gealterten Affen, die natürlicherweise Alzheimer‑ähnliche Pathologie entwickeln, fanden Wissenschaftler, dass 40‑Hz‑auditive Stimulation langanhaltende biologische Effekte zeigte, die mit Amyloiddynamik assoziiert sind.
Was die Studie tat und warum sie wichtig ist
Das Team unter Leitung von Dr. Xintian Hu arbeitete mit neun älteren Rhesusmakaken im Alter von 26 bis 31 Jahren — Tieren, die weit verbreitete Amyloidplaques entwickeln, die denen der menschlichen Alzheimer‑Erkrankung ähneln. Das Versuchsdesign war klar und methodisch präzise: Die Tiere der Behandlungsgruppe erhielten an sieben aufeinanderfolgenden Tagen jeweils eine Stunde am Tag eine 40‑Hz‑auditive Stimulation — ein 1‑kHz‑Reinton, der mit 40 Schwingungen pro Sekunde moduliert wurde. Vor der Behandlung, unmittelbar danach und erneut 35 Tage später wurden Proben der Cerebrospinalflüssigkeit (Liquor) entnommen, um biochemische Veränderungen zu verfolgen.
Die Durchführung in einem Primatenmodell erfordert spezialisierte Protokolle zur Sedierung, Stabilisierung und standardisierten Probengewinnung. Die Forschenden berichten, dass sie kontrollierte Umgebungsbedingungen, reproduzierbare Schallpegel und standardisierte Zeitpunkte für Liquorentnahmen einhielten, um biologische Variabilität zu minimieren. Zusätzlich zu den Liquoranalysen wurden bei ausgewählten Tieren elektrophysiologische Messungen und bildgebende Verfahren eingesetzt, um Veränderungen in neuronaler Oszillation, kortikaler Erregbarkeit und potenziellen Entzündungsmarkern zu evaluieren. Solche multimodalen Daten erhöhen die Aussagekraft der Befunde und erlauben erste Hypothesen über mögliche Wirkmechanismen.
Die Ergebnisse waren bemerkenswert. Die Konzentrationen von zwei Schlüssel‑Beta‑Amyloid‑Peptiden, Aβ42 und Aβ40, stiegen nach der einwöchigen Stimulation deutlich im Liquor an — Zunahmen von mehr als 200 % gegenüber dem Ausgangswert wurden berichtet. Noch überraschender: Diese erhöhten Konzentrationen blieben mehr als fünf Wochen nach dem Ende der Stimulation bestehen. Eine derartige anhaltende Reaktion wurde in Mausmodellen bisher nicht beobachtet und legt nahe, dass primate Gehirne entweder anders auf 40‑Hz‑Entrainment reagieren oder dass die zugrunde liegenden Clearance‑Mechanismen bei Primaten langlebigere Modulationen zeigen.
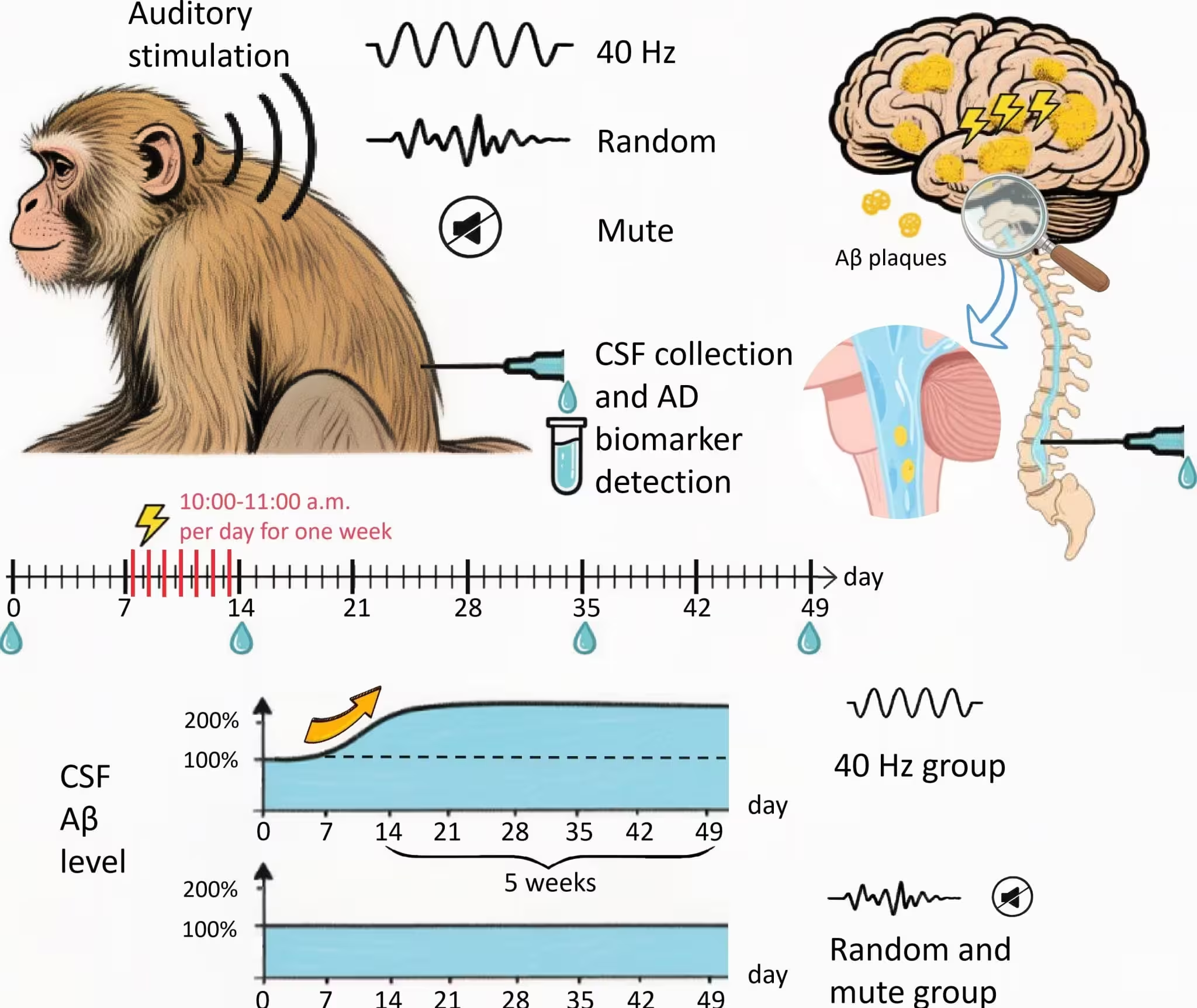
Die 40‑Hz‑auditive Stimulation führte spezifisch zu einer signifikanten Zunahme von über 200 % der Aβ42‑ und Aβ40‑Proteinwerte im Liquor gealterter Affen, die länger als fünf Wochen anhielt.
Warum ist ein Anstieg der Amyloidkonzentration im Liquor bedeutsam? In vielen experimentellen Kontexten wird ein höherer löslicher Aβ‑Spiegel im Liquor als Hinweis darauf interpretiert, dass sich die Peptidlast von unlöslichen Depositen im Gehirngewebe in ein Kompartiment verlagert hat, in dem Clearance‑Mechanismen wirken können. Anders formuliert: Bewegung, nicht vermehrte Produktion. Die Forschenden argumentieren, dass 40‑Hz‑Entrainment Pfade verstärken könnte, die aggregierte Proteine mobilisieren und zur Entfernung bereitstellen. Mögliche beteiligte Systeme sind die Mikroglia‑Aktivierung, vaskuläre Abflusswege und das glymphatische System — Komponenten, die zusammen die Homöostase und Proteinentfernung im ZNS regulieren.
Die Stabilität der Effekte über Wochen ist besonders relevant für die klinische Übersetzung: Wenn eine kurze Interventionsperiode anhaltende biologische Effekte induziert, könnten weniger häufige Behandlungszyklen ausreichen, was die Akzeptanz und Kostenstruktur verbessert. Gleichzeitig eröffnet die Langlebigkeit des Effekts wichtige Fragen über die Plastizität zellulärer und vaskulärer Clearing‑Mechanismen im alternden Gehirn.
Wie dies in die Alzheimer‑Forschung und klinische Bedürfnisse passt
Aktuelle Anti‑Amyloid‑Therapien — namentlich monoklonale Antikörper — haben in klinischen Studien gezeigt, dass sie den kognitiven Abbau verlangsamen können, bringen aber echte Risiken mit sich: zerebrale Ödeme (ARIA‑E) und Mikroblutungen (ARIA‑H) gehören zu den schwerwiegenden unerwünschten Wirkungen. Diese Nebenwirkungen bedingen oft intensive Bildgebungskontrollen und in manchen Fällen Therapieunterbrechungen. Ein nicht‑pharmakologischer Ansatz, der die körpereigenen Clearance‑Mechanismen stimuliert, könnte Nebenwirkungen reduzieren, Kosten senken und die Zugänglichkeit verbessern, falls die Wirksamkeit auf den Menschen übertragbar ist.
Ein weiterer Vorteil liegt in der Wahl des Modells: Primatengehirne sind Menschen in Struktur, Lebensdauer und Muster der Amyloidakkumulation näher als Nagetiermodelle. Das Beobachten eines robusten, langanhaltenden Effekts in gealterten Rhesusmakaken stärkt das Argument für vorsichtig gestaltete, gut kontrollierte Humanstudien. Zudem erlaubt das Primatenmodell besser die Beurteilung systemischer Reaktionen, Verhaltensänderungen und möglicher langfristiger Risiken, die bei Mäusen schwerer abzuschätzen sind.
Dennoch bleiben erhebliche Lücken bestehen. Der genaue Mechanismus hinter den anhaltenden Liquor‑Zunahmen ist nicht vollständig geklärt. Werden Mikrogliazellen dauerhaft aktiviert und räumen sie Amyloid physisch ab? Verbessert sich der vaskuläre Abfluss über perivaskuläre Räume oder das glymphatische System? Oder verändert die rhythmische Stimulation die neuronalen Netzwerkaktivitäten so, dass Amyloid besser löslich wird und in die Zirkulation übergeht? Möglicherweise wirken mehrere Mechanismen gleichzeitig. Die Studie öffnet jede dieser Fragen, anstatt sie abschließend zu beantworten, und macht deutlich, dass zusätzliche Experimente nötig sind — etwa zeitaufgelöste Bildgebung, Zell‑spezifische Markeranalysen und Manipulationen einzelner Clearance‑Pfade.
Aus klinischer Sicht muss auch die Frage der Dosis, Dauer und Sicherheitsparameter geklärt werden: Welcher Schalldruckpegel, welche Stimulationsdauer pro Sitzung und welches Behandlungsintervall sind optimal? Gibt es Alterseffekte, geschlechtsspezifische Unterschiede oder Genotyp‑abhängige Reaktionen (z. B. APOE‑ε4‑Träger)? Wie interagiert auditive 40‑Hz‑Stimulation mit bestehenden Therapien wie Antikörpern, cholinergen Medikamenten oder Lebensstilinterventionen? Solche Fragestellungen sind essenziell für die Planung von Phase‑I/II‑Studien, die Sicherheit, Verträglichkeit und biomarkerbasierte Effekte beim Menschen evaluieren.
Experteneinschätzung
„Das Anhalten erhöhter Liquor‑Amyloidwerte Wochen nach einem kurzen Kurs von 40‑Hz‑Stimulation war unerwartet“, sagt Dr. Liwen Chen, Neurologin, die nicht an der Studie beteiligt war. „Wenn dies reproduzierbar ist, deutet es auf eine Modulation langlebiger Clearance‑Pfadmechanismen hin, nicht nur auf eine vorübergehende Umverteilung. Das hat praktische Implikationen für Dosierung, Sicherheit und die Integration mit anderen Therapien.“
Solche Einschätzungen unterstreichen, dass translative Schritte sorgfältige Sicherheitstests, optimierte Stimulationsprotokolle und prädiktive Biomarker erfordern. Klinische Biomarker könnten neben Liquor‑Aβ auch MRT‑Marker (z. B. ARIA‑Screening), inflammatorische Marker und funktionelle Messungen wie EEG‑Oszillationen umfassen, um mechanistische Hinweise zu liefern. Außerdem ist prädiktive Validierung notwendig: Welche biomarkerbasierten Veränderungen korrelieren mit klinisch relevanten Verbesserungen der Kognition, des Verhaltens oder des täglichen Funktionierens?
Trotz offener Fragen ist die Idee, Klang zu nutzen — günstig, nicht invasiv und skalierbar — um dem Gehirn bei der Entfernung toxischer Proteine zu helfen, überzeugend. Sie schlägt eine neue Art von Intervention vor: eine, die gleichermaßen zuhört und behandelt. Klangbasierte Neuromodulation könnte sich ergänzend zu medikamentösen Strategien, Lebensstilmaßnahmen (wie Schlafoptimierung, die das glymphatische System beeinflussen kann) und anderen neuromodulatorischen Ansätzen (z. B. transkranieller Magnetstimulation) einfügen.
Wenn Forschende die nächsten Schritte planen, müssen Machbarkeitsstudien beim Menschen Strenge mit Dringlichkeit verbinden und eine einfache, aber entscheidende Frage beantworten: Kann rhythmischer Klang die Kognition verbessern oder den kognitiven Abbau verlangsamen, wenn er mit Biomarkern gekoppelt wird, die bedeutsame Veränderungen zeigen? Solche Studien sollten kleinere, biomarkergetriebene Endpunkte (z. B. Liquor‑Aβ, EEG‑Oszillationen, funktionelle Bildgebung) mit sicherheitsorientierten Endpunkten und explorativen kognitiven Messungen kombinieren.
Die Arbeit verspricht keine Heilung. Sie bietet ein anderes Instrument — eines, das neben Medikamenten, Lebensstiländerungen und anderen Neuromodulationsmethoden stehen könnte, um die Behandlung neurodegenerativer Erkrankungen neu zu gestalten. Wichtig ist, dass jede mögliche klinische Anwendung auf reproduzierbaren biologischen Effekten, klaren Sicherheitsprofilen und demonstrierbarer klinischer Wirksamkeit beruht. Nur dann kann eine kostengünstige auditive Intervention realistisch in Versorgungswege integriert werden und den großen Bedarf an zugänglichen Alzheimer‑Therapien adressieren.
Quelle: scitechdaily

Kommentar hinterlassen