8 Minuten
Man kann so lange laufen, bis die Beine streiken, doch das Blut könnte früher aufgeben. Dieses schonungslose Bild stammt aus einer neuen Studie, die Elite-Läufer bei zwei sehr unterschiedlichen Wettbewerben verfolgte: einem rund 40 Kilometer langen Rennen und dem zermürbenden Ultra-Trail du Mont Blanc, einem 171 Kilometer langen Ausdauertest. Die Forschenden stellten fest, dass mit zunehmender Distanz — und kumulativem Stress — auch Hinweise darauf zunahmen, dass rote Blutkörperchen (Erythrozyten) altern und ihre Beweglichkeit sowie Funktionseffizienz verlieren.
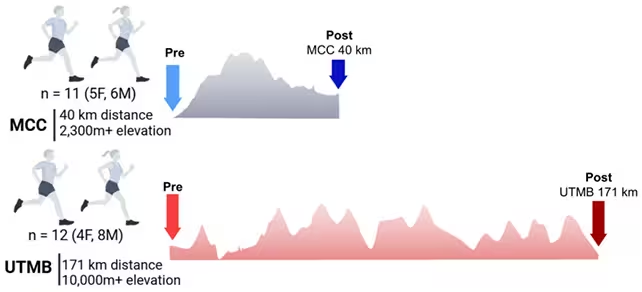
Blutproben von Läufern zweier verschiedener Rennen wurden analysiert.
Studienaufbau und zentrale Ergebnisse
Ein internationales Forscherteam sammelte Blutproben von 23 Elite-Athletinnen und -Athleten unmittelbar vor sowie direkt nach den Wettbewerben. Die teilnehmenden Sportlerinnen und Sportler liefen entweder das Rennen Martigny–Combes à Chamonix (etwa 40 km) oder den Ultra-Trail du Mont Blanc (etwa 171 km). Im Labor wurden zahlreiche molekulare Marker gemessen — Metabolite, Lipide und Indikatoren mechanischer Belastung —, um ein umfassendes Bild davon zu zeichnen, wie Erythrozyten mit extremer Ausdauerbelastung umgehen.
Kurz zusammengefasst: Beide Rennen zeigten Hinweise auf zelluläre Schäden, doch die Ultra-Distanz-Läufer wiesen deutlich stärkere Veränderungen auf. Rote Blutkörperchen wurden weniger flexibel. Sie akkumulierten biochemische Läsionen, die mit einem beschleunigten Abbau assoziiert sind. Besonders auffällig war eine Überlastung eines spezifischen Reparaturwegs — des sogenannten Lands-Zyklus, eines Membranreparaturmechanismus — bei den Ultra-Läufern. Das deutet darauf hin, dass der Körper Schwierigkeiten hatte, das Tempo der Schädigung mit Reparaturmechanismen auszugleichen.
Die Untersuchung umfasste neben Standardblutwerten auch detaillierte Analysen von Lipidoxidation, Membranlipid-Profilen und Metabolom-Daten, die zusammengenommen eine robuste Sicht auf die zellulären Effekte erlauben. Solche multimodalen Daten sind wichtig, weil einzelne Marker leicht fehlinterpretiert werden könnten, während das Zusammenwirken von mechanischen und biochemischen Parametern ein konsistentes Muster ergab.
Was bedeutet diese verringerte Flexibilität praktisch? Rote Blutkörperchen müssen sich durch Kapillaren zwängen, die oft schmaler sind als ihr Ruhredurchmesser. Wenn sie an Geschmeidigkeit verlieren, verschlechtert sich die Mikrozirkulation. Steifere Zellen werden schneller aus dem Kreislauf entfernt, was die kurzfristige Sauerstofftransportkapazität reduziert. Die Studie beobachtete einen Abfall zirkulierender Erythrozyten ausschließlich bei den Ultra-Läufern — ein Befund, der mit diesem Mechanismus konsistent ist.
Warum rote Blutkörperchen besonders anfällig sind
Rote Blutkörperchen sind ungewöhnlich: Sie besitzen keinen Zellkern. Ohne Zellkern können sie keine neuen Proteine synthetisieren und haben eine eingeschränkte Fähigkeit, intern entstandene Schäden zu reparieren. Erythrozyten altern im Blutkreislauf und werden schließlich in Milz und Leber recycelt. Wenn mechanische Beanspruchung und molekulare Stressfaktoren zunehmen — beispielsweise oxidative Reaktionen, Lipidabbau und Membrandisruptionen —, können sich Erythrozyten nicht so effizient selbst reparieren wie kernhaltige Zellen.
Das macht Ausdauerbelastung besonders relevant. Muskulatur, Sehnen und das Herz passen sich über Trainingsreize an; Erythrozyten hingegen besitzen nur begrenzte adaptive Kapazität. Die Forschenden beschreiben das beobachtete Muster als ein Ungleichgewicht zwischen Stress und Reparatur: Jenseits einer bestimmten Schwelle in Bezug auf Dauer und Belastung — irgendwo zwischen Marathon-Distanz und 100-Meilen-Rennen — häufen sich Schäden schneller an, als der Körper sie beheben kann.
Technisch gesprochen betrifft das vor allem Membranlipide und Membranproteine, deren Strukturintegrität für die Verformbarkeit essenziell ist. Lipidperoxidation verändert die Fluidität der Membran, während Proteinschäden am Zytoskelett die Fähigkeit der Zelle zum Deformieren einschränken. Beide Effekte führen zu einer erhöhten Fragilität und letztlich zu einer vermehrten Aussortierung durch die Milz.
Der leitende Forscher Travis Nemkov von der University of Colorado Anschutz brachte es unmissverständlich auf den Punkt: ‚Wir können nicht pauschal empfehlen, ob Menschen an solchen Veranstaltungen teilnehmen sollten oder nicht. Was wir sagen können, ist, dass anhaltender Stress die am häufigsten vorkommende Zelle im Körper schädigt.‘ Diese oder ähnliche Formulierungen zeigen, dass die Studie eher auf Mechanismen und Forschungsfragen zielt als auf unmittelbare Verhaltensanweisungen für Sportler.
Ein weiterer bemerkenswerter Aspekt der Arbeit ist eine unerwartete Parallele zur Transfusionsmedizin. Die gemessenen biochemischen Läsionen in den Erythrozyten von Ultra-Läufern ähneln denen, die in gelagertem Spendeblut entstehen. Angelo D'Alessandro, Koautor und Biochemiker, schlug vor, dass extreme körperliche Belastung als kontrolliertes menschliches Modell dienen könnte, um Interventionen zu testen, die darauf abzielen, die Zellfunktion während der Lagerung zu erhalten. Das eröffnet potenziell translative Forschungswege zwischen Sportphysiologie und Blutbankmedizin.
Interpretation, Einschränkungen und offene Fragen
Wichtige Vorbehalte sind zu beachten. Die Stichprobe war klein — 23 Athletinnen und Athleten — und die beiden Rennen unterschieden sich in vielerlei Hinsicht neben der Distanz: Tempogestaltung, Höhenmeter, Temperaturbedingungen und Streckenbeschaffenheit variierten. Das erschwert direkte Ursache-Wirkungs-Schlüsse. Zudem folgte die Studie den Teilnehmenden nicht langfristig, sodass unklar bleibt, ob die beobachteten akuten Veränderungen zu bleibenden Schäden führen oder ob eine vollständige Erholung innerhalb von Tagen oder Wochen erfolgt.
Im Kontext früherer Forschung ist zu berücksichtigen, dass Elite-Ausdauerathletinnen und -athleten oft eine längere Lebenserwartung und günstigere kardiovaskuläre Profile aufweisen als die Allgemeinbevölkerung. Das bedeutet: Ein akuter zellulärer Stress während eines einzelnen Wettkampfs impliziert nicht zwangsläufig gesundheitliche Nachteile auf lange Sicht. Dennoch wirft die Beobachtung, dass eine weit verbreitete Zellenart durch extreme Belastung in Richtung beschleunigtes Altern gedrängt werden kann, wichtige Fragen für Sportmedizin und Transfusionswissenschaft auf.
Weitere Studien sollten größere Kohorten verfolgen, Zwischenstrecken einschließen, um den Wendepunkt zu identifizieren, und detaillierte Erholungszeitenkartierungen vornehmen. Ebenso wichtig ist die Prüfung von Interventionen: Ernährungsstrategien (z. B. Antioxidantien, gezielte Fettsäuresupplementierung), Renomierte Hydrierungs- und Pacing-Strategien, oder pharmakologische Ansätze könnten protektiv wirken und Membran- sowie Stoffwechsel-Schäden abschwächen. Randomisierte, kontrollierte Studien wären ideal, um kausale Effekte zu klären.
Zusätzlich wäre es nützlich, Studien zu entwerfen, die wiederholte Belastungen untersuchen — also den Effekt von mehreren aufeinanderfolgenden Wettkämpfen oder intensiven Trainingsblöcken. Erkenntnisse darüber, wie sich Erythrozyten zwischen Belastungen erholen und ob wiederholte Events zu kumulativen Effekten führen, wären für Trainingsplanung und Athletenbetreuung wertvoll.
Experteneinschätzung
„Wir neigen dazu, die Effekte von Ausdauerbelastung auf Muskeln und Gelenke zu fokussieren“, sagt Dr. Lena Morales, eine Sportphysiologin, die nicht an der Studie beteiligt war. „Aber Blut ist das eigentliche Liefersystem. Kleine Defizite in der Deformabilität roter Zellen können sich während wiederholter Belastungsphasen zu einer reduzierten Sauerstoffverfügbarkeit in peripheren Geweben aufschaukeln. Die Überwachung dieser Veränderungen könnte Athleten helfen, die Erholung zu optimieren und kurzfristige Leistungsverluste zu reduzieren.“
Sie ergänzt: „Wenn die Parallele zur Blutlagerung Bestand hat, könnten wir disziplinenübergreifende Vorteile sehen — bessere Transfusionsprodukte und optimierte Versorgung von Athleten. Solche translationalen Einsichten sind genau das, was man sich von Humanstudien wünscht, die zwar unordentlich aussehen, aber tiefergehende physiologische Geschichten erzählen.“
Diese Arbeit steht an der Schnittstelle von Sportwissenschaft und zellulärer Physiologie. Sie verbietet nicht zu laufen; vielmehr deutet sie auf ein Schwellenphänomen hin und öffnet Wege für weiterführende Forschung und praktisches Monitoring. Der nächste Schritt ist konzeptionell einfach, praktisch jedoch anspruchsvoll: Mehr Menschen länger verfolgen und fragen, wie — und wie schnell — sich diese Zellen erholen.
Für Sportlerinnen und Sportler sowie Betreuer bedeutet das: Es ist sinnvoll, nach extremen Belastungen Blutparameter im Blick zu behalten, insbesondere wenn Wiederholungsrennen geplant sind. Wer auf Nummer sicher gehen will, kann einfache Kontrollen erwägen — Hämoglobin, Hämatokrit, Marker für Hämolyse und Entzündung — und mit Sportmedizinern individuelle Erholungspläne abstimmen.
Die Studie hat auch Implikationen für die Trainingsgestaltung. Periodisierung, angepasste Reduktionsphasen und gezielte Regenerationsmaßnahmen könnten helfen, die Balance zwischen Belastung und Reparatur zugunsten der Gesundheit zu verschieben. Zudem könnten Athletinnen und Athleten von Ernährungsempfehlungen profitieren, die die Membransubstrate stabilisieren und oxidative Schäden minimieren.
Schließlich bleibt ein praktischer Rat: Laufe die Distanz, wenn du es möchtest. Aber eventuell lohnt sich ein Blutcheck danach. Die Forschung erinnert uns daran, dass nicht alles so stoisch nachgibt wie der menschliche Wille — manche physiologischen Systeme haben enge Grenzen.
Quelle: sciencealert


Kommentar hinterlassen