8 Minuten
Erstaunlich, einfach und hartnäckig: Wenn man über viele Jahre weniger isst, könnte die Verschaltung im Gehirn langsamer altern. Das ist die provokante Schlussfolgerung eines langjährigen Experiments, das Probanden über ihre gesamte Lebensspanne verfolgte und Gehirngewebe auf zellulärer Ebene untersuchte.
Eine jahrzehntelange Studie legt nahe, dass anhaltende Kalorienrestriktion die zelluläre Alterung des Gehirns beeinflussen kann. Durch die Analyse einzelner Gehirnzellen fanden Forschende heraus, dass eine reduzierte Kalorienzufuhr mit wichtigen Faktoren zusammenhing, die die Integrität der weißen Substanz bewahren.
Langfristige Kalorienrestriktion und Gehirnresilienz
Mit zunehmendem Alter verlieren Neurone nicht nur ihre Funktionalität; die unterstützenden Systeme um sie herum verschleißen. Myelin — die fetthaltige Hülle, die Axone isoliert und schnelle Signalübertragung ermöglicht — baut sich allmählich ab. Mikroglia, die immunologischen Wächter des Gehirns, können von hilfreichen „Hausmeistern“ zu chronisch aktivierten Entzündungsförderern umschlagen. Das Resultat sind verlangsamte Kommunikation zwischen Zellen, fragile weiße Substanz und eine erhöhte Anfälligkeit für neurodegenerative Erkrankungen.
Die Boston University Chobanian & Avedisian School of Medicine berichtet über Hinweise, dass eine um etwa 30 % reduzierte Kalorienzufuhr, über mehr als zwei Jahrzehnte in einem experimentellen Primatenmodell aufrechterhalten, mit molekularen Zeichen eines erhaltenen Gehirnzustands verknüpft war. Das Forschungsteam beobachtete zwei Gruppen über ihre natürliche Lebensspanne — eine Gruppe erhielt eine ausgewogene Ernährung mit üblichen Kalorienmengen, die andere eine konsequente Kalorienrestriktion — und führte detaillierte postmortale Analysen durch, um die über Jahre geschriebenen zellulären Befunde zu entschlüsseln.
Im Kontext von Ernährung, Altersprozessen und molekularer Biologie ist diese Studie bemerkenswert, weil sie mehrere Aspekte kombiniert: Langzeitintervention, ein länger lebendes Tiermodell, Einzelzellanalysen und fokusierte Auswertung auf weiße Substanz und gliale Zellen. Solche Verknüpfungen sind wichtig für das Verständnis von Mechanismen, die Gehirnalterung modulieren könnten, und liefern Ansatzpunkte für translationale Forschung, etwa zu Kalorienrestriktion, Intervallfasten oder Kalorienrestriktions‑Mimetika (CR‑Mimetika).
Untersuchungen und Ergebnisse der Forscher
Um in einzelne Zellen hineinzublicken, verwendete das Team die Einzelkern‑RNA‑Sequenzierung (single‑nuclei RNA sequencing), eine Methode, die Genaktivität kernweise erfasst. Dadurch konnten sie Expressionsmuster zwischen Zelltypen vergleichen: Neurone, Oligodendrozyten (die Zellen, die Myelin produzieren), Mikroglia und weitere Stützzellen. Die Unterschiede waren nicht geringfügig. Zellen aus der kalorienreduzierten Gruppe zeigten höhere Expression von Genen, die mit Myelinbildung assoziiert sind, sowie stärkere Aktivität in zentralen Stoffwechselwegen — speziell Glykolyse und Fettsäuresynthese — also in Pfaden, die Myelinstruktur mit Substraten und Energie versorgen und erhalten.
Warum ist das relevant? Myelin ist keine passive Umhüllung. Es ist energetisch aufwendig, es aufzubauen und zu reparieren. Wenn die zellulären Maschinen, die Substrate und Energie liefern, beeinträchtigt sind, verschlechtert sich die Myelinintegrität, Signalübertragung verlangsamt sich, und kognitive Prozesse, die auf schnelle neuronale Koordination angewiesen sind, werden ineffizienter. Dies betrifft Funktionen wie Verarbeitungsgeschwindigkeit, episodisches Gedächtnis, motorische Koordination und die Anpassungsfähigkeit neuronaler Netzwerke.
Die Studie beobachtete zudem Veränderungen in den Mikroglia‑Profilen. Anstatt Marker chronischer Aktivierung zu zeigen, wie sie typischerweise im Alter auftreten, behielten Mikroglia aus kalorienreduzierten Individuen ein Genexpressionsmuster bei, das für eine ausgeglichene immunologische Überwachung spricht. Kurz gesagt: weniger anhaltende Entzündung und ein zelluläres Umfeld, das eher auf Erhaltung als auf Schädigung ausgerichtet ist. Diese Beobachtung ist im Hinblick auf inflammaging — die altersbedingte, low‑grade Entzündungsantwort — besonders relevant.
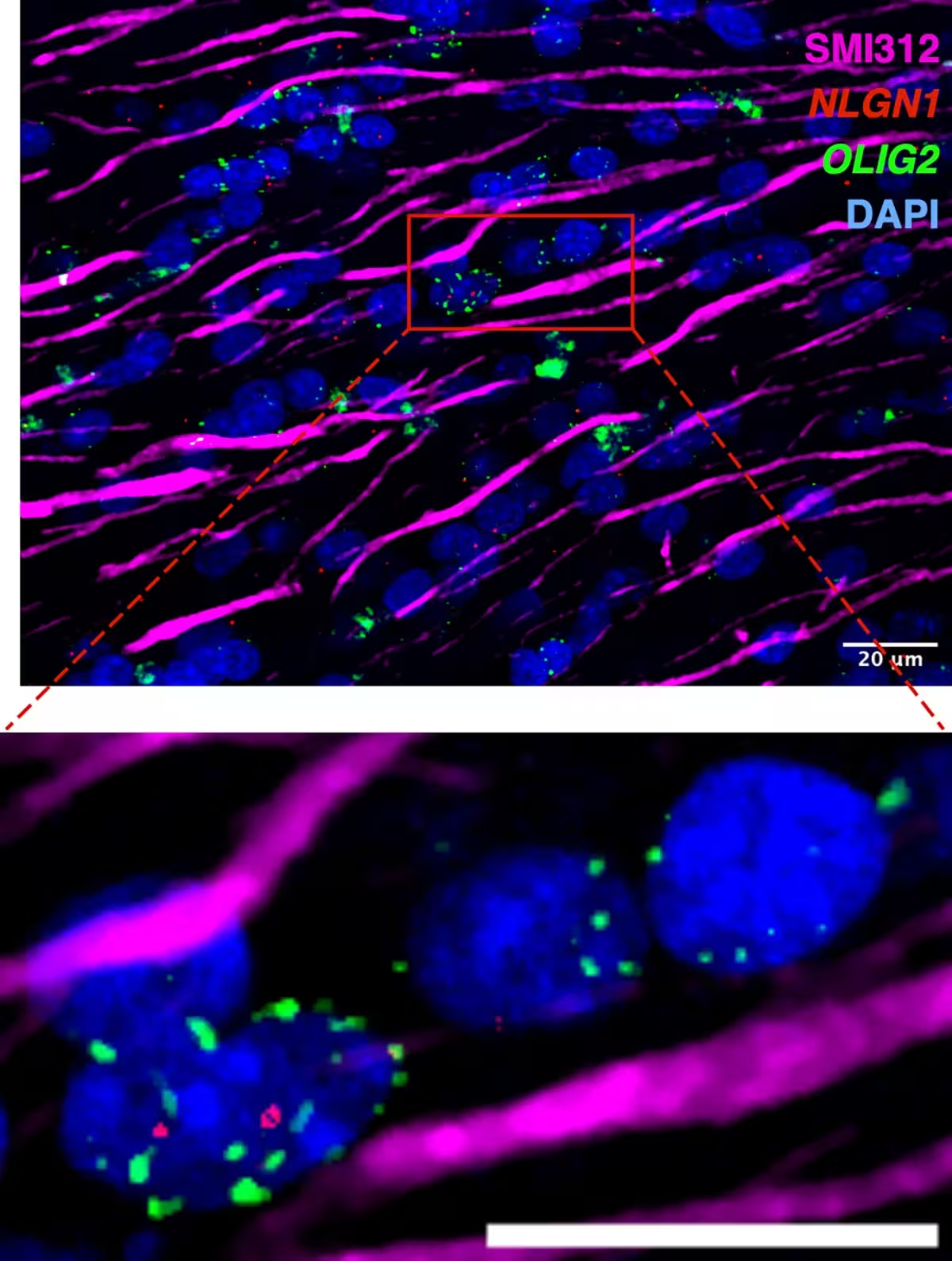
Axonale Nervenfasern (magenta) umgeben von unterstützenden Gehirnzellen, deren Zellkerne blau angefärbt sind. Grüne Punktierungen zeigen OLIG2‑mRNA, die Oligodendrozyten identifiziert — die Gehirnzellen, die die schützende Myelinscheide um Nerven bilden. Rote Punktierungen zeigen NLGN1, ein Molekül, das diesen Oligodendrozyten hilft, sich mit Nervenfasern zu verbinden. Normalerweise reduziert das Altern NLGN1‑Spiegel und stört so die Myelinbildung. Die Forschenden fanden jedoch, dass langfristige Kalorienrestriktion die NLGN1‑Expression erhalten hilft, was potenziell eine gesunde Nervenisolierung und Kommunikation bewahren kann.
Technisch gesehen liefern OLIG2 und NLGN1 greifbare Biomarker für Oligodendrozytenfunktion und Myelinnetzwerkverbindungen. Die beobachteten Erhöhungen myelinassoziierter Transkripte lassen auf eine gesteigerte Synthese von Lipiden, Membranproteinen und Enzymen schließen, die für Myelinaufbau nötig sind. Parallel dazu deuten veränderte Expressionen in Glykolyse‑ und Lipidbiosynthese‑Genen auf eine robuste Energieversorgung hin: Gliazellen können Glukose‑Intermediate und Fettsäuren bereitstellen, die für Membransynthese und Reparatur unabdingbar sind.
Wichtig ist auch, dass diese molekularen Signale eine plausible Kaskade skizzieren: Kalorienrestriktion moduliert metabolische Signale (z. B. AMPK, mTOR‑Pfad, Insulin/IGF‑Signaling), diese beeinflussen Genexpressionsprogramme in Gliazellen, die wiederum Myelinproduktion und Immunüberwachung steuern — wodurch neuronale Leitungsfähigkeit und kognitive Resilienz theoretisch verbessert werden können. Solche Mechanismen sind konsistent mit Erkenntnissen aus Modellorganismen, in denen Energie‑ und Lipidstoffwechsel entscheidend für Langlebigkeit und Gewebehomöostase sind.
Interpretation, Grenzen und praktische Erwägungen
Die Hauptautoren hoben die breitere Bedeutung hervor. Ana Vitantonio, Erst‑Korrespondenzautorin und Doktorandin, bemerkte, dass Kalorienrestriktion zwar in kurzlebigeren Arten Lebensspanne und Stoffwechsel beeinflusst hat, diese Arbeit jedoch seltene, nachhaltige Hinweise liefert, dass ähnliche protektive molekulare Signaturen im Gehirngewebe eines länger lebenden, komplexen Modells auftreten. Tara L. Moore, PhD, Mitautorin, betonte die kognitiven Implikationen: Wenn Myelinbildung und metabolische Unterstützungssysteme robuster bleiben, könnte das zelluläre Fundament für Lernen und Gedächtnis besser erhalten bleiben.
Es gibt jedoch wichtige Vorbehalte. Es handelt sich um ein experimentelles Tiermodell, nicht um eine randomisierte kontrollierte Studie am Menschen. Kalorienrestriktion beim Menschen wirft praktische Fragen zu Nährstoffversorgung, langfristiger Compliance, psychosozialen Effekten und unbeabsichtigten Nebenwirkungen auf — etwa Verlust von Muskelmasse, hormonelle Veränderungen oder Unterversorgung mit Mikronährstoffen, wenn sie nicht gut geplant ist. Zudem variieren metabolische Reaktionen zwischen Arten, Altersgruppen und individuellen Stoffwechselprofilen.
Trotzdem bieten die zellulären Signale — höhere myelinbezogene Genexpression, erhaltene metabolische Pfade und gedämpfte Mikroglia‑Überaktivierung — eine plausible mechanistische Verbindung zwischen Ernährung und der Art und Weise, wie das Gehirn die Zeit übersteht. Diese molekularen Marker können in zukünftigen Studien als endpoints dienen, um weniger extreme oder besser verträgliche Strategien zu testen, die ähnliche Vorteile liefern könnten, etwa intermittierendes Fasten, zeitlich begrenzte Nahrungsaufnahme (time‑restricted feeding) oder pharmakologische CR‑Mimetika.
Pragmatische Forschungsfragen für die Translation in den Menschen sind unter anderem:
- Welche Form und Intensität der Kalorienreduktion sind praktikabel und sicher für verschiedene Altersgruppen?
- Können gezielte Nährstoffergänzungen (z. B. essentielle Fettsäuren, bestimmte Aminosäuren, Vitamine) die Nachteile einer Reduktion kompensieren?
- Zeigen biomarkerbasierte Beobachtungs‑ oder Interventionsstudien bei Menschen ähnliche Veränderungen in myelinassoziierten Genen und Mikroglia‑Markern?
Forscher sollten zudem kontrollierte Langzeitstudien mit intensiver Ernährungsüberwachung und multimodalen Endpunkten (neuroimaging der weißen Substanz, kognitive Tests, Biomarker für Inflammation und Lipidstoffwechsel) in Betracht ziehen. Kombinationstherapien, die Ernährung mit Bewegung, Schlafoptimierung und vaskulärer Gesundheit verbinden, könnten synergistische Effekte erzeugen, da Gefäßgesundheit und Glukoseregulation direkten Einfluss auf Gehirnstoffwechsel und Myelin haben.
Experteneinschätzung
„Dass metabolische Pfade, die mit Myelinwartung verbunden sind, auf langfristige Ernährungsänderungen reagieren, ist überzeugend“, sagt Dr. Lena Carter, eine fiktive, aber plausibel dargestellte Neurowissenschaftlerin und Wissenschaftskommunikatorin. „Es gibt uns einen mechanistischen Ansatzpunkt: Interventionen, die Energieversorgung und Lipidbiosynthese in Gliazellen unterstützen, könnten sich in einer besseren Gesundheit der weißen Substanz niederschlagen. Ernährung ist ein Hebel unter vielen — Bewegung, Schlaf und vaskuläre Gesundheit sind ebenfalls wichtig — aber diese Studie erinnert uns daran, dass das, was wir über Jahrzehnte essen, zelluläre Bahnen neu schreiben kann.“
Die nächsten Schritte sind klar: prüfen, ob ähnliche molekulare Muster bei Menschen auftreten, die eine maßvolle, ernährungswissenschaftlich überwachte Kalorienreduktion praktizieren; weniger extreme oder intermittierende Ernährungsstrategien testen, die vergleichbare Vorteile bringen; und nach pharmakologischen oder lebensstilbasierten Interventionen suchen, die die schützenden Signaturen nachahmen, ohne eine strenge langfristige Einschränkung zu erfordern.
Für den Moment ist die Botschaft nuanciert. Eine Reduktion der Kalorienzufuhr um etwa dreißig Prozent über Jahre scheint in diesem langfristigen experimentellen Befund einige molekulare Aspekte der Gehirnalterung zu verlangsamen — hauptsächlich indem die Zellen und Pathways unterstützt werden, die Myelin aufbauen und erhalten, und indem Immunzellen daran gehindert werden, in schädliche chronische Aktivierung zu kippen. Es erinnert uns daran, dass Altern nicht nur ein Kalendereffekt ist; es wird durch Jahrzehnte metabolischer Entscheidungen und zellulärer Interaktionen geformt, die diese Entscheidungen hervorrufen.
Wissenschaftlich gesehen erweitert die Studie das Verständnis von „healthy brain aging“ und bietet konkrete molekulare Ziele (z. B. Enzyme der Fettsäuresynthese, Transkriptionsfaktoren für Oligodendrogenese, Marker für Mikroglia‑Aktivierung) für präklinische und klinische Untersuchungen. Für klinische Praktiker und Ernährungswissenschaftler ist es wichtig, Studienergebnisse in praktikable, sichere Empfehlungen zu übersetzen — mit individueller Anpassung und kontinuierlicher Überwachung, insbesondere bei älteren Menschen oder Personen mit Vorerkrankungen.
Schließlich sollte betont werden, dass Ernährung nicht isoliert wirkt. Kardiovaskuläre Gesundheit, systemische Entzündungsprozesse, metabolische Flexibilität, körperliche Aktivität und psychosoziale Faktoren interagieren komplex mit zellulären Mechanismen im Gehirn. Ein integrierter Ansatz, der Ernährung, Bewegung, Schlaf und vaskuläre Prävention umfasst, hat das größte Potenzial, Gehirnalterung und neurodegenerative Risiken nachhaltig zu beeinflussen.
Quelle: scitechdaily


Kommentar hinterlassen