8 Minuten
Neue Langzeitforschung an Rhesusaffen deutet darauf hin, dass eine moderate, über Jahre beibehaltende Reduktion der Kalorienzufuhr – in der Größenordnung von etwa 30 Prozent – altersbedingte Schäden im Gehirn verlangsamen kann. Die Studie verknüpft Kalorienrestriktion mit besserer Myelingesundheit, der isolierenden Schicht, die Neuronen schnelle Signalübertragung ermöglicht und im Alter widerstandsfähiger bleibt.
Warum Myelin für alternde Gehirne wichtig ist
Myelin ist die fetthaltige Hülle, die Axone umgibt — die langgestreckten Fortsätze, mit denen Nervenzellen Signale weiterleiten. Man kann es sich als biologische Isolierung vorstellen: Myelin erhöht die Leitungsgeschwindigkeit elektrischer Impulse und schützt die empfindlichen „Verkabelungen“ des Nervensystems. Mit zunehmendem Alter treten Abbauprozesse im Myelin auf und die Reparaturmechanismen werden weniger effizient. Diese Veränderungen tragen zu verlangsamter Informationsverarbeitung, gehäufter neuronaler Fehlkommunikation und erhöhter neuroinflammatorischer Aktivität bei — Prozesse, die mit Alzheimer, vaskulärer Demenz und anderen neurodegenerativen Erkrankungen in Verbindung gebracht werden.
Auf zellulärer Ebene sind Oligodendrozyten die zentralen Produzenten und Erhalter von Myelin im zentralen Nervensystem. Sie wickeln wiederholte Schichten von Membran um Axone und regulieren so die saltatorische Erregungsleitung an den Ranvierschen Schnürringen. Myelin besteht überwiegend aus Lipiden und myelin-spezifischen Proteinen; deshalb sind lipidstoffwechselbezogene Signalwege und Cholesterinbiosynthese für die Myelinsynthese und -stabilität essentiell. Mit dem Alter gehen sowohl die Fähigkeit zur Lipidproduktion als auch die Reparatur durch oligodendrogliale Vorläuferzellen (OPCs) zurück, was die Anfälligkeit für Demyelinisierung erhöht.
Zusätzlich spielt das Zusammenspiel mit Mikroglia und Astrozyten eine Rolle: chronische, niedriggradige Entzündungsreaktionen können myelinbildende Zellen beeinträchtigen und die Remyelinisierung erschweren. Daher ist Myelin nicht nur eine passive Hülle, sondern ein dynamisches Element neuronaler Gesundheit und kognitiver Leistungsfähigkeit.
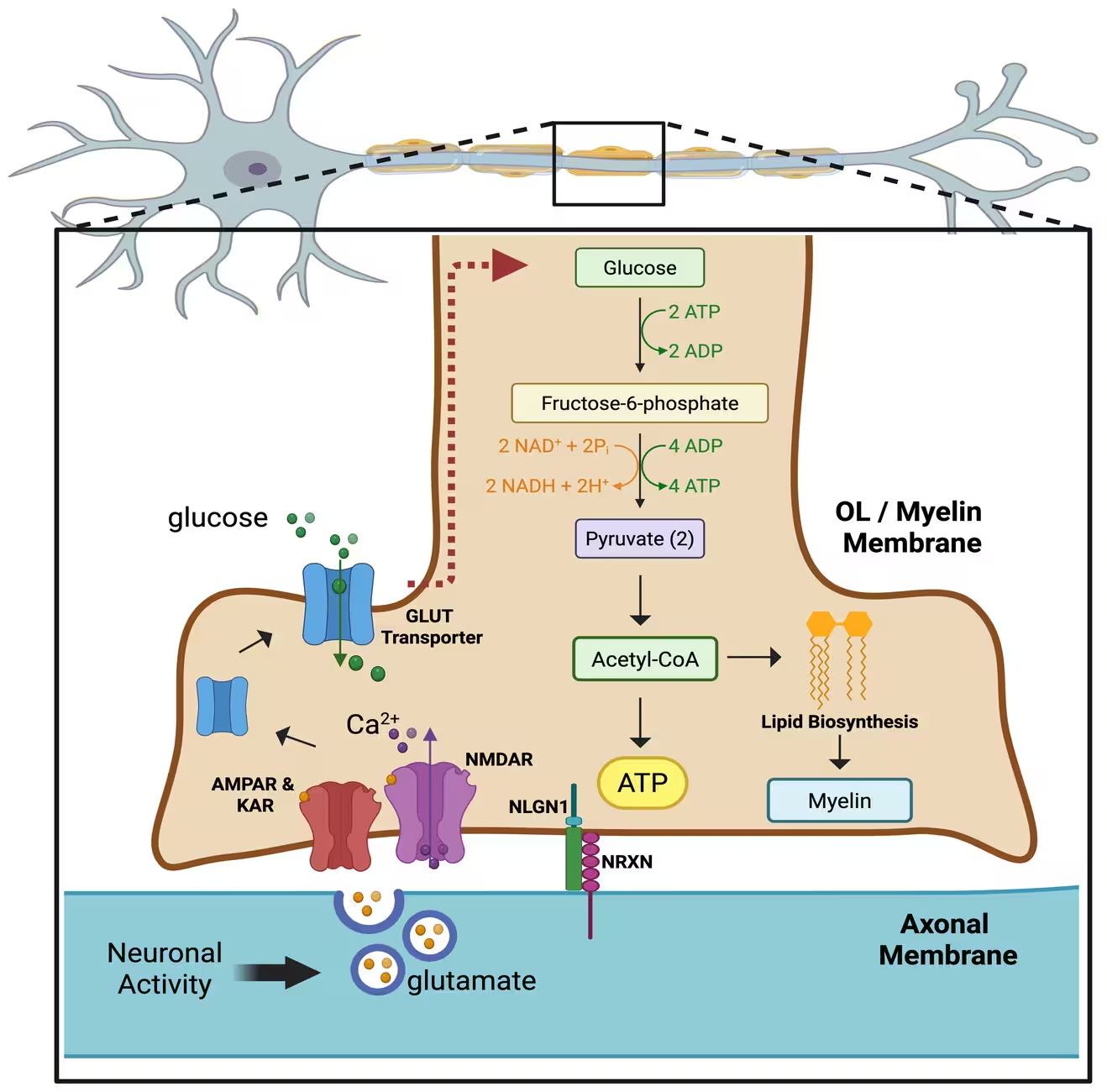
Abbildung zeigt, wie aktive Neuronen Signale an Oligodendrozyten senden, damit diese Myelin produzieren
Zwei Jahrzehnte Diätexperiment bei Rhesusaffen
Wissenschaftler der Boston University untersuchten Gehirne von 24 Rhesusmakaken (Macaca mulatta), die über mehr als 20 Jahre unterschiedlichen Ernährungsregimen gefolgt waren. Die Hälfte der Tiere erhielt eine Standardernährung, während die andere Hälfte ein streng kontrolliertes Kalorienrestriktionsprogramm absolvierte, das die Energiezufuhr um rund 30 Prozent reduzierte. Die Tiere wurden regelmäßig medizinisch überwacht, um Mangelzustände zu vermeiden und um Veränderungen von Gewicht, Stoffwechselparametern und allgemeinem Gesundheitszustand zu dokumentieren.
Bei der Analyse von Hirngewebe stellten die Forschenden deutliche molekulare und zelluläre Hinweise darauf fest, dass die Myelingesundheit bei den Tieren der kalorienreduzierten Gruppe besser erhalten war. So waren Gene, die mit Myelinproduktion und Myelinaufbau assoziiert sind, stärker exprimiert. Zusätzlich zeigten sich verbesserte Aktivitäten in Stoffwechselwegen, die die Myelinpflege unterstützen — etwa solche der Lipid- und Cholesterinsynthese, der Mitochondrienfunktion und der zellulären Proteinqualitätskontrolle.
Auf zellulärer Ebene wirkten Oligodendrozyten effizienter: Indikatoren für die Differenzierung oligodendroglialer Vorläuferzellen und für Remyelinisierungsprozesse waren erhöht, während Marker chronischer Entzündung und zellulären Stresses geringer ausfielen. Ergänzend wurden histologische Techniken, Immunfärbungen und transkriptomische Analysen kombiniert, um ein umfassendes Bild von Struktur und Funktion des myelinierenden Systems zu erhalten.
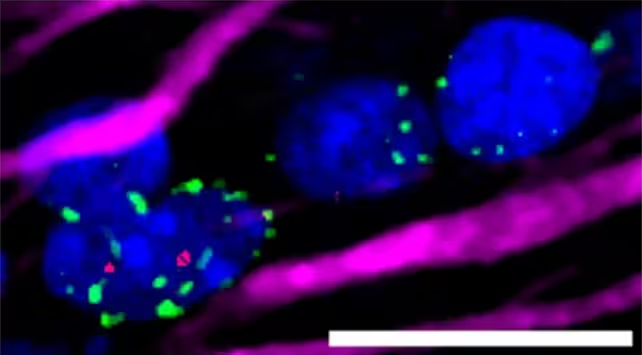
Mikroskopische Aufnahme zeigt gesunde Hinweise von Oligodendrozyten (Zellkerne blau gefärbt), die eine schützende Myelinhülle für nahe Nervenfasern (magenta) bilden. Weiße Maßstabsleiste = 20 μm.
Bedeutung der Ergebnisse für Gehirnalterung und Krankheit
Durch die Verschiebung des Stoffwechsels in einen effizienteren Zustand kann Kalorienrestriktion zellulären Verschleiß verringern. In diesem Forschungsprojekt lässt sich dieser metabolische Shift offenbar in eine bessere Erhaltung von Myelinstruktur und -funktion übersetzen, was wiederum die entzündliche Kaskade dämpfen könnte, die sonst den kognitiven Abbau beschleunigt. Weniger Myelinverlust bedeutet potenziell stabilere neuronale Signalübertragung, was sich positiv auf Lernen, Merkfähigkeit und Reaktionsgeschwindigkeit auswirken kann.
Die Leiterin der Studie, die Neurobiologin Ana Vitantonio von der Boston University, weist darauf hin, dass Kalorienrestriktion bereits in kurzlebigen Tiermodellen als Intervention gegen biologisches Altern gut dokumentiert ist. Diese Untersuchung liefert seltene, langfristige Befunde, die darauf hindeuten, dass ähnliche protektive Effekte auch im Gehirn einer Primatenart auftreten können, die in vielen Aspekten dem Menschen ähnlicher ist als Nagetiere.
Koautorin Tara Moore betont, dass der Erhalt von intaktem Myelin direkte Auswirkungen auf Kognition und Lernprozesse haben könnte, da gut erhaltenes Myelin schnelle und präzise neuronale Kommunikation unterstützt. Zusammengefasst legen die Daten nahe, dass die Reduktion zellulärer Belastungsfaktoren — z. B. oxidativer Stress, mitochondriale Dysfunktion und chronische Entzündung — die Integrität myelinierter Fasern erhöht und dadurch neurodegenerative Prozesse zumindest verlangsamen kann.
Wesentliche Mechanismen, die als Verbindung zwischen Kalorienrestriktion und verbesserter Myelinversorgung diskutiert werden, umfassen:
- Verbesserte Lipid- und Cholesterinstoffwechselwege, die für Myelinsynthese zentral sind.
- Erhöhte Autophagie und Proteinnetzwerk-Qualitätskontrolle, die fehlerhafte Proteine und zellulären Abfall abbauen.
- Reduzierte systemische und neuronale Entzündung durch modulierte Immunantworten.
- Verbesserte mitochondrial-metabolische Effizienz, die die Energieversorgung oligodendroglialer Zellen stützt.
Studieneinschränkungen und Kontext für die Praxis
Trotz der positiven Hinweise bleiben wichtige Einschränkungen: Die Stichprobe war klein — 24 Tiere — und Rhesusaffen sind zwar ein wertvolles Modell für die menschliche Biologie, aber kein identisches Abbild. Die Übertragbarkeit eines strengen, jahrzehntelangen 30-prozentigen Kaloriendefizits auf Empfehlungen für Menschen ist komplex. Faktoren wie langfristige Therapietreue, ausgewogene Nährstoffzufuhr, psychosoziale Aspekte und mögliche Nebenwirkungen müssen berücksichtigt werden.
Potenzielle Risiken einer langfristigen, starken Kalorienreduktion bei Menschen können Mangelversorgung bestimmter Mikronährstoffe, verringerte Knochendichte, Verlust an Muskelmasse und in einigen Fällen eine beeinträchtigte Immunfunktion umfassen. Deshalb sind begleitende Maßnahmen wie ausgewogene Makro- und Mikronährstoffzufuhr, Krafttraining zur Erhaltung der Muskelmasse und medizinische Überwachung essenziell, wenn man ernährungsbasierte Interventionen in die klinische Praxis überführen möchte.
Es ist ebenfalls wichtig zu betonen, dass die Ernährung nur ein Aspekt in einem multifaktoriellen Puzzle der Gehirngesundheit ist. Schlafqualität, geistige Aktivität (etwa das Erlernen neuer Fähigkeiten oder Sprachen), regelmäßige körperliche Bewegung, kardiovaskuläre Gesundheit und psychosoziale Faktoren beeinflussen gemeinsam, wie unser Gehirn altert. Künftige Humanstudien müssen diese Variablen kontrollieren oder in die Analyse einbeziehen, und prüfen, ob weniger drastische oder intermittierende Energieeinschränkungen (z. B. Intervallfasten oder zeitbegrenzte Nahrungsaufnahme) gleiche Vorteile bei geringerem Risiko bieten.
Breitere Implikationen und nächste Schritte
Die Verbindung zwischen Myelinabbau und neurodegenerativen Erkrankungen steht zunehmend im Fokus neurologischer Forschung. Bildgebende Studien bei Menschen mit raschem kognitiven Abbau zeigen Hinweise auf myelinäre Veränderungen; die hier beschriebene Primatenstudie liefert eine mögliche Interventionsroute, die in zukünftigen klinischen Ansätzen berücksichtigt werden könnte. Wenn Kalorienrestriktion oder bestimmte Kalorienmuster den Myelinabbau verlangsamen, könnten TherapeutInnen eines Tages diätetische Strategien mit Pharmazeutika oder anderen Lebensstilmaßnahmen kombinieren, um besonders verletzliche neuronale Schaltkreise zu schützen.
Konkrete nächste Forschungsstufen umfassen:
- Längsschnittstudien am Menschen, die Kalorienmuster, Nährstoffdichte und klinische Endpunkte (kognitive Tests, MRT-Myelinbildgebung) kombinieren.
- Größere Kohortenstudien bei Nicht-Menschen-Primaten zur Replikation und Erweiterung der Ergebnisse.
- Molekulare Studien, die gezielt untersuchen, welche metabolischen Signalwege (z. B. Lipidsynthese, mTOR/AMPK-Signaling, Autophagie) durch Kalorienrestriktion moduliert werden und wie diese Pfade die Oligodendrozytenfunktion beeinflussen.
- Interventionsstudien, die weniger extreme oder intermittierende Formen der Energieeinschränkung mit Blick auf Sicherheit und Praktikabilität prüfen (z. B. zeitlich begrenztes Essen, periodisches Fasten).
Die Autoren empfehlen sorgfältig geplante klinische Studien, die praktikable, sichere und wirksame Ernährungsstrategien definieren. Darüber hinaus ist die Kombination ernährungsbasierter Ansätze mit pharmakologischen Remyelinisierungsstrategien ein vielversprechendes Forschungsfeld, das gezielt oligodendrogliale Reparaturmechanismen unterstützen könnte.
Experteneinschätzung
„Diese Ergebnisse sind spannend, weil sie eine gut steuerbare metabolische Intervention mit einem präzisen zellulären Ziel — dem Myelin — verbinden,“ sagt Dr. Elena Morales, Neurowissenschaftlerin mit Schwerpunkt auf Stoffwechsel des alternden Gehirns. „Die praktische Anwendung verlangt jedoch Nuancen: Gesamtkalorien, Nährstoffdichte und individueller Gesundheitszustand sind entscheidend. Wir benötigen klinische Studien, die realistische, nachhaltige Ansätze für Menschen testen, statt extrem strenger Regime.“
Aus praktischer Sicht bedeutet das: Forschungsteam und Klinikbetreuer sollten zusammenarbeiten, um Interventionen zu entwickeln, die sowohl biologisch wirksam als auch für Menschen langfristig durchführbar sind. Dazu gehören personalisierte Empfehlungen, regelmäßige hämatologische und metabolische Kontrolluntersuchungen sowie begleitende Maßnahmen wie Krafttraining, Schlafoptimierung und kognitive Stimulation.
Zusammenfassend lässt sich sagen, dass eine etwa 30-prozentige Kalorienreduktion in einem kontrollierten, langjährigen Setting molekulare Hinweise auf eine Erhaltung der Myelingesundheit bei Rhesusaffen zeigte. Diese Befunde bieten einen vielversprechenden Ansatzpunkt dafür, wie Ernährungsgewohnheiten die Gehirnalterung beim Menschen beeinflussen könnten. Der Weg nach vorne besteht darin, diese Befunde in sichere, evidenzbasierte Empfehlungen für Menschen zu übersetzen und zugleich Alternativen mit geringerem Risiko — wie weniger extreme Einschnitte oder intermittierende Fastenregime — auf ihre Schutzwirkung für Myelin und kognitive Funktionen zu prüfen.
Quelle: sciencealert

Kommentar hinterlassen