7 Minuten
Stellen Sie sich vor, Sie erfahren Jahre bevor ein verlegter Schlüssel oder ein vergessener Name den ersten Hinweis gibt, dass Sie sich auf einem Weg in Richtung Demenz befinden. Dies ist das Versprechen einer neuen, überraschend einfachen, blutbasierten „molekularen Uhr“, die den wahrscheinlichen Beginn von Alzheimer-Symptomen auf ein Fenster von drei bis vier Jahren eingrenzen kann.
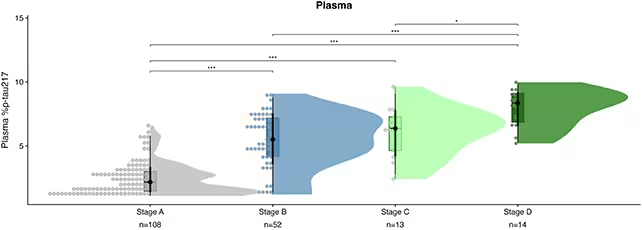
Die Konzentrationen des Proteins p‑tau217 im Blut korrelierten mit dem Fortschreiten von Alzheimer.
Wie ein Protein im Blut Jahre von Gehirnveränderungen abbildet
Wissenschaftler der Washington University in St. Louis passten einen bestehenden Bluttest für p‑tau217 an und legten darüber mathematische Modellierung. Das Ergebnis ist ein Instrument, das gemessene Proteinkonzentrationen mit dem Zeitpunkt verknüpft, an dem Gedächtnis- und andere kognitive Probleme offenbar werden. Auf den ersten Blick schlicht. In der Anwendung sehr wirkungsvoll.
Warum p‑tau217? Weil diese phosphorylierte Form des Tau-Proteins zwei der zentralen biologischen Kennzeichen von Alzheimer widerspiegelt: aggregierte Tau‑Fibrillen (Tangles) und Amyloid‑β‑Plaques. Die Blutkonzentrationen von p‑tau217 spiegeln Prozesse wider, die im Gehirn ablaufen, und bieten damit ein Fenster in eine langfristige, langsam voranschreitende Pathologie — ohne die Kosten, Risiken und Beschwerden von PET-Scans oder Lumbalpunktionen.
In der untersuchten Studie analysierten die Forschenden longitudinale Blutdaten von 603 Teilnehmerinnen und Teilnehmern, die über mehrere Jahre hinweg gesammelt worden waren. Indem sie die Trajektorien von p‑tau217 gegen das Alter abbildeten, in dem kognitive Symptome erstmals auftraten, leiteten sie mathematische Formeln und Modelle ab, die eine Person auf einer Zeitachse zwischen dem frühesten biologischen Wandel und dem klinischen Abfall positionieren. Der typische Zeitraum zwischen ersten Hirnveränderungen und nachweisbarer kognitiver Beeinträchtigung ist lang – häufig 10 bis 30 Jahre – daher ist ein Werkzeug, das die Vorhersage auf wenige Jahre einengt, sowohl für die Forschung als auch perspektivisch für die Patientenversorgung sehr wertvoll.
Technisch stützt sich die Methode auf wiederholte Messungen und statistische Trajektorienanalyse. Solche Modelle berücksichtigen die individuelle Dynamik der Biomarker‑Veränderung, etwa durch glättende Splines oder nichtlineare Regressionsverfahren, und verknüpfen diese mit klinischen Endpunkten wie dem ersten Auftreten subjektiver oder objektiver Gedächtnisstörungen. Wichtig ist, dass die Modelle sowohl Populationsmuster als auch individuelle Abweichungen einfangen, um robuste, aber auch probabilistische Zeitfenster zu liefern.
Dennoch gibt es Einschränkungen. Derzeit eignet sich die Methode besser für Vorhersagen auf Gruppenebene. Sie trennt Kohorten zuverlässig in jene, die wahrscheinlich innerhalb eines definierten Fensters Symptome entwickeln, liefert aber noch keine punktgenauen Prognosen für einzelne Personen. Die Forschenden betonen, dass mehr Daten, Validierung in unabhängigen und diverseren Kohorten sowie algorithmische Verfeinerungen nötig sind, bevor dies ein routinemäßiger prognostischer Test in der Klinik werden kann.
Muster, Alterseffekte und warum die Uhr wichtig ist
Erstautor Kellen Petersen vergleicht die Anhäufung von Amyloid und Tau mit Jahrringen eines Baumes: Liest man die Ringe falsch, schätzt man das Alter falsch; liest man sie richtig, kann man abschätzen, wann der Baum gewachsen ist. Der Vergleich trifft zwei Punkte: Erstens folgt die Anreicherung bei vielen Menschen einer konsistenten Trajektorie; zweitens ist das Alter, in dem diese Biomarker einen pathologischen Schwellenwert überschreiten, ein starker Prädiktor dafür, wann Symptome auftreten werden.
Ein bemerkenswertes Ergebnis der Analyse war: Ältere Personen hatten tendenziell ein kürzeres Intervall zwischen Beginn der biologischen Veränderung und dem Auftreten klinischer Symptome. Jüngere Gehirne scheinen Schäden länger zu kompensieren und können pathologische Veränderungen besser maskieren, selbst wenn sich die Pathologie bereits aufbaut. Für die Planung von klinischen Studien hat das erhebliche Folgen: Die Einschreibung jüngerer, biomarker‑positiver Probanden erfordert möglicherweise längere Nachbeobachtungszeiträume, um das Auftreten von Symptomen zu erfassen, während ältere Teilnehmende schneller klinische Veränderungen zeigen könnten.
Die praktischen Vorteile einer solchen molekularen Uhr erstrecken sich weiter. Klinische Studien zur Prävention benötigen Teilnehmerinnen und Teilnehmer, die wahrscheinlich während des Studienzeitraums Symptome entwickeln. Eine blutbasierte Uhr hilft dabei, diese Personen gezielter auszuwählen und so die Stichprobengröße und Studienlaufzeit zu reduzieren. Darüber hinaus erhöht sich die Zugänglichkeit: Bluttests sind erheblich günstiger und einfacher skalierbar als Bildgebung (z. B. PET) oder Diagnostik über Rückenmarkflüssigkeit, die teuer ist und in vielen Regionen nicht breit verfügbar.
Auf methodischer Ebene kann eine genauere Zeitbestimmung die statistische Planung optimieren — etwa die Schätzung des erwarteten Ereignisaufkommens, die Festlegung von Endpunkten oder die Selektion von Hochrisikogruppen. Das verbessert die Effizienz von Phase‑II‑ und Phase‑III‑Prüfungen und kann die Ressourcenallokation in der Alzheimerforschung nachhaltiger gestalten.
Gleichzeitig bleiben ethische und kommunikative Fragen offen: Möchten Menschen wissen, dass sie ein enges Zeitfenster für den wahrscheinlichen Beginn von Symptomen haben, wenn therapeutische Optionen zur Verhinderung des Fortschreitens begrenzt sind? Wie sollten Ärztinnen und Ärzte probabilistische Vorhersagen vermitteln, sodass Patientinnen und Patienten informierte Entscheidungen treffen können? Diese Herausforderungen betreffen nicht nur die Technik, sondern auch Einwilligung, Beratung und gesundheitsökonomische Planung.
Eine transparente Begleitung — etwa standardisierte Aufklärungsunterlagen, psychologische Beratung und klare Empfehlungen für Monitoring und Lebensstilinterventionen — wird unabdingbar sein, um möglichen Schaden durch Fehlinformation oder unnötige Ängste zu minimieren. Ebenso wichtig ist die Schulung von klinischem Personal im Umgang mit Wahrscheinlichkeitsaussagen und im kommunikativen Management von Unsicherheiten.
Expertinnen- und Experteneinschätzung
„Das ist die Art von translationalem Fortschritt, die wir uns erhoffen — eine Brücke zwischen Laborbefunden und praktischer Entscheidungsfindung“, sagt Dr. Maya Chen, eine Neuroepidemiologin, die an der Studie nicht beteiligt war. „Wenn die Methode in verschiedenen Bevölkerungsgruppen validiert wird, könnte eine Blut‑Uhr die Rekrutierung für Studien neu definieren und für Kliniker die Priorisierung von Überwachung und Intervention erleichtern. Wir dürfen sie jedoch nicht losgelöst von umfangreichen Beratungsressourcen einsetzen; das Wissen um ein Zeitfenster ohne klare Präventionsoptionen kann mehr schaden als nützen.“
Die Studie wurde in Nature Medicine veröffentlicht und wird von Neurologinnen und Neurologen an der Washington University geleitet, darunter Suzanne Schindler, die besonders die Zugänglichkeit betont: Bluttests können Forschung und klinische Reichweite über die wenigen Zentren hinaus erweitern, die PET-Scans oder Lumbalpunktionen durchführen können. Als nächste Schritte nennen die Forschenden die Validierung des Modells in größeren und diverseren Kohorten, die Integration weiterer blutbasierter Biomarker und die Verfeinerung der Algorithmen, um die Vorhersagegenauigkeit auf Individualebene zu verbessern.
Konkreter angedachte Verbesserungen umfassen die Kombination von p‑tau217 mit anderen Biomarkern wie Neurofilament light chain (NfL), spezifischen Amyloid‑Signalen im Blut und genetischen Risikomarkern (z. B. APOE‑Genotyp). Solche multimodalen Modelle könnten die Sensitivität und Spezifität erhöhen und zusätzlich Informationen zur Geschwindigkeit des Fortschreitens liefern.
Für die klinische Umsetzung wären standardisierte Testverfahren, Qualitätskontrollen in Laboren und klare Schwellenwerte erforderlich, damit Messergebnisse zwischen verschiedenen Einrichtungen vergleichbar sind. Regulatory Aspekte — etwa Zulassungen durch Gesundheitsbehörden oder Leitlinien professioneller Gesellschaften — werden ebenfalls eine zentrale Rolle spielen.
Derzeit ist die molekulare Uhr weniger ein persönliches Horoskop als ein Instrument für die Wissenschaft — eines, das die Zeitplanung von Studien präziser machen und unser Verständnis des langsamen, jahrelangen Fortschreitens von Alzheimer vertiefen kann. Die Hoffnung ist, dass eine bessere zeitliche Einordnung Therapien beschleunigt und eines Tages Menschen eine klarere Vorstellung davon gibt, was sie erwarten können und wann sie aktiv werden sollten.
Zusammenfassend bietet p‑tau217 als blutbasierter Biomarker vielversprechende Perspektiven für die Früherkennung und Risikostratifizierung bei Alzheimer. Während die aktuellen Modelle das Potential für eine bessere wissenschaftliche Planung und erweiterte Testzugänge zeigen, bleibt die Herausforderung, die Vorhersagen auf Individualebene zu validieren und sie verantwortungsvoll in klinische und gesellschaftliche Kontexte einzubetten.
Quelle: sciencealert

Kommentar hinterlassen