8 Minuten
Ein Großteil des Lebens fühlt sich das Altern wie ein langsames Aufglimmen an – subtil, fast höflich. Dann verschiebt sich etwas. Nicht von heute auf morgen, aber unumstößlich. Eine wachsende Zahl von Studien deutet jetzt darauf hin, dass der menschliche Körper um das 50. Lebensjahr einen biologischen Wendepunkt erreicht, an dem das Altern nicht nur weitergeht, sondern beschleunigt.
Diese Idee ist nicht philosophisch. Sie ist molekular. Und sie steht in unseren Proteinen geschrieben.
Wenn der Körper das Tempo ändert
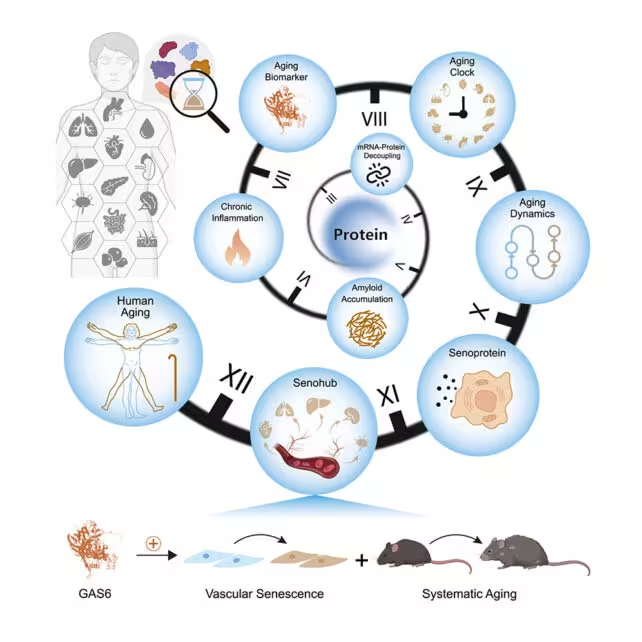
Eine 2025 veröffentlichte Studie unter Leitung von Forscherinnen und Forschern der Chinesischen Akademie der Wissenschaften hat kartiert, wie sich Proteine in verschiedenen menschlichen Geweben über die Zeit verändern. Proteine, die molekularen Maschinen, die Zellen am Laufen halten, fallen nicht einfach gleichmäßig ab. Vielmehr folgen sie je nach Organ unterschiedlichen Verläufen – und diese Verläufe scheinen sich in der Lebensmitte deutlich zu krümmen.
Durch die Analyse von Gewebeproben aus 76 Spenderinnen und Spendern im Alter von 14 bis 68 Jahren konstruierten die Wissenschaftlerinnen und Wissenschaftler sogenannte „proteomische Altersuhren“ – biologische Zeitachsen, die nachverfolgen, wie Gewebe auf molekularer Ebene altern. Ihr Datensatz war ungewöhnlich breit und umfasste 13 Gewebetypen aus wichtigen Körpersystemen, darunter das Herz-Kreislauf-, Immun-, Verdauungs- und Atmungssystem.
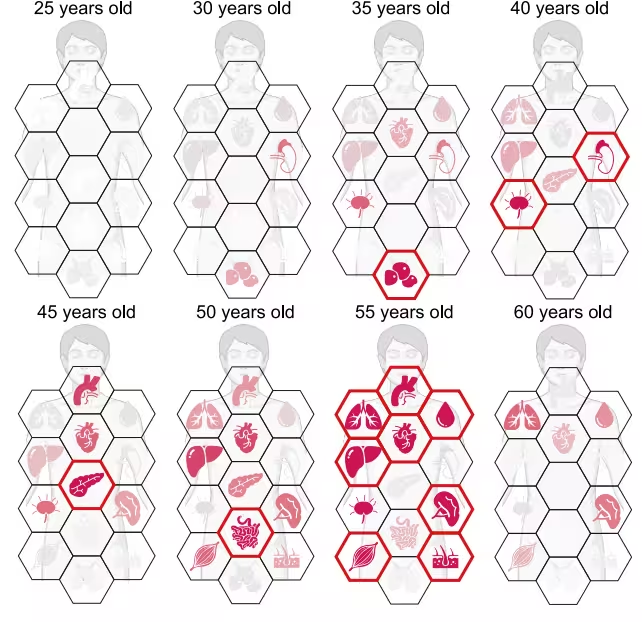
Die Kernaussage? Altern ist keine gleichmäßige Abfahrt. Es ist eher eine Treppe mit spürbaren Stufen. Und eine der steilsten Stufen liegt zwischen etwa 45 und 55 Jahren.
„Wir beobachteten einen klaren Wendepunkt um das 50. Lebensjahr“, stellten die Forschenden fest und verwiesen auf eine Phase, in der mehrere Organe verstärkte molekulare Abnutzungserscheinungen zeigen. Diese Beobachtung beruht nicht nur auf einzelnen Proteinveränderungen, sondern auf systemweiten Mustern, die in den proteomischen Altersuhren sichtbar werden und die biologische Alterung als zeitlich fokussierte, organabhängige Dynamik beschreiben.
Die stille Belastung der Blutgefäße
Nicht alle Organe altern gleich schnell. Einige halten länger durch, andere zeigen frühere Verschleißerscheinungen. Besonders die Blutgefäße scheinen früh und deutlich belastet zu sein.
Die Studie fand heraus, dass die Aorta – die Hauptschlagader des Körpers – während der Lebensmitte einige der dramatischsten Proteinveränderungen durchläuft. Diese Veränderungen betreffen die strukturelle Integrität und Elastizität, zentrale Faktoren für die kardiovaskuläre Gesundheit. Einfach gesagt verlieren die Gefäße, die das Blut im Körper transportieren, an Widerstandsfähigkeit und Anpassungsfähigkeit.
Das erklärt teilweise, warum kardiovaskuläre Erkrankungen häufig in der zweiten Lebenshälfte auftreten oder sich verschlechtern. Es ist nicht nur der Lebensstil, der aufholt, sondern auch die Biologie, die unweigerlich einen Gang höher schaltet. Veränderungen in der Gefäßwandstruktur, der extrazellulären Matrix sowie in entzündungs- und altersassoziierten Signalwegen erscheinen in der Proteomanalyse als frühe Marker für erhöhtes Risiko.
Auch Bauchspeicheldrüse und Milz zeigten bemerkenswerte altersabhängige Verschiebungen. Die Bauchspeicheldrüse, zentral für Verdauung und Blutzuckerregulation, wies Proteinmuster auf, die mit metabolischem Stress und verminderter sekretorischer Kapazität korrelieren. Die Milz, ein zentrales Organ für Immunfunktion und Filterung, zeigte anhaltende molekulare Veränderungen, die erklären können, warum die Immunantwort mit dem Alter schwächer und weniger anpassungsfähig wird.
Proteine erzählen die Geschichte von Krankheiten
Bei tiefergehender Analyse verglichen die Forschenden ihre Proteindaten mit bekannten krankheitsassoziierten Genen und Signalwegen. Sie identifizierten 48 Proteine, deren Expression mit dem Alter zunahm und die mit Erkrankungen wie Herz-Kreislauf-Leiden, Lebererkrankungen, Fibrosen und bestimmten Krebsarten verknüpft sind.
Diese Verbindung zwischen Proteomik und Krankheitsrisiko ist zentral. Sie legt nahe, dass die Saat vieler altersbedingter Erkrankungen lange vor dem Auftreten klinischer Symptome gelegt wird – eingebettet in sich verschiebende Proteinnetzwerke und veränderte Signalwege. Solche Proteine können als frühe Biomarker dienen und erlauben potenziell eine präventive Identifikation vulnerabler Organsysteme.
Mit anderen Worten: Altern ist nicht nur ein Prozess des Abbaus. Es ist auch eine Form der Umprogrammierung, bei der Gewebefunktion, Reparaturmechanismen und stressbedingte Reaktionen neu kalibriert werden. Diese Reprogrammierung kann adaptive und maladaptive Aspekte haben: einige Veränderungen wirken kompensatorisch, andere erhöhen das Risiko für pathologische Entwicklungen.
Altern im Labor testen
Um über reine Beobachtung hinauszugehen, führten die Forschenden ein Experiment an Mäusen durch. Sie isolierten ein Protein, das mit Gefäßalterung assoziiert ist, und führten es jungen Mäusen zu. Die Ergebnisse waren eindrücklich und lieferten funktionale Hinweise auf Kausalität.
Die behandelten Tiere zeigten verringerte körperliche Leistungsfähigkeit: eine schwächere Griffkraft, geringere Ausdauer und schlechtere Koordination im Vergleich zu unbehandelten Tieren. Gleichzeitig trugen sie klare biologische Marker der Gefäßalterung, darunter strukturelle Veränderungen in Gefäßwänden und veränderte Expressionsprofile entzündlicher und matrixassoziierter Proteine.
Dieses Experiment bot etwas Seltenes in der Alternsforschung: eine direkte ursächliche Verbindung zwischen der Veränderung eines einzelnen Proteins und messbaren Zeichen von Alterung in einem ansonsten jungen Organismus. Solche funktionalen Validierungen sind wichtig, weil Korrelationsdaten allein keine kausalen Mechanismen belegen.
Die Ergebnisse unterstreichen zudem die Bedeutung der Muskelkraft – besonders der Griffkraft – als mehr als ein reines Fitnessmaß. Muskelkraft korreliert zunehmend mit allgemeiner Gesundheit, Funktionalität und Resilienz im Alter und dient in klinischen Studien häufig als prognostischer Indikator für Morbidität und Mortalität.
Altern geschieht in Wellen, nicht in Linien
Die Vorstellung einer Beschleunigung des Alterns in der Lebensmitte ist nicht völlig neu. Frühere Untersuchungen aus den USA identifizierten zusätzliche „Peaks“ des Alterns um die 44. und 60. Lebensjahre. Jede Phase war mit unterschiedlichen molekularen Verschiebungen verbunden: von Lipidstoffwechsel und kardiovaskulären Veränderungen bis hin zu Immunregulation und Nierenfunktion.
Was die 2025-Studie besonders auszeichnet, ist ihr systemübergreifender Ansatz. Anstatt sich auf ein Organ oder einen Signalweg zu konzentrieren, erfasst sie Altern als koordinierten, multi-organischen Prozess – unordentlich, ungleichmäßig und tief vernetzt. Diese Perspektive hilft zu verstehen, warum einzelne Biomarker oft nur begrenzte Voraussagekraft haben, während integrative Modelle systemische Vulnerabilitäten besser abbilden.
Ein solcher Wellencharakter des Alterns impliziert kritische Fenster – Zeiträume, in denen gezielte Interventionen besonders wirksam sein könnten. Wenn bestimmte Organe zu vorhersehbaren Zeitpunkten anfälliger werden, eröffnet das Möglichkeiten für zeitlich zugeschnittene Prävention, Monitoring und therapeutische Maßnahmen.
Experteneinschätzung
Dr. Elena Márquez, eine fiktive Biogerontologin am Europäischen Institut für Gesundes Altern, betrachtet diese Erkenntnisse als Wendepunkt für das Verständnis von Langlebigkeit.
„Was hier faszinierend ist, ist nicht nur, dass das Altern beschleunigt, sondern dass es dies in identifizierbaren Phasen tut“, erklärt sie. „Wenn wir genau bestimmen können, wann bestimmte Gewebe besonders verletzlich werden, können wir gezielte Interventionen entwickeln – sei es durch Medikamente, Lebensstilmodifikationen oder Überwachungsstrategien – genau zum richtigen Zeitpunkt.“
Sie ergänzt, dass die Proteomik, die großflächige Untersuchung von Proteinen, bald zu einer Säule der personalisierten Medizin werden könnte. „Wir bewegen uns auf eine Zukunft zu, in der Ihr biologisches Alter nicht eine einzige Zahl ist – es ist eine Landkarte Ihrer Organe, die jeweils in eigenem Tempo altern.“
Was das für die Zukunft der Gesundheit bedeutet
Zu verstehen, wann und wie das Altern beschleunigt wird, öffnet die Tür zu präziserer Gesundheitsversorgung. Anstatt nur auf Krankheit zu reagieren, könnte die Medizin beginnen, sie vorherzusehen und einzugreifen, bevor Schäden irreversibel werden. Das reicht von regelmäßigen proteomischen Screenings bis zu gezielten Interventionen, die auf die jeweils gefährdeten Gewebe abzielen.
Die Forschenden der Studie planen, einen umfassenden Atlas des menschlichen Alterns auf Proteinbasis aufzubauen, der Jahrzehnte des Lebens abdeckt. Ein solcher Atlas könnte helfen, universelle Mechanismen des Alterns zu identifizieren sowie gewebespezifische Verwundbarkeiten aufzuzeigen. Für die Forschung bedeutet dies bessere Modelle, für die Klinik frühere Warnsignale und für die Arzneimittelentwicklung neue Zielstrukturen.
Wenn Altern eine Reihe biologischer Verschiebungen statt eines stetigen Niedergangs ist, könnte das Timing genauso wichtig sein wie die Behandlung.
Diese Einsicht könnte alles verändern – von Präventivmedizin über Medikamentenentwicklung bis hin zu öffentlichen Gesundheitsstrategien. Und für Einzelne liefert sie eine klarere Botschaft: Die Lebensmitte ist nicht nur ein Meilenstein – sie ist ein biologischer Scheidepunkt, an dem gezielte Prävention und Aufmerksamkeit besonders viel bewirken können.
Wichtig ist auch, die Grenzen der aktuellen Forschung zu beachten. Die meisten proteomischen Studien basieren auf Querschnittsanalysen oder begrenzten Kohorten; longitudinale Daten über Jahrzehnte hinweg sind rar, aber entscheidend, um individuelle Alterungsverläufe zuverlässig zu modellieren. Zudem können Lebensstil, Umweltfaktoren und genetische Variabilität die proteomischen Signaturen stark beeinflussen. Künftige Studien sollten deshalb größere, diversere Populationen und wiederholte Messungen über längere Zeiträume einschließen, um die Generalisierbarkeit und prognostische Stärke der proteomischen Altersuhren zu verbessern.
Praktisch könnten nächste Schritte die Entwicklung standardisierter proteomischer Panels für die klinische Anwendung, die Validierung von Proteinen als therapeutische Ziele und die Integration von Proteomik mit Genomik, Metabolomik und klinischen Parametern umfassen. Solche integrativen Ansätze könnten dazu beitragen, personalisierte Präventionspläne zu erstellen, die auf dem molekularen Alter einzelner Organe basieren – ein konkreter Schritt in Richtung präziser, vorausschauender Gesundheitsversorgung.


Kommentar hinterlassen