8 Minuten
Stellen Sie sich vor, man sagt Ihnen, Ihr Blut sei älter als Sie selbst. Nicht als Metapher, sondern als messbare Tatsache. Das ist das provokante Ergebnis einer neuen Studie der Universität Konstanz: ein Satz von Blutmarkern, die zusammen erkennen können, ob jemand schneller oder langsamer altert, als sein Kalenderalter vermuten lässt. Diese Form der Altersbestimmung, oft als biologisches Alter bezeichnet, ergänzt das chronologische Alter um einen molekularen Blick auf Gesundheit, Stoffwechsel und Organfunktion.
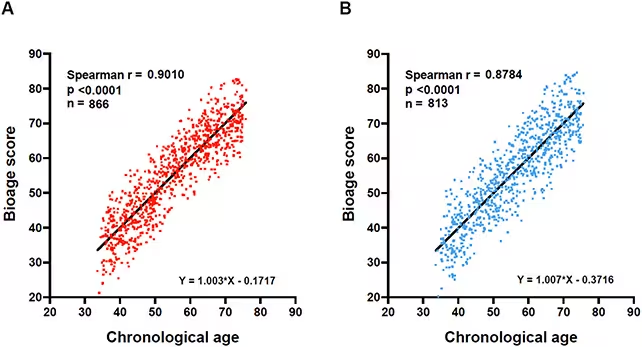
Die Forschenden durchleuchteten eine weite biochemische Landschaft — 362 verschiedene Blutparameter — gewonnen von mehr als 3.300 Erwachsenen im Alter von 35 bis 74 Jahren. Sie suchten nicht nach einer einzigen »Räuberpistole«. Stattdessen ließen sie statistische Modellierung und maschinelles Lernen die Muster identifizieren, die am stärksten mit dem Alter korrelierten. Heraus kamen kompakte Panel-Module: zehn Biomarker für Männer und ein eigenes Set von zehn Biomarkern für Frauen. Jedes Panel ist im Grunde genommen eine Signatur dessen, wie Blut typischerweise in verschiedenen Lebensjahren aussieht.
Wie der Test aufgebaut wurde und warum das Geschlecht eine Rolle spielt
Warum zwei Listen? Weil Männer und Frauen nicht identisch altern. Hormone, Immunreaktionen und Stoffwechselwege divergieren zwischen den Geschlechtern und erzeugen unterschiedliche biochemische Fußabdrücke. Das Konstanzer Team verglich jeden Kandidatenmarker — chemische Substanzen, genetische Signale, zelluläre Parameter und Signalstoffe — mit dem chronologischen Alter. Die Kombinationen, die das Alter am genauesten vorhersagten, behielt man bei. Das Ergebnis ist weniger eine Wunderwaffe als vielmehr ein Mosaik: mehrere Signale, die zusammen das biologische Alter einer Person zuverlässiger schätzen, als es jeder einzelne Marker könnte.
Der Aufbau des Modells folgte bewährten Schritten aus Datenwissenschaft und Epidemiologie: Datenbereinigung, Normalisierung der Messwerte, Auswahlverfahren (Feature Selection) und Validierung mit Kreuzvalidierung. Maschinelles Lernen erlaubte es, nichtlineare Zusammenhänge zu erfassen und Wechselwirkungen zwischen Parametern zu identifizieren. Dabei wurden Faktoren wie Altersspanne, Geschlechtsunterschiede und mögliche Störgrößen (z. B. akute Infektionen) berücksichtigt, um die Robustheit des Scores zu erhöhen.
Die Wissenschaftler prüften ihr Modell anschließend an realen Gruppen, die bereits für verändertes biologisches Altern bekannt sind: Menschen mit Trisomie 21 (Down-Syndrom), regelmäßige Raucher sowie Frauen unter Hormontherapie. Die Panels zeigten plausibel erwartete Verschiebungen: beschleunigte Alterungs-Signaturen bei Rauchern und Personen mit Trisomie 21 sowie differenzierte Veränderungen bei Frauen mit hormoneller Behandlung. Solche Tests erhöhten das Vertrauen, dass der Score kein statistischer Ausreißer ist, sondern ein biologisch bedeutungsvolles Signal darstellt.
„Der biologische Alterungsprozess ist sehr komplex“, konstatiert die Biologin Maria Moreno-Villanueva von der Universität Konstanz. „Er betrifft alle Gewebe und Organe des Körpers und ist nicht das Resultat einer einzigen Ursache.“ Ihr Hinweis unterstreicht eine praktische Wahrheit: Einzelne Biomarker erfassen selten die gesamte Alterungsspirale einer Person. Zusammengesetzte Scores hingegen können ein umfassenderes Bild offenbaren und so für Forschung, Prävention und klinische Studien nützlicher sein.
Treiber und Beobachter: Im Blut Ursachen statt nur Hinweise lesen
Eines der interessanten Ergebnisse der Studie ist die Unterscheidung zwischen Markern, die offenbar das Altern antreiben, und solchen, die es lediglich markieren. Manche Moleküle erscheinen mechanistisch mit dem Alterungsprozess verknüpft — potenzielle Treiber — während andere eher wie Beobachter agieren: informativ, aber nicht ursächlich. Diese Unterscheidung ist wichtig. Wenn ein Biomarker ein Treiber ist, bietet er ein mögliches Ziel für Interventionen. Ist er hingegen nur ein Beobachter, hilft er zwar, Fortschritt zu verfolgen, eignet sich aber weniger für die Entwicklung von Therapien.
Beispiele für potenzielle Treiber, die in älterer Literatur und verwandten Studien immer wieder auftauchen, sind chronische Entzündungsmarker, bestimmte Veränderungen des Lipidstoffwechsels, advanced glycation end products (AGEs) und Hinweise auf mitochondriale Dysfunktion. Beobachtermarker können Parameter sein, die stark mit Alterungsprozessen assoziiert sind, aber eher Folgeprozesse widerspiegeln — etwa einige Leberwerte oder bestimmte Elektrolytverschiebungen. Die Studie in Konstanz nähert sich dieser Trennung mit datengetriebenen Korrelationen und plausibilitätsbasierten Interpretationen, ohne definitive kausale Aussagen für jeden einzelnen Marker zu machen.
Praktische Anwendungen entstehen rasch in der Vorstellung, wenn noch nicht in allen Kliniken. Ein blutbasierter Bioalter-Score könnte verwendet werden, um Patientengruppen für präventive Maßnahmen zu stratifizieren, Veränderungen des Lebensstils zu benchmarken oder zu beurteilen, ob eine Anti-Aging-Therapie mehr leistet, als nur einen einzelnen Laborwert zu beeinflussen. Der Test kann außerdem der öffentlichen Gesundheitsforschung helfen, Trends des biologischen Alterns auf Bevölkerungsebene zu verstehen, wenn Gesellschaften älter werden und Präventionsstrategien geplant werden müssen.
In klinischen Studien könnte ein validierter Bioalter-Score als sekundärer Endpunkt fungieren: etwa um zu prüfen, ob eine Intervention die altersassoziierten biologischen Signaturen verlangsamt. Für die personalisierte Medizin eröffnet sich dadurch die Möglichkeit, Therapien individueller zuzuschneiden — beispielsweise durch gezielte Lifestyle-Empfehlungen, differenzierte Medikamentenwahl oder Monitoring von Risiko-Scores über die Zeit.
„Vor dem Hintergrund aktueller Forschung zu den Alterungseffekten von Rauchen, Hormonersatztherapie oder Trisomie 21 sind all diese Resultate plausibel und bestätigen die Validität unseres Bioalter-Scores“, sagt der Molekulartoxikologe Alexander Bürkle von derselben Institution. Solche externe Plausibilität ist beruhigend, wenn ein Modell auf komplexen Daten und fortgeschrittenen Algorithmen beruht — sie reduziert das Risiko, dass ein gutes Modell nur eine Artefakt-Konstruktion der Datensätze ist.
Experteneinschätzung
Dr. Elena Ross, eine Gerontologin, die nicht an der Studie beteiligt war, gibt eine Warnung und einen Impuls: „Zusammengesetzte Blut-Scores sind ein starker Schritt zu individualisierten Alterungsbewertungen, aber wir dürfen nicht vergessen, dass sie probabilistisch sind. Sie geben Risiko und Trend an, nicht Schicksal. Richtig eingesetzt, können sie gezielte Prävention motivieren und helfen, Interventionen zu bewerten.“ Ihre Aussage spiegelt das doppelte Versprechen und die Grenze der Studie wider: mehr Präzision ohne absolute Gewissheit.
Über die rein diagnostische Anwendung hinaus eröffnet dieser Ansatz neue Forschungswege. Die Unterscheidung von Treibern und Beobachtern fokussiert Laborarbeit auf Mechanismen; groß angelegte Panels ermöglichen Längsschnittstudien, die nicht nur fragen, wer schneller altert, sondern auch warum — und ob dieses Tempo verlangsamt oder umgekehrt werden kann. Die Konstanzer Arbeit kann als Blaupause gesehen werden: reich an Daten, sorgfältiger Modellbildung und Validierung an realen Gruppen.
Es gibt auch eine ethische und soziale Dimension. Wenn ein Bluttest jemanden biologisch älter einstuft als seine Altersgenossen: Wie soll mit dieser Information umgegangen werden? Versicherungen, Beschäftigung und psychologische Folgen müssen bedacht werden, sobald solche Werkzeuge breiter eingesetzt werden. Datenschutz, Einwilligung und der verantwortungsvolle Umgang mit Prognoseinformationen sind dabei zentrale Punkte. Für den Moment liegt der unmittelbare Wert im Wissenschaftlichen: ein kompakteres, praktisches Testverfahren für biologisches Altern und eine schärfere Linse auf die Biologie dahinter.
Wenn Forschende Menschen gleichen Geburtsjahrs gruppieren und ihre Bioalter-Scores betrachten, fällt die Streuung ins Auge. Einige Personen erscheinen auf molekularer Ebene Jahrzehnte jünger, andere deutlich älter. Diese Variabilität erinnert daran, dass das chronologische Alter nur einen Teil der Geschichte erzählt. Der Rest ist in unserem Blut geschrieben — und immer häufiger lesbar, wenn man weiß, wie man hinschaut. Die wachsende Forschung zu Blutmarkern, Biomarkern und dem biologischen Alter führt zu einem differenzierteren Verständnis von Gesundheit, Lebensstil und Prävention.
Für Ärztinnen und Ärzte, Forschende in der Altersforschung sowie Anbieter von Präventionsprogrammen bedeutet das: Ein validierter Bioalter-Test kann helfen, Risikopatienten frühzeitig zu identifizieren, Interventionen gezielter zu gestalten und individuelle Verläufe über Jahre hinweg zu verfolgen. Für die öffentliche Gesundheit eröffnet sich die Chance, altersbezogene Belastungsprofile in Populationen zu erfassen und damit Ressourcen effektiver zu planen.
Abschließend bleibt festzuhalten: Blutbasierte Bioalter-Modelle sind keine Zauberkugel, sondern datengetriebene Werkzeuge. Sie ergänzen bestehende klinische Parameter, verbessern die Risikoeinschätzung und liefern Hypothesen für mechanistische Forschung. Ihre Weiterentwicklung wird stark davon abhängen, wie gut unabhängige Studien die gefundenen Muster reproduzieren, wie repräsentativ die Stichproben sind und wie transparent Algorithmen und Validierungsprotokolle offengelegt werden. Mit dem Fortschreiten der Altersforschung dürfte sich die Genauigkeit solcher Scores weiter erhöhen — und damit ihr Nutzen für Medizin, Prävention und Gesellschaft.


Kommentar hinterlassen