8 Minuten
Neue Belege verbinden Gehirngeometrie mit kognitivem Abbau
Eine aktuelle, multi-institutionelle Studie deutet darauf hin, dass subtile Veränderungen in der dreidimensionalen Form des Gehirns Hinweise auf zukünftigen kognitiven Abbau und ein erhöhtes Demenzrisiko geben können. Forschende analysierten mehrere tausend MRT-Aufnahmen, um zu kartieren, wie sich die Gehirngeometrie mit dem Alter verändert und wie diese Verschiebungen mit Einbußen bei Gedächtnis, Schlussfolgerungsvermögen und anderen kognitiven Funktionen korrelieren.
Die Untersuchung unter Federführung von Teams an der University of California, Irvine (UC Irvine) und der Universidad de La Laguna in Spanien erweitert den Fokus von reinem Gewebeverlust auf die Gesamtmorphologie des Gehirns — also die räumliche Anordnung und Krümmung einzelner Regionen. Anstatt nur zu fragen, wie viel Volumen das Gehirn verliert, betrachteten die Forschenden, wie sich die Oberfläche und die innere Struktur des Gehirns über die Zeit verformen und ob diese Deformationen mit schlechteren Ergebnissen in kognitiven Tests übereinstimmen.
Studienaufbau und Methodik
Die Autorinnen und Autoren analysierten 2.603 MRT-Gehirnscans von Erwachsenen im Alter von 30 bis 97 Jahren, verfolgten Form- und Strukturveränderungen in spezifischen Regionen und verglichen diese Muster mit standardisierten kognitiven Tests. Fortschrittliche Bildverarbeitungs- und statistische Mapping-Verfahren ermöglichten es dem Team, Areale zu identifizieren, die konsistent mit dem Alter expandierten oder sich zusammenzogen, und zu prüfen, ob diese Muster bei Personen mit messbaren kognitiven Einschränkungen stärker ausgeprägt waren.
Die Methodik kombiniert robuste Querschnittsdaten mit longitudinalen Messungen, präziser regionaler Formmodellierung und Korrelationen zu Domänen-spezifischen kognitiven Scores (z. B. episodisches Gedächtnis, Arbeitsgedächtnis, Exekutivfunktionen). Technologien wie nichtlineare Registrierungs-Algorithmen, sphärische Harmonisierung und multivariate statistische Modelle wurden eingesetzt, um altersassoziierte Deformationsfelder auf Populationsebene zu extrahieren und regional zu vergleichen.
Wesentliche methodische Punkte
- Große Kombination aus Querschnitts- und Längsschnitt-MRT-Datensatz mit Abdeckung von mittlerem Erwachsenenalter bis ins hohe Alter.
- Regionale Formmodellierung statt ausschließlich globaler Volumenmaße.
- Kognitive Scores wurden genutzt, um Teilnehmende nach Leistung in Gedächtnis, Schlussfolgerung und weiteren Domänen zu stratifizieren.
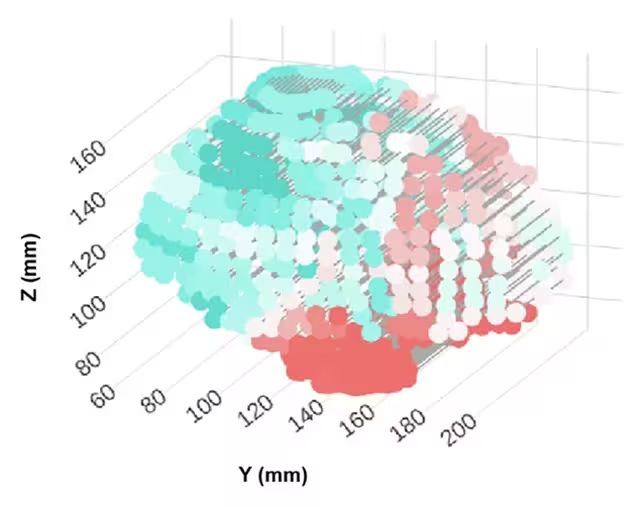
Die Studie erzeugte regionale Karten altersbedingter Expansionen und Kontraktionen in der Gehirngeometrie und verknüpfte diese mit kognitiven Testergebnissen. Die Autorinnen und Autoren präsentierten diese Karten und die analytischen Resultate in ihrer Veröffentlichung. (Escalante et al., Nat. Commun., 2025)
Hauptergebnisse und Implikationen
Die räumlichen Veränderungen waren nicht gleichmäßig verteilt: Posterior gelegene Regionen (hintere Hirnareale) zeigten tendenziell stärkeren altersbedingten Schwund, und diese Reduktionen korrelierten mit schlechteren Ergebnissen in Aufgaben des logischen Schlussfolgerns. Bei einigen Individuen war das Muster ungleichmäßiger Expansion und Kompression über Hirnregionen stärker ausgeprägt und stand in Verbindung mit kognitiven Beeinträchtigungen.
Diese Beobachtungen legen nahe, dass die Verteilung struktureller Veränderungen — nicht nur das insgesamt verlorene Volumen — für die Hirngesundheit relevant ist. Die regionale Heterogenität der Deformationen könnte funktionelle Netzwerke unterschiedlich belasten und so dominoartige Effekte auf kognitive Domänen auslösen.
Eine besonders wichtige Schlussfolgerung betrifft den entorhinalen Kortex, eine kompakte Region, die als zentraler Hub für Gedächtnisnetzwerke fungiert und zu den ersten Arealen gehört, die von Alzheimer-Pathologie betroffen sind. Die Forschenden schlagen vor, dass altersbedingte Verschiebungen in der angrenzenden Gehirngeometrie mechanischen Stress auf den entorhinalen Kortex ausüben könnten, indem sie ihn gegen nahegelegene, weniger nachgiebige Strukturen drücken. Diese mechanische Belastung könnte die Vulnerabilität gegenüber der Ansammlung toxischer Proteine erhöhen, die mit Alzheimer in Verbindung gebracht werden (z. B. Amyloid-β, Tau).
Der Neurowissenschaftler Niels Janssen (Universidad de La Laguna) fasste die Perspektivverschiebung zusammen: Statt sich ausschließlich darauf zu konzentrieren, wie viel Gewebe mit dem Alter verschwindet, sei es wichtig, systematische Veränderungen der Form des Gehirns zu kartieren und zu untersuchen, wie diese mit kognitiven Leistungen verknüpft sind. Michael Yassa (UC Irvine) ergänzte, dass geometrische Überlegungen dabei helfen könnten zu erklären, warum der entorhinale Kortex häufig zum "Ground Zero" der Alzheimer-Pathologie wird, und dass diese Einsichten neue Wege für frühe Erkennung und Intervention eröffnen könnten.
Zukünftige Forschungsrichtungen und Bedürfnisse
Die Studie stellt einen frühen, aber wichtigen Schritt dar. Forschende heben hervor, dass größere longitudinale Datensätze, hochauflösende Bildgebung und die Integration molekularer Marker (beispielsweise PET-Scans, die Amyloid und Tau quantifizieren) erforderlich sind, um Kausalität zu klären: Gehen Formveränderungen der Proteinausscheidung voraus, oder sind sie eine Folge davon? Zu beachten ist, dass Korrelationen allein keine Ursache-Wirkungs-Beziehungen beweisen.
Verbesserte biomechanische Modelle, die die tatsächlichen physikalischen Kräfte und Materialeigenschaften des Hirngewebes berücksichtigen, könnten erklären, warum sich manche Regionen mit dem Alter ausdehnen, während andere kontrahieren. Solche Modelle in Kombination mit populationsdiversen Datensätzen (Alter, Geschlecht, Ethnizität, vaskuläre Risikofaktoren) sind notwendig, um individuelle Unterschiede in der Anfälligkeit für ausgeprägte geometrische Verschiebungen zu verstehen.
Weitere Forschungsschwerpunkte umfassen:
- Validierung von Form-basierten Biomarkern in unabhängigen Kohorten und klinischen Studien.
- Integration mit genetischen Risikofaktoren (z. B. APOE) und vaskulären Markern, um multifaktorielle Modelle des Demenzrisikos zu entwickeln.
- Entwicklung automatisierter, reproduzierbarer Pipeline-Tools für die klinische Anwendung von Formmetriken in der MRT-Analyse.
- Untersuchung, ob gezielte Interventionen (Lifestyle, pharmakologische Ansätze) Formveränderungen modulieren und damit kognitive Verläufe beeinflussen können.
Die klinischen Perspektiven beinhalten die mögliche Nutzung automatisierter, MRT-basierter Formmetriken, um Personen mit erhöhtem Demenzrisiko früher als durch konventionelle Volumenmessungen zu identifizieren. Wenn sich Form-basierte Biomarker validieren lassen, könnten sie kognitive Tests und biochemische Marker ergänzen und so Diagnosegenauigkeit und das Timing therapeutischer Maßnahmen verbessern.
Technische Details und methodische Robustheit
Um die Verlässlichkeit solcher Befunde zu gewährleisten, sind mehrere technische Aspekte entscheidend: Zunächst muss die Bildqualität konsistent hoch sein; hochauflösende T1-gewichtete Sequenzen reduzieren Artefakte in der Oberflächenrekonstruktion. Zweitens erfordern Formanalysen robuste Oberflächen- und Volumenregistrierungen sowie Methoden zur Korrektur von Kopfbewegung und Scanner-Variabilität. Drittens sollten statistische Modelle multivariate Confounder berücksichtigen (Bildgebungsplattform, Bildungsniveau, vaskuläre Risikofaktoren, depressive Symptome), um verzerrte Assoziationen zu vermeiden.
Die Nutzung moderner Machine-Learning-Ansätze kann helfen, komplexe Muster regionaler Deformationen zu erkennen und diese mit multidimensionalen klinischen Endpunkten zu verknüpfen. Allerdings ist Transparenz in Modellarchitektur und Validierung essenziell, um Überanpassung zu verhindern und klinische Interpretierbarkeit zu erhalten.
Klinische Relevanz und mögliche Anwendungsfälle
Für die klinische Praxis bieten formbasierte Analysen mehrere potenzielle Vorteile:
- Frühzeitige Risikostratifizierung: Patienten mit charakteristischen Deformationsmustern könnten frühzeitig identifiziert und enger überwacht werden.
- Ergänzende Diagnostik: Formmetriken könnten neben neuropsychologischen Tests und molekularen Biomarkern zusätzliche Informationen liefern, insbesondere in Fällen mit unscharfem klinischem Bild.
- Präzisionsmedizin: Regionalspezifische Muster erlauben differenziertere Vorhersagen über betroffene kognitive Domänen und könnten individualisierte Therapieziele ermöglichen.
Wichtig ist, dass solche Anwendungen erst nach unabhängiger Validierung und klinischer Nutzbarkeitsstudien in Routinediagnostik übernommen werden sollten. Ethische Aspekte (z. B. Kommunikation von erhöhtem Demenzrisiko) und ökonomische Bewertung (Kosten-Nutzen bei flächendeckender Implementierung) müssen ebenfalls berücksichtigt werden.
Expertinnen- und Experteneinschätzungen
Dr. Laura Mendes, kognitive Neurowissenschaftlerin (fiktiv), kommentierte: "Diese Forschung stellt Altern als nicht nur ein Problem des Gewebeverlusts, sondern auch der architektonischen Umgestaltung dar. Hirnregionen sind in einen physischen Raum eingebettet; wenn dieser Raum sich neu formt, können verletzliche Hubs mechanisch belastet werden. Die Kombination von Geometrie-Analysen mit molekularer Bildgebung könnte die Früherkennung deutlich verbessern."
Solche Expertinnen- und Expertenkommentare unterstreichen, dass interdisziplinäre Ansätze — die Neuroanatomie, Bildverarbeitung, Biomechanik und molekulare Neurologie verbinden — besonders vielversprechend sind, um die Pathophysiologie kognitiver Erkrankungen besser zu verstehen.
Schlussfolgerung
Die Studie macht deutlich, dass die 3D-Geometrie des Gehirns — seine Form und die regionalen Deformationsmuster — relevante Informationen über das kognitive Altern und das Demenzrisiko enthält. Das Tracking dieser Formveränderungen parallel zu etablierten Biomarkern (z. B. Amyloid-/Tau-PET, Liquorbiomarker) könnte neue Wege für frühe Erkennung, Risikostratifizierung und gezielte Versorgungsstrategien eröffnen. Weitergehende Forschung ist notwendig, um Kausalmechanismen zu klären, Form-basierte Biomarker zu validieren und standardisierte, klinisch anwendbare Analysetools zu entwickeln.
Insgesamt erweitert die Integration von Gehirngeometrie in die neurodegenerative Forschung die Perspektive von einfachen Volumenmessungen hin zu einem differenzierten Verständnis von Architektur, Belastung und regionaler Vulnerabilität — ein Schritt, der die Präzision der Neurologie und Demenzforschung verbessern könnte.
Quelle: sciencealert

Kommentar hinterlassen