8 Minuten
Forscher, die Proben von Maria Branyas analysierten — sie starb 2024 im Alter von 117 Jahren — fanden eine überraschende Kombination aus jugendlichen genetischen und physiologischen Merkmalen, die zur Erklärung ihrer außergewöhnlichen Lebensspanne beitragen könnten. Die Studie, geleitet von Epigenetikern in Barcelona, hebt seltene DNA‑Varianten, ein widerstandsfähiges Immunprofil und Stoffwechselmerkmale hervor, die eher jüngeren Personen ähneln und Hinweise auf Mechanismen für gesunde Langlebigkeit liefern.
Was das Genom und die Biomarker zeigten
Die Forscher sammelten Blut, Speichel, Urin und Stuhlproben von Branyas vor ihrem Tod und analysierten ihr Genom, epigenetische Muster, das Lipidprofil, Immunzellpopulationen und das Darmmikrobiom. Auf mehreren Analyseebenen verhielten sich viele Zelltypen so, als seien sie deutlich jünger als das chronologische Alter. Dieses "jugendliche" Signal zeigte sich in DNA‑basierten Messungen des biologischen Alters, in Genvarianten, die mit kardiovaskulärer und neuronaler Gesundheit in Verbindung stehen, sowie in ungewöhnlich günstigen Cholesterin‑ und Entzündungswerten.
Insbesondere fiel ein geringes Niveau systemischer Entzündung auf, kombiniert mit sehr niedrigen Werten für LDL‑Cholesterin und Triglyceride sowie einem ungewöhnlich hohen HDL‑Cholesterin. Solche metabolischen Profile sind in epidemiologischen Studien häufig mit reduziertem Risiko für Herz‑Kreislauf‑Erkrankungen assoziiert. Zusätzlich trug ihr Immunsystem Signaturen, die eher jüngeren Kohorten entsprechen: Hinweise auf erhaltene naive und regulatorische T‑Zell‑Anteile, eine reduzierte proinflammatorische Zytokinantwort und eine Immunprofilbalance, die mit besserer Pathogenabwehr und reduziertem chronischem Entzündungsdruck in Verbindung gebracht wird.
Das Darmmikrobiom zeigte Merkmale, die in anderen Studien mit metabolischer Gesundheit und entzündungshemmender Wirkung verknüpft wurden, darunter erhöhte Diversität und das Vorhandensein SCFA‑produzierender Bakterien, die kurzkettige Fettsäuren wie Butyrat bilden. Insgesamt deuten diese Befunde auf ein koordiniertes Netzwerk von genetischen, immunologischen und metabolischen Faktoren hin, die die sogenannte Healthspan — die Zeitspanne, die in relativ guter Gesundheit verbracht wird — unterstützten.

Maria Branyas an ihrem 117. Geburtstag
Telomere, Krebsrisiko und ein Paradoxon
Ein überraschender Befund war die starke Erosion der Telomere, der schützenden Kappen an den Enden der Chromosomen. Kurzere Telomere werden klassisch mit erhöhter Mortalität und zellulärem Altern assoziiert, weshalb dieser Befund auf den ersten Blick paradox erscheint. Die Autoren der Studie schlagen eine mögliche Erklärung vor: sehr kurzlebige Zellen könnten die Chance für die Expansion maligner Klone verringern, weil potenziell entartete Zellen schneller eliminiert oder durch gewebsinterne Mechanismen ersetzt werden. In diesem Szenario reduziert die Telomerverkürzung das Krebsrisiko, obwohl sie andere Alterszeichen begünstigen kann.
Bei Branyas führten kurze Telomere jedoch nicht zu einem deutlich schlechteren Gesundheitszustand; vielmehr koexistierten sie mit Biomarkern physiologischer Resilienz. Das Ergebnis illustriert eine zentrale Lehre der Alternsforschung: Einzelne Biomarker erzählen selten die ganze Geschichte. Telomerlänge, epigenetisches Alter, Entzündungsmarker, genetische Varianten und Lebensstilfaktoren interagieren komplex und nicht linear, sodass ein isolierter Indikator nur begrenzte Aussagekraft hat.
Genetische Faktoren spielten bei Branyas eindeutig eine Rolle. Das Team identifizierte seltene Varianten, die mit Langlebigkeit, immunologischer Kompetenz und kardiovaskulärem Schutz assoziiert sind. Solche Varianten können funktionelle Effekte haben, etwa auf Stressreaktionen, Lipidstoffwechsel oder DNA‑Reparaturpfade. In der Literatur werden Gene wie FOXO3, CETP oder bestimmte APOE‑Allele wiederholt als Kandidaten für Schutzmechanismen genannt; die Studie betont jedoch die Notwendigkeit, solche Assoziationen robust in größeren Kollektiven zu bestätigen.
Breiter wissenschaftlicher Kontext und Implikationen
Obwohl die Untersuchung sich auf eine einzige außergewöhnliche Person konzentriert, passen die Ergebnisse zu größeren Kohortenstudien, die bei Hundertjährigen und Supercentenarians charakteristische Biomarker gefunden haben. Solche Kohorten zeigen häufig eine Kombination aus protektiven Genvarianten, günstigen Lipidprofilen, geringerer systemischer Entzündung und einem resilienten Mikrobiom. Die Identifikation kombinierter Merkmale — also Multimarker‑Signaturen — liefert Forscherteams plausible Kandidaten für Biomarker des gesunden Alterns.
Solche Marker sind wertvoll, weil sie zwei Ziele ermöglichen: erstens die bessere Risikostratifikation in epidemiologischen Studien, zweitens die Entwicklung zielgerichteter Interventionen, die sowohl Lebensdauer als auch Healthspan verbessern könnten. In der Praxis könnten kombinierte Profile helfen, Personen zu identifizieren, die von präventiven Maßnahmen besonders profitieren, oder molekulare Zielstrukturen für Medikamente aufzudecken.
Die Autorinnen und Autoren mahnen jedoch zu Vorsicht: Befunde aus einer Einzelfallstudie lassen sich nicht ohne Weiteres verallgemeinern. Sie fordern größere, gut kontrollierte Studien, die außergewöhnlich langlebige Individuen mit kürzer lebenden Peers vergleichen, um Kandidatenbiomarker zu validieren und kausale von bloß korrelativen Merkmalen zu trennen. Längsschnittdaten, funktionelle Experimente und interdisziplinäre Ansätze — von Genetik über Immunologie bis hin zur Mikrobiomforschung — sind notwendig, um belastbare Schlussfolgerungen zu ziehen.
Mögliche Strategien, die sich aus den Befunden ableiten lassen
Eine direkte Übertragbarkeit der Ergebnisse auf die Allgemeinbevölkerung wäre verfrüht. Dennoch legt die Studie mehrere Forschungsrichtungen nahe:
- Langzeitmonitoring epigenetischer Altersmarker (Epigenetic Clocks) in der mittleren Lebensphase, um Interventionseffekte abzubilden.
- Vertiefte Studien zur Immunresilienz, etwa zur Erhaltung naiver T‑Zell‑Kompartimente und zur Balance pro‑ und antiinflammatorischer Reaktionen.
- Systematische Untersuchung von Mikrobiomkonstellationen, die mit metabolischer Gesundheit und geringer inflammatorischer Aktivierung verknüpft sind.
- Suche nach protektiven genetischen Varianten als Ausgangspunkt für Wirkstoffentwicklung oder als Biomarker für personalisierte Prävention.
Translational orientierte Forschung könnte testen, ob therapeutische Maßnahmen wie die gezielte Verbesserung von Lipidprofilen (beispielsweise durch Ernährung, Bewegung, oder medikamentöse Maßnahmen), die Reduktion chronischer Entzündungsprozesse oder die Modulation spezifischer Immunpfade messbare Verbesserungen in biologischen Altersmaßen bewirken. Auch Lebensstilinterventionen, die nachweislich HDL erhöhen oder Entzündungsmarker senken — etwa mediterrane Ernährung, regelmäßige körperliche Aktivität und soziale Integration — sind praktikable Ansatzpunkte für Interventionsstudien.
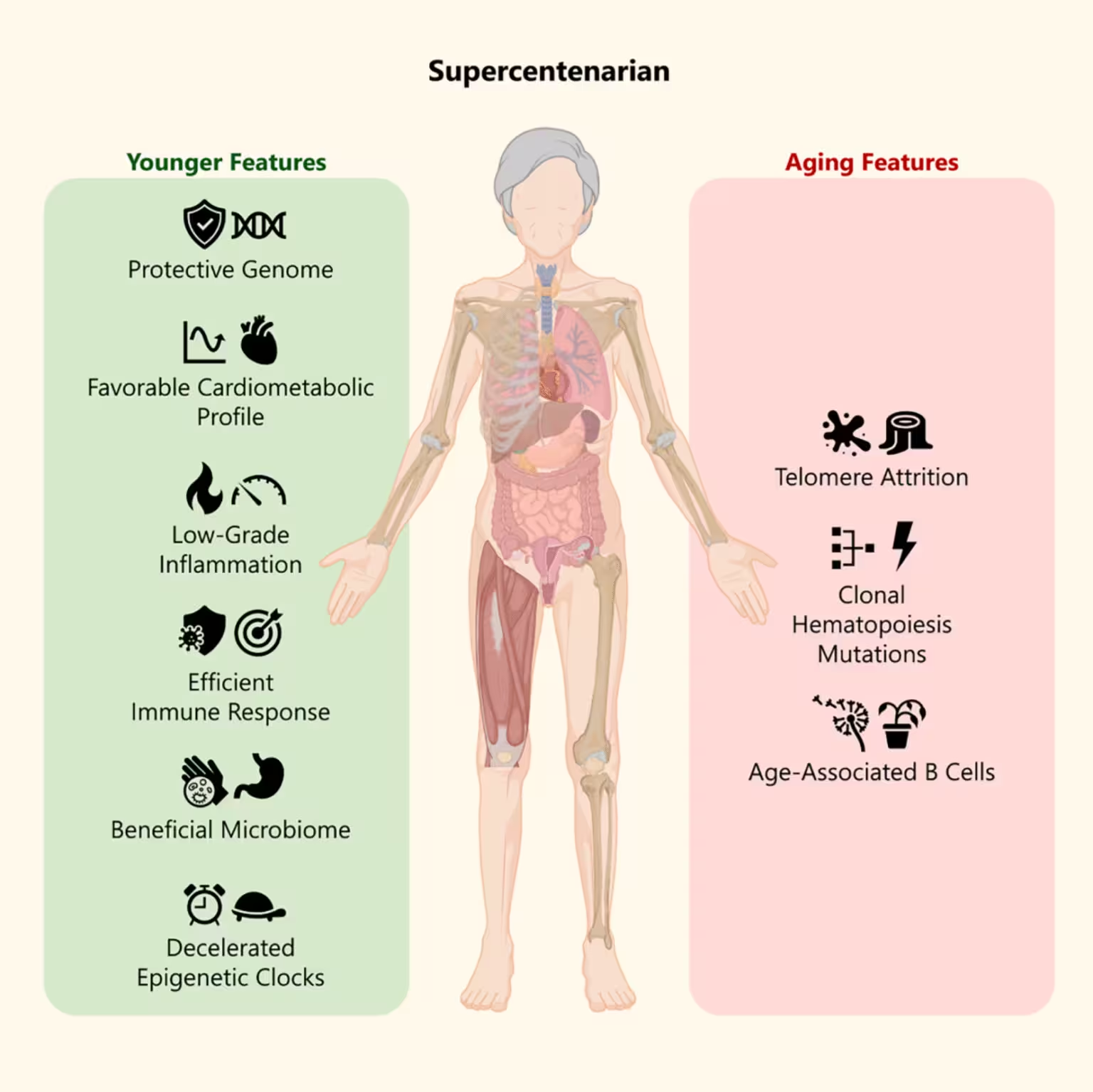
Jüngere und altersbedingte Merkmale von Maria Branyas.
Fachliche Einordnung
"Einzelfallstudien wie diese sind seltene Fenster in das menschliche Altern", erklärt Dr. Elena Márquez, eine hypothetische Forscherin aus dem Bereich Geroscience. "Sie liefern keine endgültigen Antworten, weisen aber auf Mechanismen hin, die in größeren Gruppen getestet werden sollten. Das gleichzeitige Auftreten jugendlicher epigenetischer Signaturen, eines vorteilhaften Immunprofils und günstiger Lipidwerte legt eine multisystemische Koordination nahe — genau das ist ein Ziel für Therapien, die gesunde Lebensjahre verlängern sollen."
Aus wissenschaftlicher Sicht sind mehrere technische und methodische Aspekte wichtig: die Reproduzierbarkeit molekularer Messungen über Plattformen hinweg, die Standardisierung von Protokollen für die Analyse des Mikrobioms sowie die Einbindung funktioneller Assays, um die biologischen Effekte identifizierter Varianten zu prüfen. Studien, die genomische Daten mit Transkriptom-, Proteom‑ und Metabolomdaten kombinieren — sogenannte Multi‑Omics‑Ansätze — sind besonders geeignet, komplexe Interaktionen zwischen Genetik, Immunität, Stoffwechsel und Mikrobiom sichtbar zu machen.
Darüber hinaus ist die epidemiologische Kontextualisierung entscheidend. So können demografische Faktoren, sozioökonomischer Status, frühere Infektionsereignisse und Lebensstilfaktoren wie Ernährung, Bewegung und soziale Einbindung die Interpretation biomolekularer Signale stark beeinflussen. In Branyas Fall werden eine aktive soziale Teilhabe, regelmäßige körperliche Aktivität und eine mediterran angelegte Ernährung als wahrscheinliche unterstützende Faktoren genannt, die mit den molekularen Befunden plausibel interagieren.
Schlussfolgerung
Das biologische Profil von Maria Branyas zeigt, dass extremes Alter mit bemerkenswerter physiologischer Resilienz koexistieren kann. Ihr Genom und die multiomischen Signaturen liefern Hypothesen zu Schutzmechanismen gegen altersbedingte Krankheiten. Die nächsten Schritte bestehen in größeren, kontrollierten Studien, die bestimmen, welche genetischen und molekularen Merkmale verlässlich als Prädiktoren für gesunde Langlebigkeit dienen und welche Befunde eher dem individuellen Lebenslauf dieser einzigartigen Person geschuldet sind.
Für die klinische und translationale Forschung bedeutet dies: Identifizierte Biomarker sollten systematisch validiert werden. Langfristige Interventionsstudien können prüfen, ob gezielte Maßnahmen — sei es auf genetisch basierte Therapien, immunmodulierende Behandlungen, Mikrobiom‑Manipulation oder Lebensstilinterventionen — biologische Altersmaßen verschieben und so die Healthspan nachhaltig verlängern. Die Kombination aus molekularer Diagnostik, epidemiologischer Validierung und klinischer Testung ist der Weg, um belastbare Erkenntnisse zu gewinnen, die über Einzelfälle hinausgehen.
Quelle: sciencealert


Kommentar hinterlassen