7 Minuten
Forscher an der University of Vermont haben eine überraschende molekulare Bremse für Drucksensoren in Blutgefäßen des Gehirns identifiziert — und das Wiederherstellen dieser Bremse könnte einen neuen therapeutischen Weg darstellen, um reduzierte zerebrale Durchblutung und bestimmte Formen von Demenz zu behandeln. Die Entdeckung weist auf ein Membranphospholipid namens PIP2 als potenziellen Ansatzpunkt, um die Mikrozirkulation zu normalisieren und die Gehirnfunktion zu schützen.
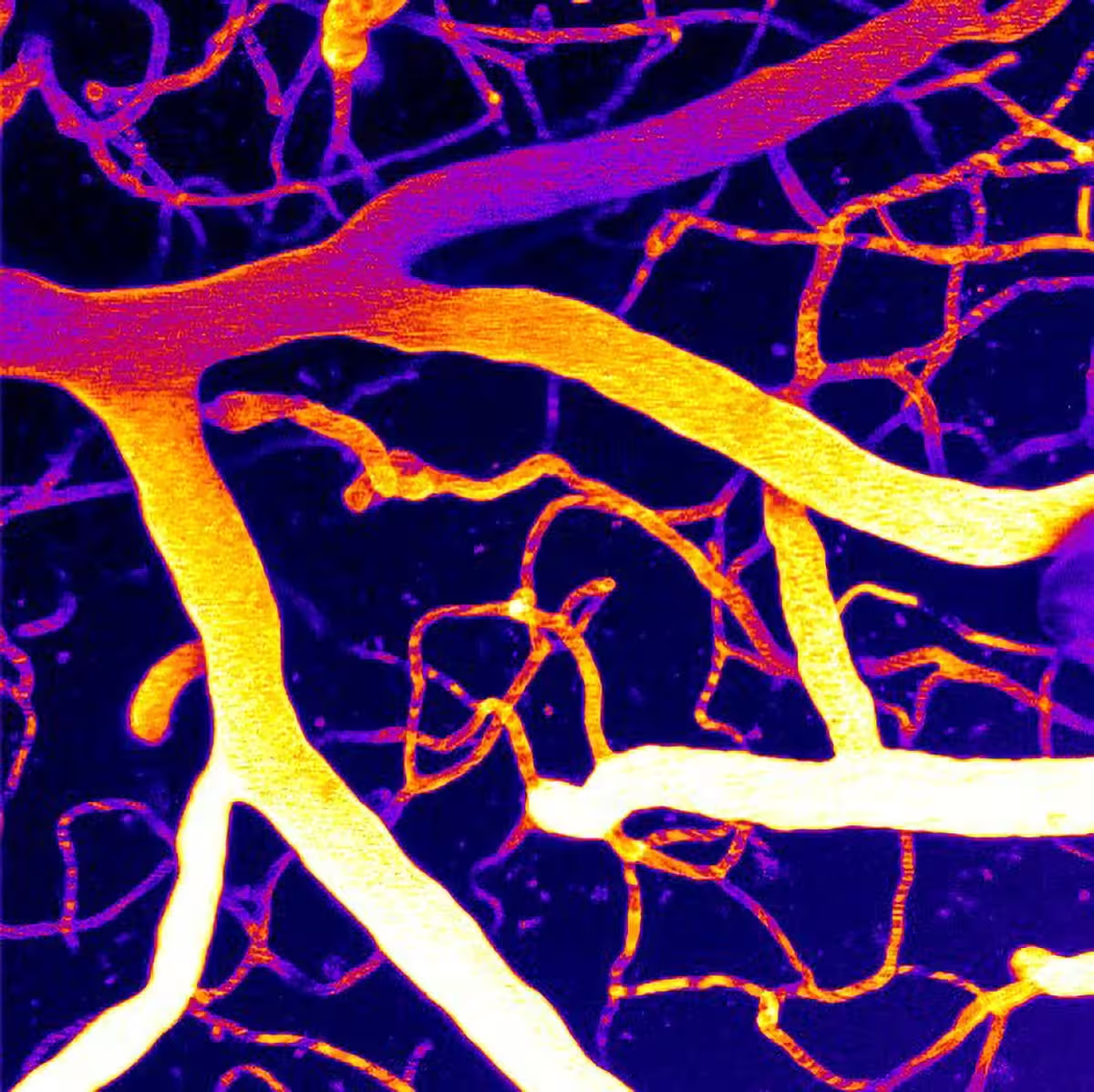
Die Mikrozirkulation eines Gehirns, aufgenommen mit Zwei-Photonen-Laserscanning-Mikroskopie.
Wie ein Membranlipid die Hirndurchblutung stabil hält
Die Aufrechterhaltung einer stabilen Durchblutung im Gehirn beruht auf fein abgestimmten Signalen zwischen Blut, Gefäßwand und dem umgebenden Nervengewebe. Zentral in dieser Regulation steht Piezo1, ein mechanosensitiver Ionenkanal, der in vaskulären Zellen exprimiert wird. Piezo1 öffnet sich als Reaktion auf mechanische Kräfte, die durch den Blutfluss entstehen, und hilft Blutgefäßen, ihren Tonus und Durchmesser anzupassen.
In präklinischen Arbeiten, veröffentlicht in Proceedings of the National Academy of Sciences, zeigte das Team unter Leitung von Osama Harraz, Ph.D., am Larner College of Medicine, dass die Aktivität von Piezo1 außer Kontrolle geraten kann, wenn ein Membranphospholipid — Phosphatidylinositol 4,5-bisphosphat (PIP2) — vermindert ist. PIP2 ist bekannt dafür, viele Ionenkanäle und Signaltransduktionswege zu regulieren. In diesem Fall wirkt PIP2 wie ein natürlicher Hemmstoff von Piezo1: Fallen die PIP2-Spiegel, wird Piezo1 überaktiv und stört die zerebrale Blutversorgung.
Mechanistisch ist zu beachten, dass Piezo1-Calciumströme kurzfristig vasodilatatorische oder vasokonstriktorische Effekte auslösen können, abhängig von der Zellart (Endothelzellen versus glatte Muskelzellen) und dem lokalen Kontext. PIP2-interagierende Mechanismen beeinflussen sowohl die Kanal-Gating-Eigenschaften als auch die Membrankomposition — Faktoren, die für die Hämodynamik auf Mikroebene entscheidend sind. Für die Optimierung zukünftiger Therapien ist eine genaue Kenntnis dieser Wechselwirkungen essenziell.
Vom Labor zur verbesserten Mikrozirkulation: PIP2 wiederherstellen
In Tiermodellen testeten Harraz und Kolleginnen, ob die Auffüllung von PIP2 Piezo1 zügeln und die normale Durchblutung wiederherstellen kann. Ihre Ergebnisse zeigten, dass die Wiederherstellung von PIP2 überaktive Piezo1-Signale unterdrückte und zur Normalisierung der mikrovenösen und arteriellen Zirkulation im Gehirn beitrug. Diese vaskulären Änderungen gingen mit verbesserten Perfusionsparametern einher, die häufig bei Demenzpatienten gestört sind, darunter verringerter zerebraler Blutfluss (CBF) und beeinträchtigte Mikrozirkulation.
Die Experimente umfassten elektrophysiologische Messungen, live-Bildgebung der Gefäßreaktion und funktionelle Perfusionsmessungen. Durch den Einsatz von zwei-Photonen-Laserscanning-Mikroskopie konnten die Forscher Veränderungen in der Kapillardynamik und im Gefäßtonus in Echtzeit beobachten. Solche technischen Kombinationen erhöhen die Robustheit der Befunde und liefern direkte Hinweise darauf, wie Lipid‑Kanal-Interaktionen die Mikrozirkulation beeinflussen.
Harraz kommentierte die Bedeutung der Ergebnisse: "Diese Entdeckung ist ein großer Schritt vorwärts in unseren Bemühungen, Demenz und neurovaskuläre Erkrankungen zu verhindern. Wir entschlüsseln die komplexen Mechanismen dieser verheerenden Erkrankungen und können nun beginnen, darüber nachzudenken, wie sich diese Biologie in Therapien übersetzen lässt." Die Aussage unterstreicht sowohl das therapeutische Potenzial als auch die frühen Stadien der translationalen Entwicklung.
Warum das für Alzheimer und verwandte Demenzen wichtig ist
Alzheimer und verwandte Demenzen betreffen derzeit weltweit mehrere zehn Millionen Menschen. Gefäßdysfunktion wird zunehmend als entscheidender Faktor für kognitive Beeinträchtigung erkannt. Reduzierte zerebrale Durchblutung, eingeschränkter Abtransport von Stoffwechselabfällen (einschließlich Amyloid-β) und chronische Mikrovaskulusschäden beschleunigen neuronale Fehlfunktionen und Neurodegeneration.
Die Arbeiten der UVM-Gruppe verknüpfen eine plausible molekulare Kette: Verlust von PIP2 → unkontrollierte Piezo1-Aktivität in Gefäßzellen des Gehirns → gestörte zerebrale Durchblutung → mögliche Verschlechterung von Demenzsymptomen. Indem man entweder die PIP2-Spiegel stabilisiert oder die Piezo1-Funktion moduliert, hoffen Forschende, die vaskuläre Regulation wiederherzustellen, die das Hirngewebe mit Sauerstoff und Nährstoffen versorgt.
Aus klinischer Perspektive ist hier wichtig, dass vaskuläre Interventionen komplementär zu amyloid- oder tau-orientierten Strategien wirken könnten. Während amyloide Pathologien direkte neuronale Schädigungen adressieren, zielen vaskuläre Therapien darauf, die Grundversorgung und Abfallbeseitigung zu sichern — beides ist für die Aufrechterhaltung kognitiver Reserve und den langfristigen Schutz vor Demenz entscheidend.
Was kommt als Nächstes: Bindungsstellen, Membranphysik und Wirkstoffentwicklung
Wesentliche Fragen sind noch offen. Das Harraz-Labor plant, genau zu kartieren, wie PIP2 Piezo1 einschränkt: Bindet PIP2 direkt an spezifische Proteindomänen des Kanals, oder verändert es die physikalischen Eigenschaften der Membran, sodass die Kanalpore seltener öffnet? Die Unterscheidung ist entscheidend für die Entwicklung zielgerichteter Therapien, denn direkte Kanalmodulatoren, Membranlipid-Analoga oder Enzym-Inhibitoren würden unterschiedliche pharmazeutische Strategien erfordern.
Mögliche Entwicklungswege schließen ein: (1) kleine Moleküle oder Lipidanaloga, die PIP2 funktionell nachahmen (PIP2-Mimetika), (2) Therapeutika, die lokale PIP2-Synthese fördern, etwa durch Aktivierung der PI4P5-Kinasefamilie, und (3) selektive Piezo1-Hemmer, die für die zerebrale Vasculatur optimiert sind. Jeder Ansatz bringt unterschiedliche Herausforderungen mit sich, insbesondere bezüglich Blut-Hirn-Schranke (BHS), zielgerichteter Verteilung in die Mikrozirkulation und Vermeidung systemischer Nebenwirkungen.
Parallel dazu müssen Forschende untersuchen, warum PIP2 in bestimmten Krankheitszuständen reduziert ist. Ist der PIP2-Verlust Folge von Entzündungsprozessen, verändertem Lipidstoffwechsel, vermehrter Aktivität von Phospholipasen (z. B. Phospholipase C) oder anderen altersbedingten Pathologien? Antworten auf diese Fragen könnten nicht nur therapeutische Hebel liefern, sondern auch Biomarker identifizieren, die das Ansprechen auf Interventionen in klinischen Studien messen lassen.
Langfristig sind auch Lieferlösungen ein kritischer Entwicklungsbereich: Nanopartikel, liposomale Systeme oder ligandengesteuerte Träger könnten notwendig sein, um lipophile Moleküle oder lipidmodulierende Enzyme gezielt in das zerebrale Mikrovaskulaturbett zu bringen, ohne systemische Lipidprofile oder periphere Gefäße zu stören.

Osama Harraz, Ph.D., Assistenzprofessor für Pharmakologie am Larner College of Medicine, betrachtet in seinem Labor an der University of Vermont die Hirngefäße mithilfe eines Weitfeld-Fluoreszenzmikroskops.
Experteneinschätzung
"Die gezielte Beeinflussung von Lipid–Kanal-Interaktionen ist eine aufkommende Grenze in der neurovaskulären Medizin", sagt Dr. Maya Singh, eine Neurowissenschaftlerin, die nicht an der Studie beteiligt war. "Wenn PIP2-Ersatz oder Piezo1-Modulation sicher gemacht und in die richtigen Hirnregionen geliefert werden können, könnten solche Ansätze amyloid- oder tau-orientierte Therapien ergänzen, indem sie die vaskuläre Unterstützung bewahren, die Neuronen benötigen."
Diese Einschätzung verdeutlicht die komplementäre Rolle vaskulärer Interventionen in einem multidisziplinären Therapieansatz gegen Alzheimer und verwandte Demenzen. Die Entdeckung ist ein früher, aber vielversprechender Schritt. Die Translation in humanmedizinische Anwendungen erfordert detaillierte Mechanikstudien, umfassende Sicherheitsprüfungen und ein sorgfältiges Design von Lieferstrategien, um die zerebrale Mikrozirkulation zu erreichen, ohne systemische Nebenwirkungen hervorzurufen.
Zusammenfassend eröffnet diese Forschung eine konkrete molekulare Kontrollstelle für die Blutflussregulation im Gehirn. Die Identifikation von PIP2 als Regulator von Piezo1 bietet nicht nur neue biologische Einblicke in die Grundlagen der Gefäßfunktion, sondern schafft auch eine Plattform für die Entwicklung innovativer Therapeutika gegen vaskuläre Beiträge zu Demenz. Durch die Kombination von biophysikalischer Charakterisierung, präklinischer Modellierung und gezielter Wirkstoffentwicklung kann diese Richtung das Potenzial haben, klinisch relevante Verbesserungen der Hirndurchblutung und damit der kognitiven Gesundheit älterer Patienten zu erzielen.
Wichtige Keywords in diesem Forschungsfeld sind: PIP2, Piezo1, zerebrale Durchblutung, Demenz, Alzheimer, Mikrozirkulation, Membranlipide, Ionenkanal-Modulation und Blut-Hirn-Schranke. Indem Forschende diese Konzepte konsistent benennen und verknüpfen, lässt sich die wissenschaftliche Kommunikation stärken und die Grundlage für translationsnahe Studien verbessern.
Quelle: scitechdaily

Kommentar hinterlassen