11 Minuten
Demenzen werden oft als Erkrankungen des hohen Lebensalters betrachtet, doch zahlreiche Hinweise deuten darauf hin, dass ihre Ursprünge sich über Jahrzehnte zurückverfolgen lassen — bis in die Schwangerschaft und Kindheit. Forschende vertreten zunehmend die Auffassung, dass das günstigste Zeitfenster zur Senkung des lebenslangen Demenzrisikos weit vor dem Rentenalter beginnt, nämlich dort, wo Bildung, Umwelt und Lebensstil das sich entwickelnde Gehirn prägen.
Wurzeln vor den Symptomen: Warum frühe Lebensphasen wichtig sind
Neuere Studien aus Schweden, der Tschechischen Republik und vom Global Brain Health Institute (GBHI) machen eine unbequeme, aber wichtige Erkenntnis deutlich: Risikofaktoren für Demenz beginnen nicht alle erst im Alter. Einige liegen bereits bei der Geburt oder in der frühen Kindheit vor, andere entstehen in der Adoleszenz oder im jungen Erwachsenenalter. Wenn sich neurodegenerative Erkrankungen schließlich klinisch zeigen, sind die dafür verantwortlichen Prozesse häufig schon über Jahrzehnte hinweg wirksam gewesen.
Längsschnittstudien, die kognitive Leistungen von der Kindheit bis ins hohe Alter verfolgen, liefern einen der klarsten Hinweise. Personen, die im Alter von etwa 11 Jahren in kognitiven Tests relativ niedrig bewertet werden, bleiben oft auch mit 70 Jahren im Vergleich zu ihren Altersgenossen tendenziell niedriger — ein Muster, das eher auf persistierende frühe Unterschiede als auf eine ausschließlich steilere altersbedingte Abnahme hindeutet. Auch bildgebende Verfahren unterstützen dieses Bild: Bestimmte strukturelle Veränderungen, die bei älteren Menschen mit Demenz in Zusammenhang gebracht werden, korrelieren mit frühen Lebensumständen und Expositionen.
Diese Befunde legen nahe, dass die Entwicklung des Gehirns in pränatalen und frühkindlichen Phasen sowie in der Jugend prägende Weichenstellungen für die spätere kognitive Gesundheit setzt. Faktoren wie frühe Unterernährung, toxische Umweltbelastungen, fehlende kognitive Anregung oder eingeschränkter Zugang zu Qualitätsbildung können langfristig die neuronale Architektur und die Widerstandskraft des Gehirns beeinträchtigen — Begriffe, die in der Forschung häufig unter dem Schlagwort kognitive Reserve zusammengefasst werden. Daraus folgt: Vorbeugungsmaßnahmen, die nur auf ältere Populationen fokussieren, greifen zu kurz, wenn der Ursprung eines Teils des Risikos viel früher liegt.
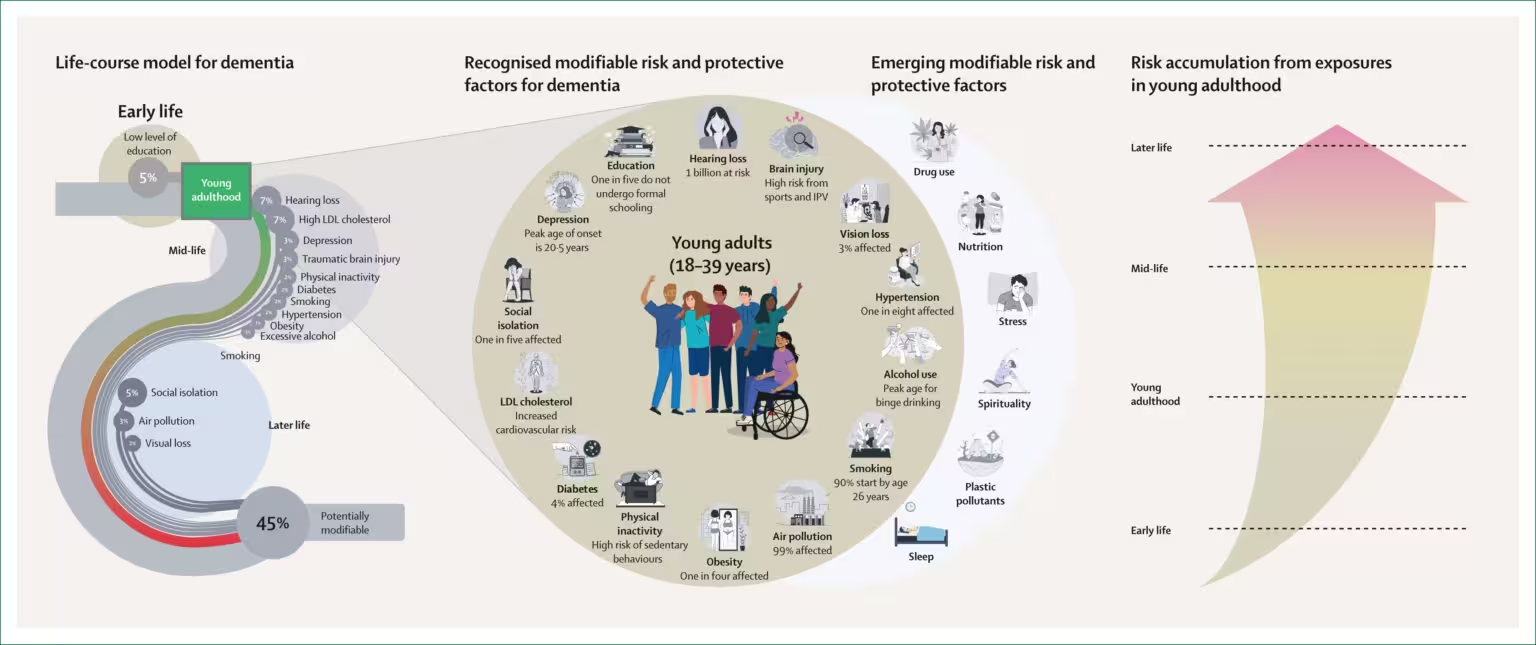
Welche frühen Risikofaktoren die Evidenz identifiziert
Forschende haben eine Mischung aus nicht veränderbaren und modifizierbaren Risiken in frühen Lebensphasen katalogisiert. Geburtsbezogene Faktoren, die eine multinational angelegte Untersuchung von 2023 identifizierte — etwa Mehrlingsgeburten, der Altersabstand zu Geschwistern oder das elterliche Alter zum Zeitpunkt der Zeugung — sind größtenteils nicht beeinflussbar, liefern Epidemiologinnen und Epidemiologen jedoch wichtige Hinweise auf Vulnerabilitätsmuster innerhalb der Bevölkerung.
Handlungsfähige Faktoren treten über die gesamte Entwicklung hinweg bis ins junge Erwachsenenalter auf. Ein GBHI-geführter Konsens aus dem Jahr 2024 fasst Lebensstil-, Umwelt- und klinische Einflussgrößen zusammen, die das langfristige Demenzrisiko erhöhen können:
- Lebensstil: starker Alkoholkonsum, Tabakrauchen, geringe körperliche Aktivität und soziale Isolation — Verhaltensweisen, die sich oft schon in der Jugend etablieren und kumulative Wirkung entfalten.
- Umweltfaktoren: Luft- und Feinstaubbelastung, wiederholte Kopfverletzungen (einschließlich Gehirnerschütterungen) sowie Sinnesverluste wie Hör- oder Sehbeeinträchtigungen, die soziale Teilhabe erschweren können.
- Gesundheitszustände: Übergewicht und Adipositas, Typ-2-Diabetes, arterieller Bluthochdruck, erhöhter LDL-Cholesterin-Spiegel und Depressionen — viele dieser Bedingungen entstehen durch oder werden verstärkt durch früh etablierte Lebensgewohnheiten.
- Bildungs- und soziale Determinanten: geringe formale Schulbildung und fehlende frühkindliche kognitive Förderung, die mit dem Konzept der kognitiven Reserve zusammenhängen (die Fähigkeit des Gehirns, krankheitsbedingte Schäden funktional zu kompensieren).
Einige dieser Pfade wirken direkt: wiederholte traumatische Hirnverletzungen können bleibende strukturelle Schäden hinterlassen, die das Demenzrisiko erhöhen. Andere Verknüpfungen sind indirekt: Hörverlust zum Beispiel kann durch eingeschränkte Kommunikation soziale Isolation fördern und dadurch die kognitive Beanspruchung steigern, was wiederum den Abbau beschleunigen kann. Ebenso können früh etablierte schlechte Ernährungsgewohnheiten oder Bewegungsmangel über Jahre Stoffwechsel- und Gefäßschäden aufbauen, die später neurodegenerative Prozesse begünstigen.
Darüber hinaus zeigen Genetik und Umwelt oft Wechselwirkungen: Träger bestimmter genetischer Risikofaktoren — etwa Varianten im APOE-Gen — können besonders empfindlich auf Umwelteinflüsse reagieren. Das bedeutet nicht Determinismus, sondern eröffnet interaktive Präventionsansätze, in denen sowohl genetische Risikoerkennung als auch Lebensstilmodifikation eine Rolle spielen.
Warum das junge Erwachsenenalter ein entscheidendes Interventionsfenster ist
Die Neurowissenschaftlerin Francesca Farina, die mit GBHI kooperiert, betont, dass die Altersgruppe von etwa 18 bis 39 Jahren eine Schlüsselphase für Präventionsstrategien darstellt. In dieser Lebensphase werden viele Verhaltensmuster und Expositionen gefestigt — Rauchgewohnheiten, Trinkmuster, Berufs- und Bildungsentscheidungen — und öffentliche Gesundheitsmaßnahmen können hier noch wirksamen Einfluss auf die mittlere und späte Gehirngesundheit nehmen.
Frühes Eingreifen hat zwei zentrale Gründe: Erstens reduziert das Verhindern oder Verzögern des Auftretens von Risikofaktoren (etwa durch Blutdruckkontrolle oder Prävention von Adipositas) die kumulative physiologische Schädigung über Jahrzehnte hinweg. Zweitens führt die Stärkung schützender Faktoren wie Bildung, regelmäßiger körperlicher Aktivität und sozialer Vernetzung zum Aufbau kognitiver Reserve, die es dem Gehirn erlaubt, spätere Pathologien besser zu tolerieren, bevor klinische Symptome auftreten.
Praktisch betrachtet bietet das junge Erwachsenenalter auch strukturelle Chancen: Zugang zu betrieblicher Gesundheitsförderung, universitären Programmen, digitalen Gesundheitsangeboten und Gemeinschaftsinitiativen, die Gesundheitsverhalten gezielt formen können. Kampagnen, die auf diese Lebensphase zugeschnitten sind — zum Beispiel zu verantwortungsvollem Alkoholkonsum, Rauchstopp, Bewegung und psychischer Gesundheit — erreichen Menschen noch bevor schädliche Patterns verfestigt sind.
Zudem ist die ökonomische Argumentation überzeugend: Präventive Maßnahmen, die früh ansetzen, amortisieren sich oft durch vermiedene Behandlungskosten, geringeren Pflegebedarf und höhere Lebensqualität in späteren Lebensjahren. Kosten-Nutzen-Analysen aus der öffentlichen Gesundheitsforschung zeigen, dass Interventionen mit Fokus auf Prävention und Frühintervention langfristig wirtschaftlich vorteilhaft sein können.
Praktische Maßnahmen der öffentlichen Gesundheit auf verschiedenen Ebenen
Die Reduktion des lebenslangen Demenzrisikos erfordert koordinierte Maßnahmen auf individueller, kommunaler und nationaler Ebene. Auf individueller Ebene spielt Bewusstsein eine große Rolle: Aufklärungskampagnen und Lehrpläne in Schulen, die gehirngesunde Verhaltensweisen vermitteln, können junge Menschen dazu motivieren, protektive Lebensstile anzunehmen. Steuerliche Maßnahmen oder Regulierungen gegenüber schädlichen Substanzen wie Alkohol und Tabak sind bewährte Instrumente zur Verbrauchsreduktion und lassen sich als Investitionen in die kollektive Gehirngesundheit darstellen.
Auf Gemeindeebene können jugendliche Beiräte geschaffen werden, damit lokale Politiken die Perspektiven jüngerer Erwachsener widerspiegeln. Solche Beiräte können als Vermittler zwischen öffentlichen Gesundheitsdiensten und der jungen Bevölkerung fungieren, um maßgeschneiderte Interventionen zu entwickeln — von sicheren Sportprogrammen zur Senkung des Kopfverletzungsrisikos bis hin zu leicht zugänglichen Hör- und Sehtests.
Auf nationaler Ebene empfehlen Expertinnen und Experten die Verpflichtung zu einem formalen Brain-Health-Charter oder einem langfristigen Plan, der messbare Ziele zur Demenzprävention festlegt, Bildungs- und Gesundheitssysteme integriert und Forschung zu aufkommenden Bedrohungen finanziert. Wichtige Themen, die in solchen Strategien berücksichtigt werden sollten, sind etwa ultra-verarbeitete Lebensmittel, chronischer Stress, exzessive Bildschirmnutzung, Drogenkonsum und Umweltbelastungen wie Mikroplastik und Luftverschmutzung.
Konkrete Programme können Folgendes umfassen: flächendeckende Präventionsprogramme für Adipositas und Diabetes in Schulen; arbeitsschutzorientierte Maßnahmen zur Vermeidung von Kopfverletzungen in Freizeitsportarten; Ausbau von Angeboten zur psychischen Gesundheitsvorsorge für junge Erwachsene; sowie Umweltschutzmaßnahmen, die Luftqualität und Lebensraumqualität verbessern. Wichtig ist, dass solche Programme evaluiert und skaliert werden können — durch randomisierte Communities-Interventionen oder gut designte Beobachtungsstudien, die Wirksamkeit und Kostenwirkung nachweisen.
Wissenschaftlicher Kontext: Mechanismen und offene Fragen
Die biologischen Mechanismen, die frühe Expositionen mit Demenz im höheren Alter verknüpfen, sind vielschichtig. Chronische Entzündungsprozesse, vaskuläre Schäden, metabolische Dysregulation und die Akkumulation fehlgefalteter Proteine (wie Amyloid-β und Tau bei der Alzheimer-Krankheit) sind alle in neurodegenerative Prozesse involviert. Frühe Lebensbedingungen können diese Mechanismen indirekt beeinflussen, indem sie die lebenslange Gesundheitspfad beeinflussen — etwa durch Förderung von Bluthochdruck oder metabolischem Syndrom im mittleren Lebensalter — oder direkt durch Modifikation der neuronalen Entwicklung in der pränatalen und frühen postnatalen Phase.
Dabei ist zu beachten, dass mehrere Mechanismen gleichzeitig wirken können: Gefäßschäden etwa reduzieren die zerebrale Perfusion, was neuronale Vulnerabilität erhöht; metabolische Störungen können oxidativen Stress und Entzündung fördern; und wiederholte Kopftraumen können neuroinflammatorische Reaktionen auslösen und Proteinaggregation begünstigen. Diese multiplen Pfade machen klar, warum ein multipräventiver Ansatz sinnvoll ist, der sowohl kardiometabolische Gesundheit als auch Lebensstil- und Umweltfaktoren anspricht.
Ein weiteres zentrales Konzept ist die kognitive Reserve: Menschen mit höherer Bildung oder mit lebenslanger geistiger Aktivität zeigen oft später klinische Symptome trotz vergleichbarer neuropathologischer Veränderungen. Das legt nahe, dass Investitionen in frühkindliche Bildung, schulische Qualität und lebenslanges Lernen Populationseffekte haben können, indem sie die Schwere oder den Zeitpunkt des Auftretens klinischer Symptome verschieben.
Viele Fragen bleiben wissenschaftlich offen und sind Gegenstand aktueller Forschung: Wie stark interagieren genetische Risikofaktoren mit bestimmten Umwelt- oder Lebensstilfaktoren? Welche kritischen Zeitfenster sind am sensitivsten gegenüber bestimmten Expositionen? Welche präventiven Maßnahmen sind kosteneffektiv und wie lassen sie sich in unterschiedliche Gesundheitssysteme integrieren? Antworten erfordern gut designte Langzeitkohorten, die detaillierte frühe Lebensdaten, moderne Bildgebung, Biomarker und klinische Endpunkte verknüpfen.
Expertinnen- und Experteneinschätzung
„Die Erweiterung des Fokus bei der Demenzprävention um Kindheit und junges Erwachsenenalter ist keine akademische Spitzfindigkeit — es ist eine gesundheitspolitische Notwendigkeit“, sagt Dr. Emily Carter, Neurologin und Gesundheitsforscherin. „Einfache Maßnahmen — die Verbesserung der Schulernährung, die Reduktion der Luftverschmutzung, der Ausbau der primärmedizinischen Versorgung und psychischer Gesundheitsangebote — summieren sich über Jahrzehnte. Wenn Gesundheitssysteme und Gemeinschaften früh investieren, zahlt sich das durch eine geringere Krankheitslast und eine höhere Lebensqualität im Alter aus.“
Dr. Carter weist darauf hin, dass pragmatische Forschungsprioritäten Langzeitkohorten umfassen sollten, die detaillierte frühe Lebensexpositionen mit Bildgebung des Gehirns und klinischen Ergebnissen verknüpfen, sowie randomisierte kommunale Interventionen, die skalierbare Präventionsmodelle testen. Zusätzlich fordert sie bessere Dateninfrastrukturen, um sozial-ökologische Determinanten und Umweltbelastungen systematisch zu erfassen.
Folgen für Einzelpersonen und Entscheidungsträger
Für Einzelpersonen ist die Botschaft ermächtigend: Entscheidungen, die in Jugend und jungem Erwachsenenalter getroffen werden, haben Bedeutung. Das Aufgeben des Rauchens, ein moderater Umgang mit Alkohol, regelmäßige körperliche Aktivität, der Schutz von Hör- und Sehvermögen, die Weiterverfolgung formaler Bildung und die Pflege sozialer Kontakte sind praktische Schritte, die die Resilienz gegen kognitiven Abbau stärken können. Auch Maßnahmen zur Stressreduktion — wie Schlafhygiene, psychologische Unterstützungsangebote und ausgewogene Lebensführung — tragen zu einer langfristig günstigeren Gehirngesundheit bei.
Für politische Entscheidungsträgerinnen und -träger sprechen die Befunde klar für einen Lebenslaufansatz (life-course approach) in der Gehirngesundheit: Demenzprävention sollte in die Schwangerenvorsorge, frühkindliche Programme, Bildungspolitik, Umweltschutzmaßnahmen und die Primärversorgung integriert werden. Investitionen, die Luftverschmutzung reduzieren, die Ernährungsqualität verbessern, traumatische Hirnverletzungen verhindern und psychische Gesundheitsdienste sicherstellen, sind nicht nur kurzfristig gesundheitsfördernd, sondern können über Jahrzehnte hinweg die Inzidenz neurodegenerativer Erkrankungen mindern.
Dies erfordert vernetzte Politiken: Bildungsreformen, städtische Planung mit Fokus auf saubere Luft und sichere Freizeitangebote, Arbeitsmarktprogramme zur Förderung gesunder Arbeitsbedingungen und Finanzierungslinien in Gesundheitssystemen, die präventive Betreuung in jungen Jahren priorisieren. Solche Integrationsstrategien erhöhen die Wahrscheinlichkeit, dass Präventionsmaßnahmen nachhaltig sind und breite Bevölkerungsschichten erreichen.
Abschließende Perspektive
Die Sichtweise, Demenzprävention als lebenslange Aufgabe zu begreifen, verändert sowohl Forschung als auch Politik. Anstatt erst im hohen Alter zu reagieren, kann die öffentliche Gesundheit das zukünftige Demenzrisiko senken, indem sie Gehirngesundheit vom Mutterleib an bis ins junge Erwachsenenalter fördert und schützt. Dieser Paradigmenwechsel — weg von späten Interventionen hin zu einer Prävention über den gesamten Lebenslauf — kann entscheidend sein, wenn es darum geht, die Kurve der Demenzinzidenz weltweit abzuflachen.
Konkrete nächste Schritte sind die Stärkung von Forschungsnetzwerken für Langzeitdaten, die Implementierung und Evaluation zielgruppenspezifischer Präventionsprogramme für Kinder, Jugendliche und junge Erwachsene, sowie die politische Umsetzung umfassender Strategien zur Verbesserung von Bildung, Umwelt und Lebensstilfaktoren. Nur durch koordiniertes Handeln über Sektoren hinweg lässt sich das volle Potenzial einer lebenslauforientierten Demenzprävention realisieren.
Quelle: sciencealert


Kommentar hinterlassen