8 Minuten
Denken Sie an Makrophagen als das Reinigungsteam des Körpers: Sie räumen Zelltrümmer weg, recyceln lebenswichtige Elemente und stimmen die Funktion von Organen stillschweigend ab. Aber wer bildet dieses Team aus? Jüngste Arbeiten deuten auf einen einzelnen genetischen Regulator hin, der diesen Zellen das Regelwerk übergibt.
Forscher haben entdeckt, dass ein genetischer Faktor namens MafB als Schalter fungiert, der Makrophagen ihre Identität und ihre Fähigkeit zum Organschutz verleiht. Ohne ihn können sich diese essenziellen Immunzellen nicht vollständig ausreifen – was Prozesse vom Eisenrecycling bis zur Gesundheit von Lunge und Niere stört. Diese Einsicht verbindet Zellbiologie, Genregulation und Organhomöostase in einem gemeinsamen mechanistischen Rahmen.
Vom Monozyten zum reifen Makrophagen: der MafB-Drehpunkt
Unter dem Mikroskop wirkt die Reifung fast wie Choreografie. Im Blut zirkulierende Monozyten wandern in Gewebe ein und übernehmen, abhängig von lokalen Signalen, spezialisierte Aufgaben. MafB, ein Transkriptionsfaktor, steigt während dieses Übergangs kontinuierlich an. Er handelt nicht isoliert, sondern koordiniert ein breit angelegtes genetisches Programm, das Gene für Phagozytose, Abfallbeseitigung und Gewebeerhaltung hochfährt. Wird MafB entfernt, bleiben viele dieser Schalter aus – die Zellen verharren in einem Zwischenzustand: vorhanden, aber nicht voll ausgestattet.
Dieser Zwischenzustand hat Konsequenzen für Funktion und Morphologie. In Experimenten, die vom Institut für Immunphysiologie der Universität Lüttich geleitet wurden, erschienen Zellen ohne MafB morphologisch unreifer – runder, weniger verzweigt und funktionell eingeschränkt. Solche Unterschiede sind nicht nur optisch; sie korrelieren mit messbaren Abweichungen in Clearance-Funktionen, Signalgebung und Regenerationskapazität.
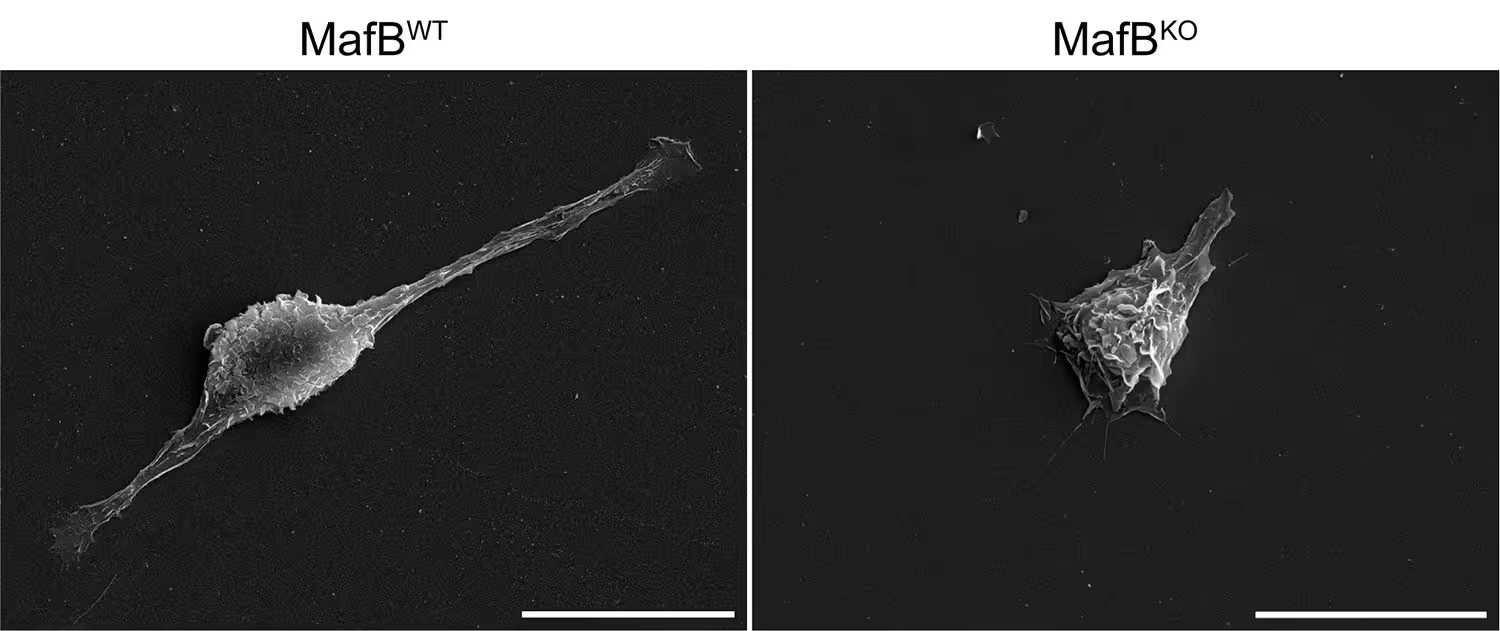
Makrophagen mit MafB (WT) wirken reif und gut geformt, während diejenigen ohne MafB (KO) rund und weniger entwickelt erscheinen.
Warum ist das wichtig? Makrophagen erfüllen weit mehr Aufgaben als nur die Bekämpfung von Infektionen. Sie transportieren Eisen aus gealterten Erythrozyten, remodeln die extrazelluläre Matrix und senden metabolische Signale, die Lunge, Nieren, Darm und Milz im Gleichgewicht halten. Ein globaler Regulator wie MafB liefert eine konservierte Identität, die es Makrophagen ermöglicht, sich lokal anzupassen und gleichzeitig Kernfunktionen in verschiedenen Geweben und Spezies zu bewahren.
Evolutionäre Konservierung und systemische Effekte
Je tiefer man in die DNA blickt, desto klarer wird das Muster: MafB lenkt ein Netzwerk von Genen, das sowohl in Mäusen als auch in Menschen vorhanden ist und sich bei Wirbeltieren widerspiegelt. Diese evolutionäre Bewahrung deutet auf ein biologisches Prinzip hin: Der Organismus nutzt ein gemeinsames genetisches Programm, um verlässliche zelluläre Akteure dort bereitzustellen, wo sie benötigt werden.
Versagt dieses Programm, zeigen sich die Folgen auf Organebene. Das Team aus Lüttich dokumentierte gestörtes Eisenrecycling in der Milz sowie subtile, aber messbare Dysfunktionen in Lunge, Darm und Niere, wenn die Makrophagenreifung stockte. Diese organ-spezifischen Veränderungen unterstreichen einen wichtigen Punkt: Die Identität von Immunzellen formt die Physiologie des Körpers und reicht weit über die bloße Abwehr von Pathogenen hinaus.
Daneben hat diese Forschung auch klinische Relevanz. Chronische Erkrankungen wie Fibrose, persistierende Entzündungen, metabolische Störungen und bestimmte Infektionen weisen Makrophagendysfunktionen als zentralen Mechanismus auf. Wenn MafB oder seine wichtigen downstream-Wegstrecken gezielt moduliert werden könnten, hätten Forscher die Möglichkeit, die Kompetenz von Makrophagen wiederherzustellen und so die Gewebereparatur sowie die Homöostase zu verbessern. Das ist ein langer Weg, aber einer mit klaren molekularen Wegweisern.
Methoden, Evidenz und technische Details
Die Ergebnisse fußen auf einer Kombination aus genetischen Modellen, Einzelzell-Profiling, Transkriptom-Analysen und vergleichender Genomik. Das Tracking von MafB-Expression während der Differenzierung von Monozyten zu geweberesidenten Makrophagen offenbarte ein reproduzierbares Muster: Ein Anstieg von MafB korrelierte konsistent mit der Aktivierung von Genen für Phagozytose, Lysosom-Funktion und anderen funktionalen Markern. Solche Korrelationen wurden durch funktionelle Assays untermauert – zum Beispiel Messungen der Phagozytose, der Zytokinproduktion und der Fähigkeit zur Matrixremodelierung.
Loss-of-function-Studien lieferten die aussagekräftigsten Daten: Tiere mit gezielter Deletion von MafB in myeloiden Linien zeigten Makrophagen, die zahlreiche ihrer essentiellen Aufgaben nicht erfüllten. Dies manifestierte sich nicht nur auf zellulärer Ebene, sondern durch messbare Änderungen in der Organphysiologie, etwa vermindertes Eisenrecycling in der Milz, veränderte Inflammationsmarker in der Lunge und erhöhte Anfälligkeit für Gewebeschäden nach Stress.
Die eingesetzten Methoden umfassen moderne Einzelzell-RNA-Sequenzierung (scRNA-seq) zur Identifikation von Subpopulationen, ATAC-seq zur Kartierung zugänglicher Chromatinregionen, ChIP-seq zur Bestätigung direkter MafB-Bindungsstellen sowie proteomische Ansätze zur Bestimmung funktioneller Effektorproteine. Ergänzend kamen in-vivo-Modelle, Gewebefärbungen und Elektronenmikroskopie zum Einsatz, um Morphologie und ultrastrukturelle Veränderungen zu dokumentieren.
Diese Veränderungen sind keineswegs abstrakt: Defekte im Eisenrecycling können die systemische Eisenhomöostase stören und zur Anämie bei chronischen Erkrankungen beitragen. Störungen in Lunge und Niere können Gewebe empfindlicher für weitere Schäden machen und die Regenerationskapazität herabsetzen. Kurz gesagt, die Rolle von MafB spannt eine Brücke zwischen molekularer Zellbiologie und der Gesundheit des gesamten Organismus.
Implikationen für Therapie und zukünftige Forschung
Die Zielrichtung eines Masterregulators birgt Chancen, aber auch Risiken. Transkriptionsfaktoren wie MafB sitzen im Zentrum zahlreicher genetischer Programme; ihr gezieltes Verändern könnte weitreichende, unvorhergesehene Effekte haben. Deshalb erscheint ein pragmatischerer kurzfristiger Ansatz sinnvoll: die Beeinflussung von downstream-Effektoren – also jener Gene und Signalwege, die MafB kontrolliert und die pharmakologisch ansprechbar sind oder gewebespezifisch moduliert werden können.
Weitere realistische Strategien umfassen zellbasierte Therapien: ex vivo programmierte Makrophagen, die in einen ausgereiften MafB-hohen Zustand gebracht werden, könnten re‐implantiert werden, um geschädigte Stellen zu unterstützen. Solche Ansätze kombinieren Zelltherapie, Gentherapie und präzise Immunmodulation und würden es erlauben, Effektivität und Sicherheit gewebespezifisch zu optimieren.
Die nächste Forschungswelle muss mehrere offene Fragen klären: Wie interagieren lokale Gewebesignale – etwa Zytokine, metabolische Verhältnisse oder mechanische Reize – mit MafB, um die bemerkenswerte Diversität von Makrophagenphänotypen zu erzeugen? Reicht eine partielle Wiederherstellung von MafB-getriebenen Programmen aus, um Organfunktionen in Krankheitsmodellen zu retten, oder sind vollständige Programme erforderlich? Und in welchem Maße untergraben Umwelt‑ oder Stoffwechselstressoren dieses Programm und beschleunigen so chronische Erkrankungen?
Außerdem sind Sicherheitsaspekte kritisch: Welche Off-Target-Effekte können bei einer systemischen Modulation auftreten? Welche Kompensationsmechanismen existieren innerhalb des myeloiden Differenzierungsnetzwerks, und wie robust sind diese gegen therapeutische Eingriffe? Das Mapping solcher Netzwerke ist nicht nur wissenschaftliche Neugier: Es ist Voraussetzung für translational erfolgreiche Interventionen.
Experteneinschätzung
Dr. Eleanor Voss, Immunologin und translationale Forscherin, bemerkt: "MafB stellt einen Drehpunkt zwischen Identität und Funktion dar. Wir wissen seit langem, dass Makrophagen sich an lokale Nischen anpassen; jetzt sehen wir ein konserviertes genetisches Rückgrat, das diese Anpassung zuverlässig macht. Therapeutisch besteht die Herausforderung darin, dieses Rückgrat zu respektieren und gleichzeitig gezielt seine Outputs zu modulieren. Das ist Präzisionsbiologie in Aktion."
Das Verständnis, wie ein einziger Transkriptionsfaktor so weitreichende zelluläre Verantwortlichkeiten koordinieren kann, verändert unser Bild von Immunzellen. Makrophagen sind keine improvisierten Verteidiger; sie sind programmierte Betreuer mit spezifischen Rollen in Geweben. Die wissenschaftliche Aufgabe besteht nun darin, diese Programmierung in therapeutische Ansätze zu überführen, die Funktion bewahren, die Regeneration fördern und dabei das komplexe Netzwerk intakt lassen, das die Evolution über Millionen von Jahren geformt hat.
Zusammengefasst eröffnet die Identifikation von MafB als Masterregulator neue Perspektiven für die Forschung an Immunzellidentität, Gewebehomöostase und therapeutischer Modulation. Durch die Kombination moderner Genomik, funktioneller Assays und translationaler Strategien können Wissenschaftler mögliche Hebel identifizieren, die Makrophagenkompetenz gezielt wiederherstellen und so die Behandlung chronischer Krankheiten verbessern.
Wichtige SEO‑Schlüsselwörter, die in diesem Kontext von Relevanz sind: MafB, Makrophagen, Transkriptionsfaktor, Immunologie, Eisenrecycling, Gewebehomöostase, Einzelzell‑Sequenzierung, Zellreifung, Zelltherapie, Entzündung und Fibrose. Diese Begriffe spiegeln zentrale Konzepte wider und sollten in weiterführenden wissenschaftlichen Beiträgen und klinischen Übersichten konsistent verwendet werden, um Fach- und Laienpublikum gleichermaßen gut zu informieren.
Quelle: scitechdaily

Kommentar hinterlassen