7 Minuten
Neue Forschung an Mäusen hat Nasengewebe-Schäden und ein verbreitetes Atemwegsbakterium mit Gehirnveränderungen in Verbindung gebracht, die Alzheimer-ähnlich erscheinen — ein Befund, der Fragen dazu aufwirft, wie Infektionen das Demenzrisiko beeinflussen könnten.
What the mouse study found
Ein Forscherteam unter Leitung der Griffith University untersuchte, wie das Bakterium Chlamydia pneumoniae, das beim Menschen Pneumonien verursachen kann, aus der Nasenhöhle ins Gehirn gelangen könnte. In ihren Experimenten aus dem Jahr 2022 bewegte sich das Bakterium entlang des Riechnervs — des neuronalen Weges, der die Nase mit dem Gehirn verbindet — und etablierte innerhalb von 24 bis 72 Stunden eine Infektion im Zentralnervensystem.
Besonders auffällig war die Beobachtung, dass Infektionen in den Riechbahn-Nerven zunahmen, wenn das Nasenepithel (die dünne Schleimhaut, die das Dach der Nasenhöhle auskleidet) beschädigt war — etwa durch mechanische Reize, die dem Nasenbohren oder dem Auszupfen von Nasenhaaren ähneln. Diese verstärkten Infektionen korrelierten mit einer erhöhten Ablagerung des Amyloid-β-Proteins im Gehirn der Mäuse. Amyloid-β ist ein Peptid, das als Reaktion auf Infektion und Entzündung freigesetzt werden kann; seine Anhäufung in Form von Plaques gilt als charakteristisches Merkmal der Alzheimer-Krankheit.
Es ist wichtig zu betonen, dass diese Experimente an Mäusen durchgeführt wurden, nicht am Menschen. Dennoch betonte das Forschungsteam die Verbindung zwischen Nasenschädigung, mikrobieller Invasion und neuropathologischen Auswirkungen als einen vielversprechenden Untersuchungsstrang, der weiterer Studien bedarf.
How bacteria could reach the brain
Biologisch stellt die Nase eine direkte — und vergleichsweise wenig geschützte — Route zum Zentralnervensystem dar. Die Fasern des Riechnervs durchdringen die Siebplatte (lat. lamina cribrosa) des Schädels und bilden damit eine Abkürzung, die einige Krankheitserreger ausnutzen können. Die Studie zeigte, dass C. pneumoniae in der Lage ist, diesen Weg aufzusteigen, insbesondere wenn die schützende epithelialle Barriere kompromittiert ist.
Infiziertes Nervengewebe reagierte mit einer vermehrten Produktion von Amyloid-β, ein Effekt, den die Forschenden als Teil einer immunähnlichen Reaktion beschreiben. Ob diese Proteinablagerungen eine reversible Abwehrreaktion darstellen oder den Beginn einer fortschreitenden neurodegenerativen Entwicklung markieren, bleibt weiterhin offen. Mechanistisch könnte Amyloid-β als antimikrobielles Peptid wirken, das Krankheitserreger einkapselt, zugleich aber bei persistierender Produktion toxische Folgen für neuronale Funktionen haben.
"Wir sind die ersten, die zeigen, dass Chlamydia pneumoniae direkt über die Nase ins Gehirn gelangen kann und dort Pathologien auslösen kann, die der Alzheimer-Krankheit ähneln", erklärte der Neurowissenschaftler James St John von der Griffith University bei Veröffentlichung der Studie. "Wir haben das in einem Mausmodell beobachtet, und die Ergebnisse sind potenziell beunruhigend auch im Kontext des Menschen." Diese Formulierung unterstreicht die Notwendigkeit, tierexperimentelle Befunde vorsichtig zu interpretieren und im nächsten Schritt translative Studien am Menschen durchzuführen.
Scientific context and caveats
Forscher haben C. pneumoniae in zahlreichen Gehirnen von Menschen mit spät einsetzender Demenz nachgewiesen, doch der konkrete Weg und der Zeitpunkt dieses Vorkommens sind nicht eindeutig geklärt. Ein wichtiger Vorbehalt lautet: Das gleichzeitige Auftreten von Amyloid-β-Plaques und Infektion beweist nicht, dass die Plaques die Alzheimer-Erkrankung verursachen. Alzheimer ist eine komplexe Erkrankung, die vermutlich altersbedingte Vulnerabilität, genetische Prädispositionen (z. B. APOE-Allele), sowie Umweltfaktoren einschließlich Infektionen vereint.
Eine Übersichtsarbeit aus dem Jahr 2024 erweiterte die Hypothese, dass nasale Infektionen und mechanische Schädigungen der Nase das Demenzrisiko erhöhen könnten und stärkte damit die Begründung für humanmedizinische Untersuchungen. Das Griffith-Team rief zu Folgeuntersuchungen am Menschen auf, um zu klären, ob derselbe olfaktorische Weg beim Menschen aktiv ist und ob alltägliche Verhaltensweisen, die die Nasenschleimhaut schädigen, das Langzeitrisiko verändern.
"Wir müssen diese Studie beim Menschen durchführen und bestätigen, ob derselbe Pfad in gleicher Weise funktioniert", fügte St John hinzu. "Diese Forschung wurde bereits von vielen vorgeschlagen, aber noch nicht abgeschlossen. Sicher ist: Dieselben Bakterien kommen auch beim Menschen vor, aber wir haben noch nicht herausgefunden, wie genau sie dorthin gelangen." Diese Aussage reflektiert die aktuelle Lücke zwischen Beobachtungen in Tiermodellen und validen Daten beim Menschen.
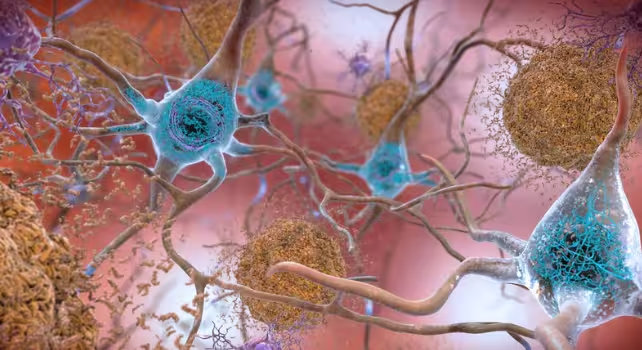
Illustration of amyloid-beta protein plaques, in orange
Practical implications: hygiene, habits and risk
Nasenbohren ist weit verbreitet — einige Umfragen legen nahe, dass die meisten Menschen es gelegentlich tun — und das Auszupfen von Nasenhaaren ist ein weiteres Verhalten, das mukosales Gewebe schädigen kann. Die Forschenden raten zu Vorsicht: Eine Schädigung der Nasenschleimhaut könnte plausibel die Wahrscheinlichkeit erhöhen, dass Bakterien zum Riechnerv aufsteigen.
"Wir möchten die Innenseite unserer Nase nicht verletzen — Nasenbohren und Auszupfen können genau das bewirken", warnte St John. "Wenn Sie die Schleimhaut der Nase beschädigen, können Sie erhöhen, wie viele Bakterien in Ihr Gehirn gelangen können." Ob mäßiges, gelegentliches Nasenbohren beim Menschen das Demenzrisiko substantiell beeinflusst, ist unbekannt; die Mausstudie macht jedoch einen Mechanismus sichtbar, der klinisch überprüfbar ist. In praktischer Hinsicht lassen sich daraus einige einfache Empfehlungen ableiten: Nasenschleimhaut nicht mechanisch reizen, bei chronischen Nasenbeschwerden ärztliche Abklärung und Behandlung suchen, und auf Nasenhygiene achten, um das Risiko persistierender Infektionen zu minimieren.

Nose picking: not just a habit for small children
Expert Insight
Dr. Amina Ross, eine Neuroimmunologin (fiktional, zur Kontextualisierung zitiert), kommentierte: "Diese Studie stärkt die Vorstellung, dass periphere Infektionen zentrale Effekte haben können. Die olfaktorische Route ist einzigartig verletzlich. Für präventive Maßnahmen im Bereich der öffentlichen Gesundheit könnten die Minimierung nasaler Traumata und die Behandlung chronischer Nasennebenhöhlen- oder Schleimhautinfektionen kostengünstige Strategien sein, die es sich zu prüfen lohnt, während wir auf humanbezogene Daten warten."
Ihre Einschätzung unterstreicht einen breiteren Forschungstrend: Es wird zunehmend untersucht, wie Mikroorganismen, Entzündungsreaktionen und immunologische Prozesse außerhalb des Gehirns neurodegenerative Prozesse im Inneren beeinflussen können. Biologisch relevante Konzepte sind dabei systemische Entzündung, Mikroglia-Aktivierung, BBB (Blut-Hirn-Schranke)-Integrität und die Fähigkeit von antimikrobiellen Peptiden wie Amyloid-β, auf Infektionen zu reagieren.
What comes next for research
Prioritäre nächste Schritte umfassen sorgfältig geplante Humanstudien, um das Vorhandensein von Mikroorganismen in Nase und Gehirn altersübergreifend zu kartieren und um zu testen, ob nasale Verletzungen mit Markern der Neurodegeneration über längere Zeiträume korrelieren. Wichtige methodische Anforderungen sind dabei longitudinale Kohorten, postmortale Gewebsuntersuchungen mit molekularen Detektionsmethoden (z. B. PCR, In-situ-Hybridisierung) sowie multimodale Bildgebung (z. B. Amyloid-PET), um Kausalrichtungen besser zu klären.
Forscher möchten außerdem wissen, ob der Anstieg von Amyloid-β eine vorübergehende immunologische Reaktion ist, die sich nach Abklingen der Infektion zurückbildet, oder ob er langfristig Plaquebildung anstößt und damit einen chronischen neurodegenerativen Prozess in Gang setzt. Tierexperimentelle Daten bieten Hinweise auf beide Möglichkeiten: In einigen Modellen normalisieren sich entzündliche Marker nach Clearance des Erregers, in anderen bleiben Veränderungen persistierend und führen zu strukturellen Schäden.
Verwandte präklinische Arbeiten haben weitere Interventionen identifiziert, die die Amyloid-Pathologie in Tiermodellen modulieren können — etwa antiinfektiöse Therapien, entzündungshemmende Strategien oder immunmodulatorische Eingriffe — doch die Übertragung dieser Ergebnisse auf die Prävention oder Behandlung der Alzheimer-Krankheit beim Menschen bleibt herausfordernd. Jede gut dokumentierte biologische Route — einschließlich der möglichen Verbindung zwischen nasaler Schädigung und bakterieller Invasion — reduziert jedoch die Zahl plausibler Mechanismen und hilft, gezieltere Hypothesen für klinische Studien zu formulieren.
Bis valide Humanstudien vorliegen, ist die konservative Schlussfolgerung pragmatisch: Vermeiden Sie Verletzungen der Nasenschleimhaut, behandeln Sie chronische nasale Infektionen zeitnah und unterstützen Sie Forschung zu infektiösen Risikofaktoren für Demenz. Das bessere Verständnis, wie Umweltfaktoren wie Bakterien und Viren mit Alterungsprozessen und genetischen Risikofaktoren interagieren, ist ein zentraler Schritt auf dem Weg zur Entschlüsselung der komplexen Ursachen von Alzheimer.
Quelle: sciencealert


Kommentar hinterlassen