7 Minuten
Eine vielversprechende Laborstudie zeigt, dass ein Wirkstoffkandidat namens P7C3-A20 den kognitiven Abbau in Mausmodellen mit fortgeschrittener Alzheimer‑ähnlicher Pathologie umkehren kann. Indem die zelluläre Energiemetabolik wiederhergestellt und entzündliche Prozesse reduziert werden, berichten Forschende, dass das geschädigte Gehirn wichtige Funktionen zurückgewinnen kann, selbst ohne die typischen Proteinaggregate vollständig zu entfernen. Diese Ergebnisse haben Bedeutung für die Alzheimer‑Forschung, die Suche nach Neuroprotektion und Ansätze zur Wiederherstellung von NAD+‑Gleichgewicht im Gehirn.
How a single compound targets brain energy
Wissenschaftlerinnen und Wissenschaftler der Case Western Reserve University und Kooperationspartner untersuchten P7C3-A20, eine neuroprotektive Verbindung, die dazu beiträgt, das Gleichgewicht von Nicotinamid‑Adenin‑Dinukleotid (NAD+) wiederherzustellen. NAD+ ist ein zentrales Stoffwechselmolekül: Zellen nutzen es, um Nährstoffe in nutzbare Energie umzuwandeln und um DNA‑Reparatur, Proteinqualitätssicherung und mitochondriale Funktionen zu unterstützen. Ein niedriger NAD+‑Spiegel wird mit dem Altern und mit verschiedenen neurodegenerativen Erkrankungen, einschließlich Alzheimer, in Verbindung gebracht. Die Modulation von NAD+ beeinflusst dabei nicht nur Energiestoffwechsel, sondern auch Signalwege wie Sirtuine und PARP‑Aktivitäten, die für zelluläre Reparaturmechanismen relevant sind.
In der vorliegenden Studie erhielten Mäuse mit fortgeschrittenen Alzheimer‑ähnlichen Symptomen über einen Zeitraum von sechs Monaten tägliche Injektionen mit P7C3-A20. Die Behandlung normalisierte die NAD+‑Konzentrationen in betroffenen Hirnregionen, reduzierte Biomarker für Entzündung und DNA‑Schäden und – was besonders wichtig ist – stoppte die Degeneration von Nervenzellen. Diese biochemische Erholung äußerte sich in messbaren Verbesserungen bei Lern‑ und Gedächtnisleistungen in beiden getesteten Mausstämmen. Konkrete Verhaltensdaten umfassten Verbesserungen in standardisierten kognitiven Tests wie dem Morris Water Maze und bei Konditionierungsaufgaben, die Hinweise auf verbesserte synaptische Funktion und Gedächtniskonsolidierung geben.
Two different Alzheimer's models, one common outcome
Das Team verwendete bewusst zwei genetisch unterschiedliche Mausmodelle, die jeweils eine der beiden kennzeichnenden Alzheimer‑Pathologien repräsentieren: Amyloid‑Beta‑Plaques und Tau‑Tangles. Diese aggregierten Proteine werden häufig in Gehirnen von Alzheimer‑Patientinnen und -Patienten nachgewiesen, doch ihre genaue Rolle in der Entstehung und dem Fortschreiten der kognitiven Beeinträchtigung bleibt komplex und weiterhin Gegenstand intensiver Forschung. Die Wahl zweier Modelle erhöht die Aussagekraft der Beobachtung, weil sie unterschiedliche genetische Ursachen und pathophysiologische Mechanismen abdeckt.
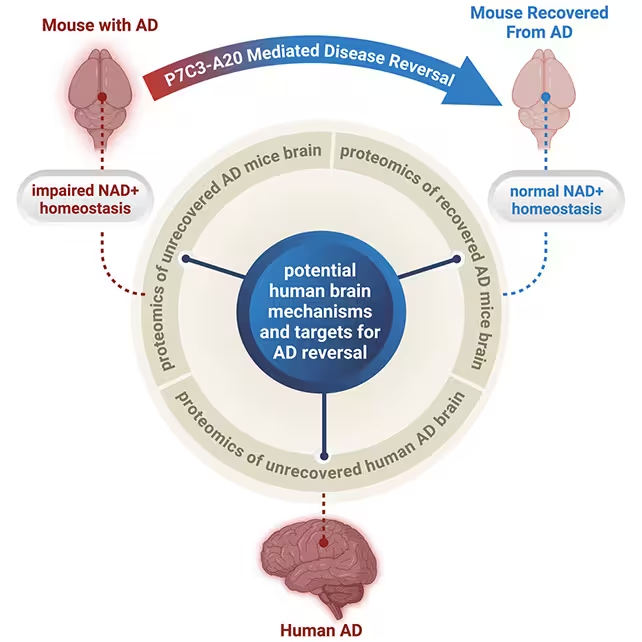
Bemerkenswerterweise verbesserte P7C3-A20 sowohl das Verhalten als auch neuropathologische Marker in beiden Modellen, ohne dass Plaques oder Tangles vollständig entfernt wurden. "Die Wiederherstellung des energetischen Gleichgewichts im Gehirn bewirkte sowohl pathologische als auch funktionelle Erholung in beiden Mausstämmen mit fortgeschrittener Alzheimer‑Pathologie", sagt der Neurowissenschaftler und Psychiater Andrew Pieper. Das Ergebnis legt nahe, dass Neurone, sobald sie ausreichend metabolische Resilienz zurückerlangen, Proteinaggregate besser tolerieren oder funktional kompensieren können. Diese Beobachtung ist relevant für Konzepte wie ‚neuronale Resilienz‘ und verschiebt den Fokus von rein ablativen Therapien (z. B. Clearance von Amyloid) hin zu Maßnahmen, die die zellulären Reparatur‑ und Energiesysteme stärken.
What the findings mean for Alzheimer's research
Die Wiederherstellung von NAD+ scheint der zentrale Mechanismus hinter der beobachteten Erholung zu sein. Frühere präklinische Studien hatten gezeigt, dass NAD+‑Booster nach Hirnverletzungen die Erholung fördern können; die vorliegende Arbeit erweitert diese Ergebnisse auf chronische neurodegenerative Prozesse. In der Publikation in Cell Reports Medicine (2025) berichteten die Autorinnen und Autoren, dass Marker für Entzündung (z. B. erhöhte Mikrogliaaktivierung, Zytokine wie IL‑1β und TNF‑α) sowie DNA‑Schadensmarker (z. B. γH2AX) in den behandelten Tieren abnahmen, was darauf hindeutet, dass Zellen wieder die Fähigkeit erhielten, homöostatische Reparaturprozesse aufrechtzuerhalten.
Technisch betrachtet spricht vieles dafür, dass eine Stabilisierung des NAD+‑Haushalts die funktionelle Kapazität von Mitochondrien, die sirtuinvermittelte Deacetylierung von Proteinen und die Aktivität von DNA‑Reparaturenzymen verbessert. Verbesserte mitochondriale Atmung, reduzierte oxidative Stresssignale und abgeschwächte neuroinflammatorische Reaktionen können zusammen den Abbau von Synapsen und Neuronen verlangsamen oder stoppen. Diese Mechanismen bieten plausible, biologisch fundierte Erklärungen für die beobachteten Verbesserungen bei Lernfähigkeit und Gedächtnis.
Dennoch mahnt das Team zur Vorsicht: Die Übertragung von Ergebnissen aus Mausmodellen auf Menschen ist bekanntermaßen schwierig. Dosierung, Behandlungsbeginn, Verträglichkeit, Pharmakokinetik und langfristige Sicherheit müssen in kontrollierten klinischen Studien sorgfältig geprüft werden. Forschende weisen außerdem darauf hin, dass eine übermäßige NAD+‑Aktivität in bestimmten Kontexten mit einem erhöhten Krebsrisiko assoziiert worden ist; daher wären bei einer möglichen Humantherapie präzise Kalibrierung, Monitoring und Risikobewertung essenziell.
Why this doesn't mean an instant cure
Alzheimer ist eine multifaktorielle Erkrankung, an der genetische Faktoren, Proteinaggregation, Entzündungsprozesse, vaskuläre Gesundheit und weitere Komorbiditäten beteiligt sind. Die Wirkung von P7C3-A20 beseitigt weder Plaques noch Tau‑Tangles, verschiebt aber möglicherweise die Balance zugunsten neuronaler Funktion trotz vorhandener Pathologie – ein wichtiger konzeptueller Wandel. "Dass dieser Effekt in zwei sehr unterschiedlichen Tiermodellen zu sehen ist, die jeweils durch verschiedene genetische Ursachen getrieben werden, stärkt die neue Idee, dass eine Erholung auch bei fortgeschrittener Krankheit möglich sein könnte, wenn das NAD+‑Gleichgewicht im Gehirn wiederhergestellt wird", erklärt Pieper.
Es ist wichtig zu betonen, dass ein solches Konzept nicht zwangsläufig jeden Patienten gleich betrifft: Alter, Krankheitsstadium, genetische Prädisposition (z. B. APOE‑Genotyp), vaskuläre Komorbiditäten und individuelle Unterschiede in Immunantwort und Stoffwechsel werden beeinflussen, wer von einer NAD+‑fokussierten Therapie profitieren könnte. Deshalb sind personalisierte Ansätze und Biomarker zur Identifikation geeigneter Patientengruppen von hoher Bedeutung.
Potential paths forward: trials and safety checks
Als nächste Schritte sind zusätzliche präklinische Untersuchungen geplant, um Dosierungsfenster, Langzeiteffekte und Sicherheit über verschiedene Altersgruppen und genetische Hintergründe hinweg abzusichern. Dazu gehören Studien zur Pharmakokinetik (PK) und Pharmakodynamik (PD), zur Toxikologie sowie zur Wirkung in älteren Tieren oder solchen mit begleitenden vaskulären Veränderungen. Falls diese Daten ermutigend sind, könnten sorgfältig designte Humanstudien folgen – voraussichtlich beginnend mit frühen Phase‑I‑Sicherheitsstudien an gesunden Freiwilligen und Probanden mit leichter bis mittelschwerer Alzheimer‑Demenz.
Parallel werden Forscherinnen und Forscher untersuchen, ob die NAD+‑Wiederherstellung als Monotherapie am effektivsten ist oder ob sie in Kombination mit Behandlungsansätzen, die Entzündung, Gefäßgesundheit und Proteinaggregation adressieren (z. B. Anti‑amyloid Therapien, Antitau‑Strategien, entzündungshemmende oder vaskuläre Interventionen), synergistische Effekte erzielt. Angesichts der Komplexität von Alzheimer erscheint ein mehrgleisiger, multimodaler Therapieansatz plausibel und wahrscheinlich effektiver als einzelne monotherapeutische Maßnahmen.
Wichtige klinische Endpunkte für zukünftige Studien würden neben Sicherheitsparametern auch kognitive Tests (z. B. ADAS‑Cog), funktionelle Messgrößen, neuropsychologische Batteries, MRT‑basierte Bildgebung zur Beurteilung von Gehirnvolumen und Stoffwechsel sowie Biomarker im Liquor und Blut (z. B. neurofilament light chain, p‑Tau, NAD+‑Relevante Marker) umfassen, um Wirkmechanismus, Zielerreichung und klinische Relevanz zu verifizieren.
Expert Insight
Dr. Lena Morales, eine fiktive, aber realistisch dargestellte leitende Neurowissenschaftlerin an einer großen Forschungsuniversität, kommentiert: "Diese Studie verändert unsere Sicht auf Resilienz im alternden Gehirn. Anstatt zu versuchen, jedes pathologische Merkmal vollständig zu entfernen, könnte das Anheben von zellulärem Stoffwechsel und Reparatursystemen die Neurone befähigen, wieder funktionell zu werden – zumindest für eine gewisse Zeit. Das ist ein ermutigender, pragmatischer Ansatz, der andere therapeutische Strategien sinnvoll ergänzt."
Obwohl noch viel Arbeit nötig ist, bietet diese Studie einen hoffnungsvollen und testbaren Ansatz: Kalibriere die Energieökonomie des Gehirns neu, und es könnte möglich sein, Erholung selbst in fortgeschrittenen Krankheitsstadien freizuschalten. Die Forschung wurde in Cell Reports Medicine (2025) veröffentlicht, und das leitende Team betont die Notwendigkeit sorgfältiger, methodischer Folgeuntersuchungen, bevor eine Anwendung beim Menschen in Betracht gezogen wird. Für die Translation in klinische Praxis werden robuste präklinische Daten, transparente Sicherheitsbewertungen und ein klarer regulatorischer Weg unabdingbar sein.
Quelle: sciencealert


Kommentar hinterlassen