7 Minuten
Stellen Sie sich vor, eine gewöhnliche Zimmerpflanze weist Forschende auf einen neuen Wirkstoffkandidaten gegen Alzheimer hin. Seltsam, ja. Doch eine aktuelle, computergestützte Studie der Hassan-II-Universität Casablanca legt nahe, dass Beta‑Sitosterol, ein in den Blättern von Aloe vera vorkommender Pflanzenstoff, mit Enzymen interagieren kann, die mit Gedächtnisverlust in Verbindung stehen — und diese Interaktion sieht in virtuellen Modellen vielversprechend aus.
Aloe vera hat eine lange Tradition in der Volksmedizin: Linderung bei Hautreizungen, Unterstützung der Verdauung, mildernde Wirkung bei Entzündungen. Die wissenschaftliche Evidenz für diese Anwendungen ist unterschiedlich stark und variiert je nach Indikation. Die hier beschriebene Forschung beweist keinen Heilsanspruch. Sie richtet jedoch das Augenmerk auf ein einzelnes Molekül und stellt eine nützliche Frage: Könnte ein pflanzliches Steroid die biochemische Erosion verlangsamen, die zur kognitiven Verschlechterung beiträgt?
Die Studie wurde vollständig in silico durchgeführt — die Forschenden nutzten molekulare Modelle und Simulationen statt Reagenzgläser und klinische Kohorten. Das ist bedeutsam: Computergestützte Chemie und virtuelles Screening können schnell eine große Zahl natürlicher Verbindungen durchsuchen und diejenigen markieren, die am ehesten an ein biologisches Ziel binden. Solche Ansätze liefern Hypothesen und Prioritäten für die Laborarbeit, können jedoch nicht allein beantworten, ob ein Kandidat in lebendem Gewebe sicher, bioverfügbar oder therapeutisch wirksam ist. Dennoch sind Simulationen ein kostengünstiger und schneller Filter, um die nächsten experimentellen Schritte zu fokussieren.
Warum Acetylcholin wichtig ist und was die Simulationen ergaben
Acetylcholin ist ein Neurotransmitter, der für Lern‑ und Gedächtnisprozesse essenziell ist. Bei vielen Menschen mit Alzheimer‑Krankheit sinken die Acetylcholinspiegel im Gehirn, was zu kognitiven Symptomen beiträgt. Zwei Enzyme — Acetylcholinesterase (AChE) und Butyrylcholinesterase (BChE) — bauen Acetylcholin ab. Deshalb ist die Hemmung dieser Enzyme eine etablierte symptomatische Therapie: Wenn Acetylcholin länger verfügbar bleibt, können Gedächtnisfunktionen und Alltagsfähigkeiten verbessert werden.
Das marokkanische Team erstellte dreidimensionale Modelle von AChE und BChE und dockte anschließend virtuell 11 Verbindungen aus Aloe‑vera‑Extrakten in die aktiven Zentren der Enzyme, um Bindungsaffinitäten abzuschätzen — je enger die Passung, desto wahrscheinlicher ist eine Blockade der Enzymaktivität. Nach den berichteten Ergebnissen zeigte Beta‑Sitosterol die stärksten Bindungswerte sowohl für AChE als auch für BChE unter den getesteten Molekülen. Solche Docking‑Scores berücksichtigen typischerweise freie Bindungsenergie, Wasserstoffbrücken, hydrophobe Kontakte und räumliche Komplementarität.
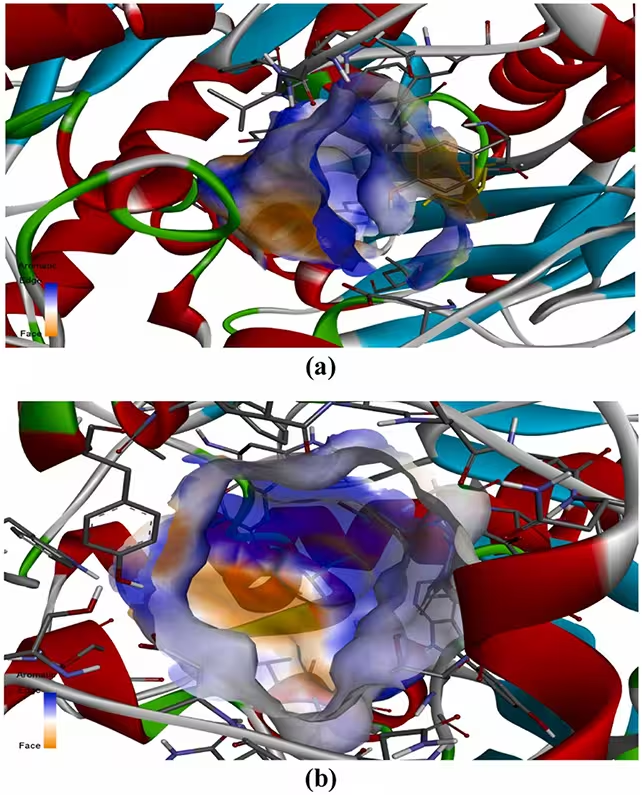
Anhand der Strukturmodelle simulierten die Forschenden, wie gut Aloe‑vera‑Verbindungen in die Bindungsstellen von AChE (oben) und BChE (unten) passen.
Bindung allein ist jedoch nicht ausreichend. Damit ein Molekül als Arzneistoff in Frage kommt, muss es auch pharmakokinetisch und toxikologisch geeignete Eigenschaften aufweisen. Deshalb führten die Autor:innen ADMET‑Vorhersagen durch — also Abschätzungen zu Absorption, Distribution, Metabolismus, Ausscheidung und Toxizität. Diese Modelle gaben für Beta‑Sitosterol akzeptable Eigenschaften an; zusätzlich wurde Succinat (Bernsteinsäure) als eine weitere Verbindung identifiziert, die einer tieferen Untersuchung wert erscheint. ADMET‑Modelle bewerten u. a. Wasserlöslichkeit, Bindung an Plasmaproteine, mögliche Metabolisierung durch CYP‑Enzyme, P‑Glykoprotein‑Substratstatus und mögliche kardio‑ oder genotoxische Risiken.
„Unsere Ergebnisse deuten darauf hin, dass Beta‑Sitosterol, eine der Verbindungen aus Aloe vera, signifikante Bindungsaffinitäten und Stabilität zeigt, was es zu einem vielversprechenden Kandidaten für die weitere Wirkstoffentwicklung macht“, sagt Meriem Khedraoui, Chemikerin in der Studie. Koautor Samir Chtita ergänzt, dass die umfassende Analyse das Potenzial dieser Verbindungen als sichere und wirksame therapeutische Agenzien stützt — eine Formulierung, die vorsichtigen Optimismus ausdrückt und keine voreilige Zuversicht signalisiert.
Grenzen, Kontext und die nächsten Schritte
Eine klare Grenze der Arbeit ist: In silico ist Hypothesengenerierung, nicht Hypothesenbestätigung. Laborassays, Zellkulturstudien und Tiermodelle sind notwendige Schritte vor jeder klinischen Studie. Danach folgen pharmakokinetische Untersuchungen, Dosisfindungsstudien und Sicherheitsprüfungen. Jeder dieser Schritte wird eine Vielzahl von Kandidaten aussortieren.
Konkreter bedeutet das: Für Cholinesterase‑Hemmer wären in vitro‑Assays wie der Ellman‑Test nötig, um die tatsächliche Enzymhemmung zu quantifizieren. Zelluläre Modelle (z. B. neuronale Zelllinien oder humanisierte iPSC‑abgeleitete Neuronen) prüfen zelluläre Verträglichkeit, neurotoxische Effekte und mögliche neuroprotektive Effekte. In vivo‑Studien in transgenen Mausmodellen der Alzheimer‑Krankheit würden dann Angaben zur Wirksamkeit im Organismus, zur Blut‑Hirn‑Schranken‑Penetration und zu Nebenwirkungen liefern. Parallel sind Formulierungsstudien erforderlich: Beta‑Sitosterol ist ein lipophiles Pflanzensterol mit eingeschränkter Wasserlöslichkeit, was die orale Bioverfügbarkeit und die Fähigkeit zur Überwindung der Blut‑Hirn‑Schranke erschweren kann.
Alzheimer ist multifaktoriell komplex. Heute sind mehr als 55 Millionen Menschen weltweit betroffen; Prognosen gehen davon aus, dass bis 2050 etwa 138 Millionen Fälle auftreten könnten, wenn Bevölkerungen altern. Verschiedene Mechanismen tragen vermutlich bei: Proteinfehlfaltung (Amyloid‑ und Tau‑Pathologie), immunologische Reaktionen, vaskuläre Faktoren, Stoffwechselstörungen — und cholinerge Defizite sind nur ein Teil des komplexen Bildes. Das bedeutet, dass kein einzelnes Molekül wahrscheinlich eine universelle Heilung bietet; die Forschung zielt oft darauf ab, Werkzeuge zu finden, die Progression verlangsamen, Lebensqualität verbessern oder in Kombination mit anderen Therapien wirksam sind.
Pflanzliche Naturstoffe bleiben ein fruchtbarer Fundus für solche Werkzeuge. Pflanzlich abgeleitete Moleküle haben die Arzneimittelentwicklung historisch stark geprägt — von Salicylsäure (Vorläufer des Aspirins) bis zu Statinen —, und computergestützte Verfahren beschleunigen die frühen Phasen der Wirkstoffsuche. Der Weg vom Pflanzenmolekül zur zugelassenen Tablette ist jedoch lang, kostspielig und mit hoher Unsicherheit verbunden: chemische Optimierung, Herstellung in pharmazeutischer Qualität, präklinische Sicherheitsdaten, klinische Prüfungen und regulatorische Zulassungsprozesse sind aufwendig und teuer.
Zusätzliche Herausforderungen betreffen die Patentierbarkeit natürlicher Substanzen und die Skalierbarkeit der Gewinnung oder Synthese. Bei einem lipophilen Steroid wie Beta‑Sitosterol können Löslichkeitsverbesserungen, Prodrugs oder Nanocarrier‑Formulierungen nötig werden, um eine gute Bioverfügbarkeit und eine ausreichende Konzentration im Gehirn zu erreichen. Medicinalchemiker können die Struktur modifizieren, um Potenz, Selektivität gegenüber AChE und BChE sowie Blut‑Hirn‑Schranken‑Durchtritt zu optimieren, wobei sie gleichzeitig die Toxizität im Blick behalten müssen.
Expertise und Perspektive
„Computergestützte Screenings gleichen dem Einschalten eines Scheinwerfers in einem dunklen Raum: Sie zeigen interessante Formen, aber man muss sie noch anfassen und prüfen“, sagt Dr. Elena Márquez, Neuropharmakologin, die nicht an der Studie beteiligt war. „Beta‑Sitosterol besitzt chemische Merkmale, die es wert machen, in Enzymassays und zellulären Modellen getestet zu werden. Die entscheidenden Fragen sind, ob es im Gehirn wirksame Konzentrationen erreicht und ob Off‑Target‑Effekte die Anwendung bei älteren Patienten einschränken.“
Die Forschenden betonen die pragmatische Sichtweise. Diese Ergebnisse bedeuten nicht, dass Aloe‑vera‑Gele oder Nahrungsergänzungsmittel Demenz verhindern. Sie bedeuten, dass Verbindungen aus einer bekannten Pflanze biochemische Eigenschaften besitzen, die eine genauere Untersuchung am Labortisch verdienen. Falls nachfolgende in vitro‑ und in vivo‑Untersuchungen Bindung und biologische Effekte bestätigen, könnten Medicinalchemiker Beta‑Sitosterol derivatisieren, um Potenz, Selektivität und Gehirndurchdringung zu verbessern — etwa durch gezielte funktionelle Gruppen, die Polarität und Permeation ausbalancieren.
Alzheimer erfordert mehrere Angriffswege: Einige Behandlungsansätze zielen auf Amyloid‑ oder Tau‑Proteine; andere greifen Entzündungsmechanismen, Durchblutung oder Stoffwechsel an. Cholinesterase‑Hemmer gehören bereits heute zum therapeutischen Instrumentarium zur Symptomlinderung; neue Hemmstoffe, die möglicherweise sicherer oder wirksamer sind, würden das Spektrum der Behandlungsoptionen erweitern.
Aktuell befindet sich Beta‑Sitosterol auf einer durch Simulationen generierten Shortlist — ein Lead, kein Rettungsanker. Die Studie wurde in Current Pharmaceutical Analysis veröffentlicht und fügt einen weiteren Datenpunkt zur umfangreichen, multidisziplinären Suche nach Behandlungsoptionen hinzu. Die nächste Phase ist klar: das Molekül dort testen, wo es zählt — in Zellkulturen und Tiermodellen — und die Evidenzlage Schritt für Schritt verfolgen.
Wissenschaft bewegt sich in kleinen, kumulativen Schritten. Manchmal beginnen diese Schritte unter einer Fensterbank.
Quelle: sciencealert


Kommentar hinterlassen