7 Minuten
Ein routinemäßiger Blick auf das Augenhintergrundbild könnte als frühes Warnsystem für kardiovaskuläre Erkrankungen dienen und aufzeigen, wie schnell eine Person biologisch altert. Neue Forschung, die Netzhautbilder, genetische Daten und Blut-Biomarker kombiniert, deutet auf messbare Signale in winzigen retinalen Gefäßen hin, die den Zustand des Gefäßsystems im gesamten Körper widerspiegeln. Solche retinalen Marker könnten in Zukunft die Früherkennung von Herz-Kreislauf-Risiken, die Bestimmung des biologischen Alters und personalisierte Präventionsstrategien verbessern.
Small vessels, big clues: why the retina matters
Die Netzhaut (Retina) ist einer der wenigen Orte im menschlichen Körper, an denen Mediziner die Mikrogefäße direkt und nicht-invasiv beobachten können. Veränderungen in den Mustern der retinalen Blutgefäße wurden lange als Hinweis auf systemische Gefäßprobleme vermutet. Die aktuelle Studie, veröffentlicht in Science Advances, stärkt diesen Zusammenhang, indem sie zeigt, dass vereinfachte, weniger verzweigte Gefäßnetzwerke in der Netzhaut mit einer höheren genetischen Prädisposition für kardiovaskuläre Erkrankungen und einem beschleunigten biologischen Altern verbunden sind. Solche Befunde stützen die Idee, dass Mikrogefäßveränderungen in der Netzhaut als Surrogatmarker für die Gesundheit des gesamten Gefäßsystems dienen können.
Die Forschenden analysierten Augen-Scans und genetische Informationen von mehr als 74.000 Freiwilligen. Dabei nutzten sie einen Ansatz, der als Mendelsche Randomisierung (Mendelian randomization) bekannt ist, um kausale Zusammenhänge zu prüfen. Bei dieser Methode werden feste genetische Varianten als Instrumente für eine Gesundheitsbedingung eingesetzt, um Ursache und Korrelation besser zu trennen. Da unsere Gene sich im Laufe des Lebens nicht verändern, sind Assoziationen, die auf diese Weise gefunden werden, wahrscheinlicher Ausdruck zugrundeliegender biologischer Mechanismen und weniger das Ergebnis rein zufälliger Zusammenhänge. Dieser methodische Schritt erhöht die Evidenz dafür, dass retinale Gefäßmuster nicht nur Marker, sondern mögliche Teilnehmer an pathophysiologischen Prozessen sind.
What the team found and why it matters
Die Analyse ergab, dass Personen mit geringerer Komplexität der retinalen Gefäße — gemessen als niedrigere fraktale Dimension beziehungsweise vereinfachte Verzweigung — auch ein höheres genetisches Risiko für Herz-Kreislauf-Erkrankungen trugen. Das deutet darauf hin, dass gemeinsame biologische Signalwege sowohl die Gefäßdeterioration in der Netzhaut als auch das erhöhte kardiovaskuläre Risiko an anderen Körperstellen antreiben. Solche gemeinsamen Mechanismen könnten Entzündungsprozesse, vaskulären Umbau, Endothelfunktion oder altersabhängige Veränderungen der Gefäßstruktur umfassen. Die Identifikation dieser Verbindung liefert damit nicht nur prädiktive Informationen, sondern eröffnet auch Ansatzpunkte für therapeutische Interventionen, die darauf abzielen, die Gefäßalterung zu verlangsamen.
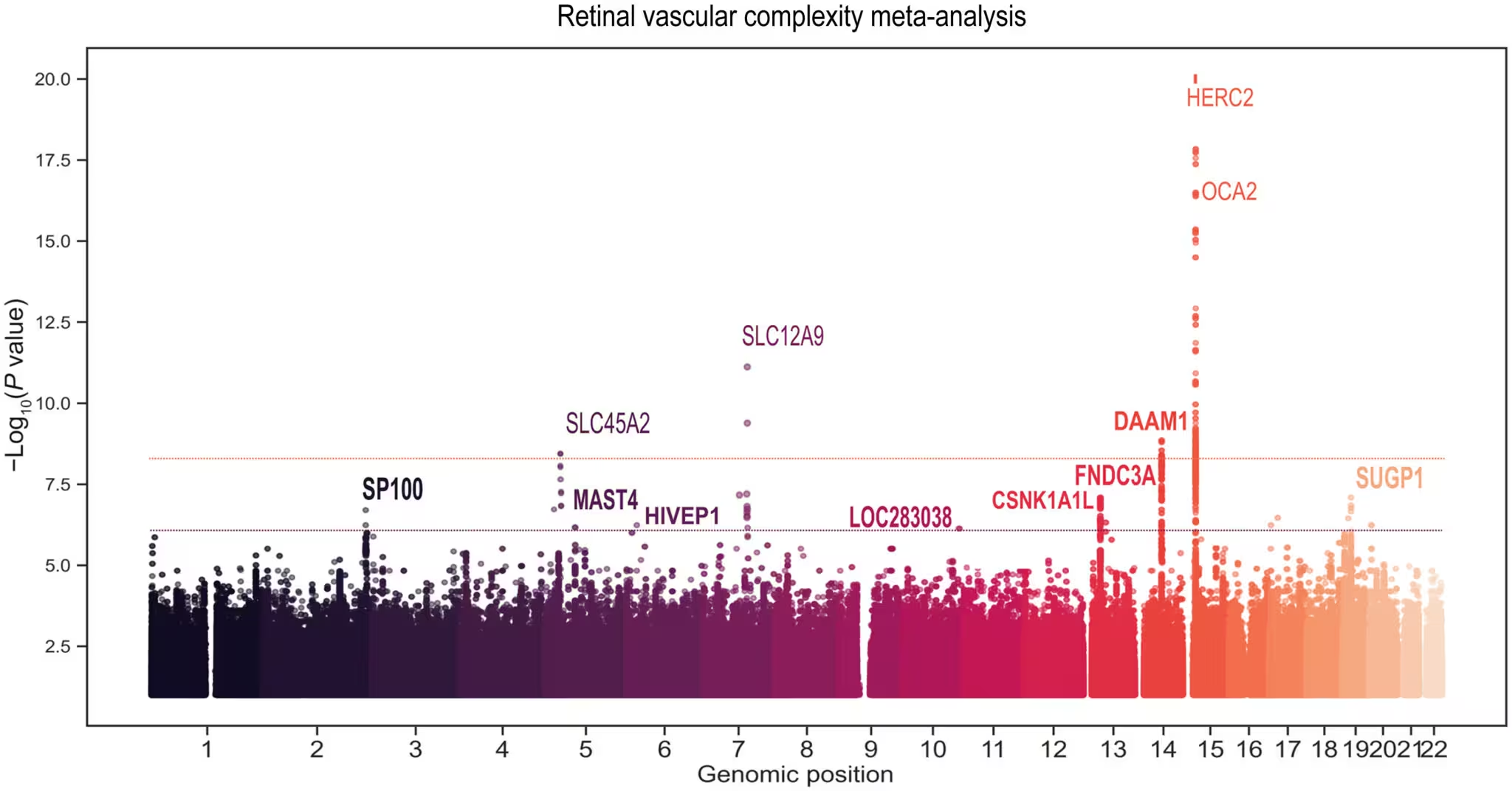
Über Bildgebung und Genetik hinaus verwendete die Studie eine separate Kohorte, um Blutproteine zu scannen und Moleküle zu identifizieren, die diese Veränderungen möglicherweise vermitteln. Zwei Proteine hoben sich deutlich hervor: MMP12, ein Enzym, das mit Gewebeumbau und Entzündungsprozessen verbunden ist, sowie der IgG–Fc-Rezeptor IIb, ein Immunrezeptor, der entzündliche Antworten modulieren kann. Beide scheinen die Struktur kleiner Gefäße zu beeinflussen und könnten zu Zielmolekülen für präventive Therapien werden, die darauf abzielen, die vaskuläre Alterung zu verlangsamen oder inflammatorische Prozesse zu dämpfen. Solche Blut-Biomarker könnten später in multimodalen Risikoscores integriert werden, um die diagnostische Genauigkeit zu erhöhen.
„Das Auge liefert eine einzigartige, nicht-invasive Sicht auf das Gefäßsystem des Körpers“, sagt Marie Pigeyre, Genetikerin an der McMaster University. „Veränderungen in den retinalen Blutgefäßen spiegeln häufig Veränderungen wider, die in den kleinen Gefäßen des gesamten Körpers stattfinden.“ Die Aussagen ihres Teams unterstreichen, wie retinales Screening die Risikoabschätzung von komplexen Laboruntersuchungen auf ein schnelles klinisches Bild verlagern könnte. Ein einfacher Retina-Scan könnte damit als Ergänzung zu traditionellen Risikofaktoren wie Blutdruck, Cholesterin und Familienanamnese dienen und die Früherkennung von Herzinfarkt- oder Schlaganfallrisiken verbessern.
From lab bench to clinic: opportunities and challenges
Aktuelle Bewertungen altersbedingter Gefäßzustände — dazu zählen Herzkrankheiten, Schlaganfälle und vaskulär bedingte Demenzen — basieren häufig auf umfangreichen Bluttests, bildgebenden Verfahren und detaillierten klinischen Anamnesen. Wenn retinal basierte Marker in größeren und diversen Populationen validiert werden, könnten Retina-Scans eine schnellere und kostengünstigere erste Screening-Ebene bieten. Stellen Sie sich vor, ein retinales Foto würde in die routinemäßigen Gesundheitschecks integriert: Kliniker könnten frühzeitig Personen identifizieren, die von gezielten Lebensstilmaßnahmen, intensiverer Überwachung oder spezifischen medikamentösen Strategien profitieren. So könnte die Prävention individualisierter und proaktiver werden, mit potenziell messbarem Einfluss auf Morbidität und Mortalität.
Gleichzeitig bestehen mehrere Herausforderungen, bevor ein solcher Ansatz breit klinisch anwendbar ist. Die Hardware für die Netzhautbildgebung und die Algorithmen zur Interpretation müssen standardisiert werden, um reproduzierbare Ergebnisse zu gewährleisten. Es bedarf klarer klinischer Leitlinien, die definieren, ab welchem Muster der Netzhaut weiterführende Diagnostik oder Interventionen angezeigt sind. Außerdem ist es entscheidend, dass prospektive klinische Studien nachweisen, dass Interventionen, die aufgrund retinaler Marker initiiert werden, tatsächlich zu einer Reduktion klinisch relevanter Endpunkte wie Herzinfarkt oder Schlaganfall führen. Ohne diese Daten bleibt der retinal basierte Ansatz ein vielversprechendes, aber noch experimentelles Werkzeug in der Gefäßmedizin.
Related technologies and future prospects
Fortschritte in der maschinellen Bildanalyse ermöglichen bereits automatisierte Auswertungen retinaler Fotos zur Detektion diabetischer Retinopathie und altersbedingter Makuladegeneration. Die Ausweitung dieser Tools, um vaskuläre fraktale Dimensionen quantitativ zu erfassen und mit genetischem oder proteomischem Risiko zu verknüpfen, könnte umfassende Screening-Plattformen schaffen. Solche Systeme würden Deep-Learning-Modelle mit klinischen Daten, Biomarkern und genetischen Risikoscores kombinieren, um individualisierte Vorhersagen zu treffen. Darüber hinaus könnten Blutbasierte Biomarker wie MMP12 und der IgG–Fc-Rezeptor IIb in multimodale Risikobewertungen integriert werden, wodurch die Spezifität steigt und die Entwicklung zielgerichteter Therapien gefördert wird.
Auf längere Sicht sind mehrere Entwicklungspfade denkbar: Validierte, standardisierte Retina-Algorithmen in der Primärversorgung; mobile oder portable Funduskameras, die Screening in unterversorgten Regionen ermöglichen; sowie klinische Studien, die Medikamente testen, die gezielt vaskuläre Entzündungs- oder Umbauprozesse adressieren. Die Kombination aus Bildgebung, Genetik und Proteomik eröffnet einen datengetriebenen Ansatz zur Prävention von Herz-Kreislauf-Erkrankungen und zur Verlangsamung des biologischen Alterns der Gefäße.
Expert Insight
Dr. Elena Ramirez, eine kardiovaskuläre Forscherin, die nicht an der Studie beteiligt war, kommentiert: „Diese Arbeit verbindet elegant Bildgebung, Genetik und Proteomik. Sie erweitert die Anwendung retinaler Scans über augenärztliche Fragestellungen hinaus und führt sie in die systemische Risikoabschätzung ein. Der nächste Schritt sind prospektive Studien, die testen, ob frühes Handeln auf Basis retinaler Signale Herzinfarkte oder Schlaganfälle verhindern kann.“ Solche kontrollierten Studien sind unerlässlich, um die klinische Relevanz retinaler Marker und damit verbundener Interventionen zu belegen.
Für Kliniker und Forscher rückt die Netzhaut damit als praktikables Fenster in die vaskuläre Alterung in den Fokus. Mit Fortschritten bei der Bildgebung, standardisierten Auswertealgorithmen und erweiterten Biomarker-Panels könnten Retina-Scans zukünftig zu einem routinemäßigen Bestandteil der präventiven Versorgung werden. Dies würde ermöglichen, kardiovaskuläre Risiken früher zu erkennen, individuelle Maßnahmen gezielter anzuwenden und letztlich das biologische Alter der Gefäße zu verlangsamen — ein potenziell wichtiger Schritt zur Reduktion kardiovaskulärer Erkrankungen weltweit.
Quelle: sciencealert

Kommentar hinterlassen