8 Minuten
Eine neue Übersichtsarbeit von Forschenden der University of Birmingham und der University of Oxford zeigt, dass kontrollierte Dosen von Distickstoffmonoxid — im Alltag oft als Lachgas bezeichnet — bei einigen Menschen rasche und klinisch bedeutsame Verringerungen depressiver Symptome bewirken können, einschließlich bei Personen mit behandlungsresistenter Depression (TRD). Die Analyse fasst aktuelle klinische Studien zusammen, diskutiert mögliche Wirkmechanismen im Gehirn, und beleuchtet Chancen sowie Risiken dieser schnell wirkenden Intervention. Für Patientinnen und Patienten, bei denen klassische Antidepressiva nur langsam oder gar nicht ansprechen, bietet Lachgas potenziell eine zusätzliche Behandlungsoption, die akute Suizidalität und schwere depressive Episoden kurzfristig lindern kann. Gleichzeitig sind Sicherheitsfragen, Langzeiteffekte und praktikable Behandlungsprotokolle bisher noch nicht abschließend geklärt.
Welche Studien wurden untersucht und welche Ergebnisse zeigten sie
Das Team wertete sieben bereits durchgeführte klinische Studien mit insgesamt 247 Teilnehmenden sowie vier geplante Studienprotokolle aus. In den untersuchten Studien inhalierten die Freiwilligen Distickstoffmonoxid gemischt mit Sauerstoff in Konzentrationen von typischerweise 25 % oder 50 %, und die Ergebnisse wurden mit Placebo‑Inhalationen verglichen. Über die Studien hinweg zeigte sich, dass die höhere 50%ige Konzentration tendenziell die stärkste und schnellste Symptomlinderung bewirkte. Dieser stärkere Effekt ging jedoch mit einer höheren Häufigkeit kurzzeitiger Nebenwirkungen wie Übelkeit, Kopfschmerzen und transienten dissoziativen Empfindungen einher.
Ein zentrales Ergebnis war die schnelle Wirkung: messbare Stimmungsverbesserungen konnten bereits innerhalb von zwei Stunden nach einer einzigen Gabe auftreten. Diese sehr rasche Ansprechzeit ordnet Lachgas einer wachsenden Gruppe schnell wirkender Interventionen zu — ähnlich dem klinischen Interesse an Ketamin — mit dem Ziel, akute Suizidalität und schwere depressive Episoden zu reduzieren, wenn herkömmliche Antidepressiva mehrere Wochen brauchen, um zu wirken.
Die meisten Studien waren randomisiert und placebokontrolliert, wenn auch mit relativ kleinen Stichproben. Effektstärken variierten zwischen den Studien, und nicht alle Ergebnisse erreichten in allen Messungen statistische Signifikanz. Einige Studien berichteten von kurzfristigen Verbesserungen bei depressiven Scores (z. B. Montgomery–Åsberg Depression Rating Scale oder Hamilton‑Skalen), während die Dauer des Effekts im Allgemeinen begrenzt war und ohne wiederholte Gaben rasch abnahm. In mehreren Protokollen sind deshalb Wiederholungsdosen oder Seriensitzungen vorgesehen, um eine anhaltendere Wirkung zu erzielen.
Wichtig für die klinische Einschätzung sind zudem die Unterschiede in Studiendesigns: Es gab Variationen in Einschlusskriterien (z. B. Schweregrad der Depression, Vorbehandlung), in der genauen Zusammensetzung der Gasgemische (insbesondere Sauerstoffanteil), in der Dauer der Inhalation und in der Art des Placebos. Solche Heterogenitäten erschweren direkte Vergleiche, legen aber gleichzeitig nahe, dass weitere standardisierte, größere randomisierte kontrollierte Studien (RCTs) notwendig sind, um optimale Dosierungsschemata und Patientengruppen zu identifizieren, die am meisten profitieren.
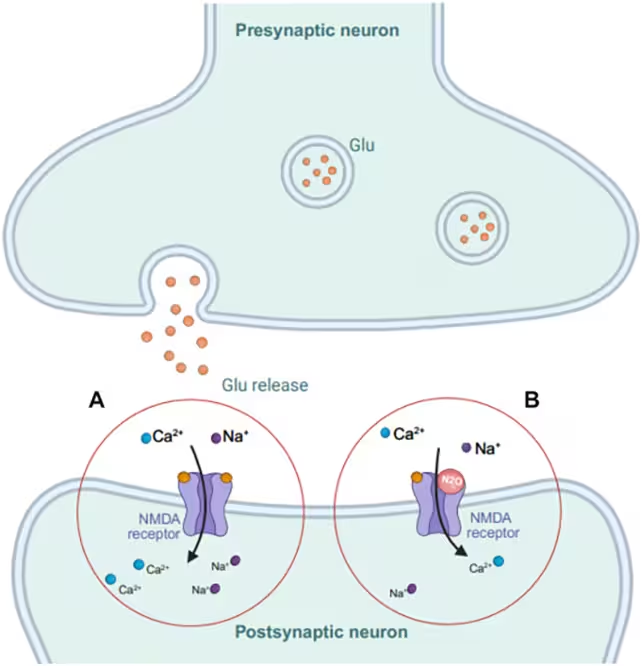
Lachgas (dargestellt durch die roten Kreise) könnte gegen Depression wirken, indem es die Signalübertragung zwischen Neuronen abschwächt.
Wie Lachgas im Gehirn wirken könnte
Forschende vermuten, dass die antidepressiven Effekte von Distickstoffmonoxid maßgeblich durch die Modulation des glutamatergen Systems zustande kommen — jenes Netzwerk von Neuronen, das den Neurotransmitter Glutamat verwendet, der die wichtigste exzitatorische Signalübertragung im Gehirn vermittelt. Eine Fehlregulation der Glutamatergik ist vielfach mit Major Depression (MDD) und therapieresistenter Depression (TRD) in Verbindung gebracht worden.
Mechanistisch wird diskutiert, dass Lachgas unter anderem als partieller Antagonist an NMDA‑Rezeptoren wirken kann, vergleichbar mit den Effekten von Ketamin, wodurch die synaptische Plastizität verändert und kurzfristig die glutamaterge Überaktivität gedämpft wird. Solche Veränderungen können eine Kaskade von Folgeprozessen auslösen, darunter erhöhte Ausschüttung von Brain‑Derived Neurotrophic Factor (BDNF) und eine Förderung synaptischer Neubildung, die mit stimmungsaufhellenden Effekten in Verbindung gebracht werden. Ob diese molekularen Veränderungen bei Menschen in vivo zuverlässig nachweisbar sind, ist Gegenstand aktueller Forschung.
Neben direkten Effekten auf Neurotransmitter moduliert Distickstoffmonoxid auch den zerebralen Blutfluss. Eine gesteigerte Hirnperfusion könnte die Versorgung mit Sauerstoff und Nährstoffen verbessern, den Abtransport metabolischer Abfallprodukte fördern und so das neuronale Milieu positiv beeinflussen. Es ist bislang unklar, in welchem Maß vaskuläre Effekte versus synaptische Modulationen für die klinische Wirkung verantwortlich sind — wahrscheinlich handelt es sich um eine Kombination beider Mechanismen.
Weitere Hypothesen beziehen immunologische und inflammatorische Pfade ein: Es gibt Hinweise, dass schnell wirkende Antidepressiva entzündliche Marker beeinflussen können, was besonders für Patienten mit erhöhten Entzündungsparametern relevant sein könnte. Funktionelle Bildgebung (fMRT), EEG und PET‑Studien könnten in zukünftigen Arbeiten helfen, typische Signaturmuster der Lachgaswirkung zu identifizieren und so prädiktive Biomarker für das Behandlungsergebnis zu entwickeln.
Für die klinische Anwendung ist es wichtig, die pharmakodynamische Zeitachse genau zu verstehen: Während die symptomatische Verbesserung rasch eintritt, folgen strukturelle synaptische Veränderungen (falls vorhanden) wahrscheinlich verzögert und könnten für eine länger anhaltende Remission entscheidend sein. Hier setzt die Forschung an: Dosierung, Frequenz und Kombination mit anderen Therapien (z. B. medikamentöse Erhaltungstherapie, Psychotherapie) müssen systematisch untersucht werden, um therapeutische Protokolle zu optimieren.
Klinische Implikationen und Sicherheitsaspekte
Die in der Übersichtsarbeit zitierten Kliniker betonen sowohl das Potenzial als auch die Notwendigkeit von Vorsicht: Für Patientinnen und Patienten, die alle anderen Optionen ausgeschöpft haben, kann eine schnelle Linderung lebensverändernd sein. Zugleich sind die bislang beobachteten Effekte häufig nur kurzzeitig, sofern keine wiederholten Behandlungen vorgenommen werden. Wiederholte Verabreichungen könnten den Nutzen verlängern, werfen aber Fragen zur Langzeitsicherheit und zum praktischen Ablauf in klinischen Settings auf.
Wichtige Sicherheitsaspekte umfassen akute Nebenwirkungen wie Übelkeit, Kopfschmerz, Schwindel und transient dissoziative Zustände, die bei höheren Konzentrationen (z. B. 50 %) häufiger auftreten. Zusätzlich gibt es gut belegte biologische Risiken bei wiederholter oder längerer Exposition gegenüber Distickstoffmonoxid: Die Substanz inaktiviert Vitamin B12 (Cobalamin) und kann dadurch Störungen der Methionin‑ und Folatstoffwechselwege verursachen. Bei längerfristiger oder häufiger Anwendung besteht deshalb ein Risiko für neurologische Schäden, vor allem neuropathische Symptome, die mit Vitamin‑B12‑Mangel assoziiert sind. Daher empfehlen Expertinnen und Experten, bei wiederholter Gabe Serum‑B12‑Werte zu überwachen und bei Bedarf zu substituieren.
Weiterhin sind klassische Kontraindikationen zu beachten: Distickstoffmonoxid kann gasgefüllte Körperhöhlen erweitern und ist daher bei Pneumothorax, schweren chronischen Lungenerkrankungen mit gefährlichen Luftansammlungen, oder bei ausgeprägten Mittelohrproblemen mit Vorsicht zu verwenden. In der Schwangerschaft sollte Lachgas nur in Ausnahmefällen und nach sorgfältiger Nutzen‑Risiko‑Abwägung eingesetzt werden. Zudem besteht ein Missbrauchspotenzial: Lachgas wird in nichtklinischen Kontexten als Rauschmittel verwendet, weshalb therapeutische Programme strenge Kontrollen, sichere Lagerung und dokumentierte Anwendung erfordern.
Logistische Herausforderungen betreffen die sichere Gaszufuhr in Klinikräumen: Adäquate Beatmungs‑ und Abgasabsaug‑Systeme, kontinuierliche Überwachung der Vitalfunktionen während der Inhalation, qualifiziertes Personal und Notfallmanagement sind Voraussetzung. Darüber hinaus müssen Behandlungszentren Protokolle für Screening, Aufklärung, Einwilligung, Nachbeobachtung und Dokumentation etablieren, um Patientensicherheit zu gewährleisten.
Aus regulatorischer Sicht gilt Distickstoffmonoxid bislang in vielen Ländern nicht als standardmäßige antidepressive Therapie. Bis belastbare Langzeitdaten vorliegen, sollte die Anwendung auf kontrollierte Forschung oder spezialisierte Zentren beschränkt bleiben, die entsprechende Sicherheitsvorkehrungen und Monitoring‑Routinen bieten.
Nächste Schritte für Forschung und Praxis
Künftige Arbeiten müssen größere randomisierte, placebokontrollierte Studien mit längeren Nachbeobachtungszeiträumen und standardisierten Endpunkten umfassen. Head‑to‑head‑Vergleiche mit anderen schnell wirkenden Behandlungen, vor allem Ketamin bzw. Esketamin, sind notwendig, um relativen Nutzen, Sicherheitsprofile und Kosten‑Nutzen‑Aspekte zu ermitteln. Ebenso wichtig sind Dosisfindungsstudien, die Konzentrationen und Inhalationsdauern identifizieren, die ein optimales Verhältnis von Schnelligkeit, Dauer und Verträglichkeit liefern.
Forschungsfragen, die priorisiert werden sollten, umfassen:
- Welche Patientenmerkmale (klinische, bildgebende oder molekulare Biomarker) sagen ein gutes Ansprechen auf Lachgas voraus?
- Welche Wiederholungsintervalle und kumulativen Dosen sind effektiv und sicher für eine anhaltende Symptomkontrolle?
- Wie lässt sich das Risiko für Vitamin‑B12‑depletionsbedingte Nebenwirkungen minimieren (Screening, Supplementation)?
- Wie verhält sich Lachgas in direkten Vergleichen zu Ketamin hinsichtlich Wirkdauer, Nebenwirkungsprofil und Umsetzbarkeit in Routinekliniken?
Auf der Praxis‑Ebene sollten Klinikerinnen und Kliniker derzeit Lachgas als experimentelle Option betrachten und es nur in kontrollierten Forschungssettings oder spezialisierten Kliniken einsetzen, die über geeignete Monitoring‑ und Notfallstrukturen verfügen. Bei laufenden Studien sind strikte Einschluss‑ und Ausschlusskriterien, standardisierte Messzeiten für primäre und sekundäre Endpunkte sowie transparente Berichterstattung über Nebenwirkungen essenziell.
Langfristig könnte Distickstoffmonoxid Teil einer neuen Generation schnell wirkender Interventionen gegen schwere Depression werden und damit die therapeutische Palette für Personen erweitern, die nicht auf bestehende Therapien ansprechen. Bis dahin bleibt die Entwicklung evidenzbasierter Leitlinien und die Durchführung groß angelegter, gut konzipierter klinischer Studien die zentrale Aufgabe der Forschungsgemeinschaft.
Zusammengefasst: Die aktuelle Evidenz ist vielversprechend, aber vorläufig. Lachgas zeigt Potenzial als schnell wirkende, symptomatisch effektive Intervention für manche Patientinnen und Patienten mit Depression, insbesondere bei behandlungsresistenter Form. Solange größere, langfristige Studien fehlen, sollte Distickstoffmonoxid für Depression nur in Forschungs- oder spezialisierten klinischen Kontexten mit angemessenem Sicherheitsmonitoring angewendet werden.
Quelle: sciencealert


Kommentar hinterlassen