8 Minuten
Neue Forschung legt nahe, dass nicht alle depressiven Symptome gleich stark mit dem Demenzrisiko verknüpft sind. Eine langfristige britische Studie identifiziert sechs spezifische Symptome im Mittelleben, die mit höheren Demenzraten Jahrzehnte später verbunden sind – und diese Hinweise könnten Klinikerinnen und Klinikern helfen, frühzeitig präventive Maßnahmen zu fokussieren.
Which depressive signs matter most?
Die Studie, geleitet von Forschenden am University College London, verfolgte 5.811 Teilnehmende über einen Zeitraum von rund 20 Jahren. Die psychische Verfassung wurde zwischen 1997 und 1999 erhoben, als die Teilnehmenden im Alter von 45–69 Jahren und ohne Demenz waren; anschließend wurden die Gesundheitsdaten bis 2023 aus Registren und medizinischen Unterlagen nachverfolgt. Insgesamt erhielten 10,1 % der Teilnehmenden im Studienverlauf eine Demenzdiagnose.
Statt Depression als einheitliche Diagnose zu betrachten, identifizierte das Team sechs einzelne Symptome, die maßgeblich mit dem erhöhten Risiko verbunden waren. Diese Symptome sind:
- Verlust des Selbstvertrauens
- Schwierigkeiten, mit Problemen fertigzuwerden
- Kein Gefühl von Zuneigung gegenüber anderen
- Anhaltende Nervosität
- Konzentrationsschwierigkeiten
- Unzufriedenheit mit der Art und Weise, wie Aufgaben durchgeführt werden
Personen, die im Mittelleben fünf oder mehr depressive Symptome angaben, hatten insgesamt ein um 27 % erhöhtes Demenzrisiko. Dieses erhöhte Risiko wurde jedoch überwiegend durch die oben genannten sechs Symptome getragen. Zwei davon fielen besonders auf: Der Verlust des Selbstvertrauens und Schwierigkeiten beim Umgang mit Problemen waren jeweils mit einem etwa 50 % höheren Demenzrisiko assoziiert.
Die Autorinnen und Autoren betonen, dass andere depressive Merkmale – wie Schlafstörungen oder Suizidgedanken – in dieser Kohorte keine klare langfristige Verbindung zur Demenz zeigten.
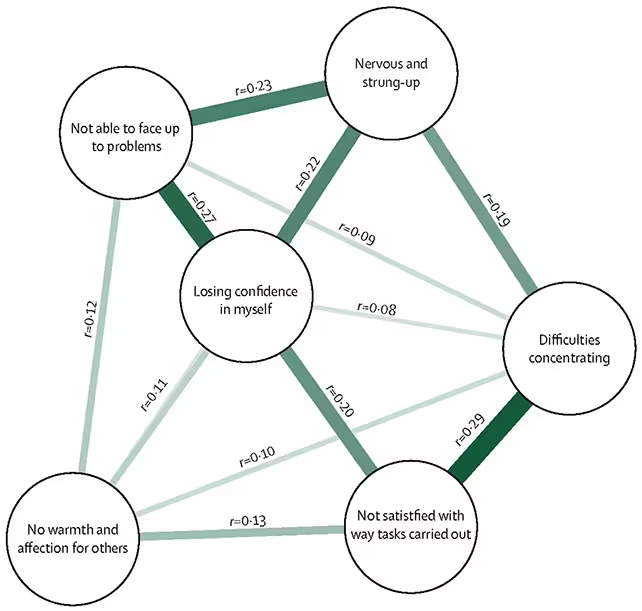
Die Forschenden verknüpften sechs depressive Symptome mit dem Demenzrisiko
How the study was done and what the numbers mean
Es handelte sich um eine longitudinale, beobachtende Studie: eine effiziente Methode, um Muster über Jahrzehnte zu identifizieren, die jedoch keine kausalen Schlussfolgerungen erlaubt. Gesundheitsoutcomes wurden aus nationalen Registern und medizinischen Unterlagen gewonnen, und die psychischen Messgrößen zum Ausgangszeitpunkt beruhten auf etablierten Symptomfragebögen und Inventaren.
Die Methodik ist wichtig, um die Aussagekraft der Ergebnisse einzuordnen. Längsschnittdaten ermöglichen es, zeitliche Zusammenhänge und Vorläufer von Erkrankungen zu erkennen. Allerdings können beobachtende Studien Störfaktoren nicht vollständig ausschließen – zum Beispiel sozioökonomische Bedingungen, Bildungsniveau, Lebensstilfaktoren oder bereits vorhandene, aber nicht diagnostizierte medizinische Veränderungen.
Warum ist das relevant? Wenn bestimmte emotionale oder kognitive Muster im Mittelleben verlässlich auf spätere Verwundbarkeiten hinweisen, könnten Ärztinnen und Ärzte frühzeitig Personen mit erhöhtem Demenzrisiko identifizieren und präventive Maßnahmen testen – von Lebensstilinterventionen bis zu gezielter psychischer Versorgung. Solche Screening-Strategien in der Primärversorgung könnten sich auf Symptome konzentrieren, die laut dieser Studie die größte prognostische Aussagekraft besitzen.
Biological and behavioral links worth watching
Depression und Demenz teilen mehrere plausible biologische und verhaltensbezogene Pfade. Chronischer Stress und depressive Erkrankungen können die Herz-Kreislauf-Gesundheit verschlechtern, systemische Entzündungsprozesse fördern und die sogenannte kognitive Reserve reduzieren – Faktoren, die zur Entwicklung verschiedener Demenzformen beitragen können. Symptome wie Konzentrationsstörungen oder anhaltende Angst können entweder frühe Hinweise auf neuronale Veränderungen sein oder den Verlauf beschleunigen, indem sie Schlafqualität, körperliche Aktivität und soziale Teilhabe negativ beeinflussen.
Auf zellulärer und systemischer Ebene werden Mechanismen diskutiert, die das Zusammenspiel von psychischer Gesundheit und neurodegenerativen Prozessen erklären könnten: Dysregulation der Hypothalamus-Hypophysen-Nebennieren-Achse (HPA-Achse) und erhöhte Cortisolspiegel, vaskuläre Schäden durch Bluthochdruck oder Diabetes, chronische niedriggradige Entzündung sowie Veränderungen in neurotrophen Faktoren, die für Synapsenbildung und neuronale Plastizität wichtig sind. Diese biologischen Pfade sind plausibel, werden aber in der vorliegenden Studie nicht direkt gemessen.
Verhaltensfaktoren spielen ebenfalls eine Rolle. Anhaltende depressive Symptome können zu sozialer Isolation, verminderter körperlicher Aktivität, suboptimaler Ernährung und schlechterem Schlaf führen – allesamt Risikofaktoren für kognitive Verschlechterung. Das Konzept der kognitiven Reserve, also der Fähigkeit des Gehirns, Schäden zu kompensieren, wird von Bildung, beruflicher Komplexität und sozialer Aktivität beeinflusst; depressive Symptome im Mittelleben können diese schützenden Faktoren schwächen.
Das präzisere Verständnis, welche einzelnen Symptome die höchste prognostische Relevanz haben, hilft, Risikomodelle zu verfeinern. Es verschiebt die Perspektive weg von der pauschalen Behandlung von "Depression" als einem einzigen Risikomarker hin zu einer differenzierten, symptombasierten Einschätzung.
Limits of the findings: who was studied?
Das UCL-Team weist auf wichtige Einschränkungen hin. Die Teilnehmenden stammen aus einer langjährigen britischen Kohorte, die überwiegend aus Angestellten des öffentlichen Dienstes bestand – eine Gruppe, die tendenziell gesünder ist als die allgemeine Bevölkerung. Die Demenzraten in der Studie lagen niedriger als in größeren Bevölkerungsstichproben im Vereinigten Königreich, sodass die genauen Risikozahlen möglicherweise nicht direkt auf andere Länder oder Bevölkerungsgruppen übertragbar sind.
Weitere Forschung in vielfältigeren Populationen ist daher nötig – etwa in Gruppen mit unterschiedlichem sozioökonomischem Hintergrund, unterschiedlicher ethnischer Zusammensetzung und unter verschiedenen Gesundheitssystemen. Darüber hinaus ist zu prüfen, ob ähnliche Muster auch in Bevölkerungen mit höherer Basisprävalenz kardiovaskulärer Risikofaktoren bestehen.
Nicht zuletzt ist zu beachten, dass die Studie die Symptome einmalig zu Studienbeginn erfasste. Depressive Symptome können im Zeitverlauf variieren; wiederholte Messungen würden Aufschluss darüber geben, ob anhaltende oder sich verändernde Symptome unterschiedlich mit späterer Demenz verknüpft sind.
Trotz dieser Limitationen ist das Signal konsistent: Bestimmte emotionale und kognitive Beschwerden im Mittelleben scheinen nützliche Informationen über die spätere Hirngesundheit zu liefern.
What this could mean for prevention
Gezielte Screenings in der Primärversorgung könnten die spezifischen Symptome erfassen, die in der Studie hervorgehoben wurden. Ein pragmatischer Ansatz wäre, neben allgemeinen Depressionsscreenings auch auf einzelne Symptome wie Selbstvertrauensverlust, Problembewältigungsfähigkeiten, anhaltende Nervosität und Konzentrationsstörungen zu achten. Standardisierte Werkzeuge wie der PHQ-9 oder ergänzende symptomorientierte Fragen können dabei unterstützen, Risikopersonen zu identifizieren.
Auf Basis einer solchen Identifikation könnten Klinikerinnen und Kliniker Interventionen anbieten, die die Hirngesundheit fördern: Behandlung bzw. Kontrolle kardiovaskulärer Risikofaktoren (z. B. Blutdruck, Diabetes, Hyperlipidämie), Förderung körperlicher Aktivität, Programme zur sozialen Teilhabe, Stressreduktionsstrategien (z. B. Achtsamkeit, Stressmanagement) und gezielte psychotherapeutische Verfahren, die auf Problemlösefähigkeiten und Selbstwirksamkeit abzielen. Multimodale Präventionsprogramme wie kognitive Trainings kombiniert mit körperlicher Aktivität und sozialer Unterstützung könnten besonders wirksam sein.
Wichtig ist, dass die symptombezogene Strategie auch die Forschung an biologischen Mechanismen vorantreibt: Wissenschaftlerinnen und Wissenschaftler können prüfen, ob diese mittleren Lebenszeichen frühe neurobiologische Veränderungen widerspiegeln (z. B. strukturelle Veränderungen im Hippocampus, Biomarker im Liquor, neuroimaging-Befunde) oder ob sie vor allem soziale und verhaltensbedingte Pfade markieren, die die kognitive Reserve beeinflussen.
Insgesamt eröffnet die Fokussierung auf einzelne Symptome praxisnahe Handlungsoptionen: Früherkennung, gezielte Interventionen und individuellere Präventionspläne könnten helfen, das Risiko für spätere kognitive Einschränkungen zu vermindern.
Expert Insight
"Wenn wir über Demenzprävention sprechen, ist der richtige Zeitpunkt entscheidend", sagt Dr. Elena Morales, eine Neurologin mit Schwerpunkt kognitive Störungen. "Das Mittelleben ist ein Fenster, in dem kleine Anpassungen – etwa das Behandeln von Bluthochdruck, die Verbesserung des Schlafs oder das Angehen anhaltender Angstzustände – langfristige Verläufe verschieben können. Studien, die zeigen, welche Symptome am besten vorhersagen, geben Klinikerinnen und Klinikern praktikable Signale, um früher einzugreifen."
Forschung wie diese liefert keine deterministischen Vorhersagen für Einzelpersonen, öffnet jedoch Wege für frühere, individuellere Präventionsstrategien. Angesichts der demografischen Alterung weltweit könnten solche inkrementellen Verbesserungen zu spürbaren Reduktionen von Demenzfällen führen.
Zukünftige Studien müssen die Befunde in breiteren Stichproben replizieren und experimentell prüfen, ob gezielte Interventionen gegen die hervorgehobenen Symptome tatsächlich zu besseren kognitiven Ergebnissen führen. Bis dahin lautet die praktische Schlussfolgerung: Einige alltägliche Schwierigkeiten im Mittelleben geben uns womöglich mehr Auskunft über die spätere Hirngesundheit, als bislang angenommen – und eine erhöhte Aufmerksamkeit kann sinnvoll sein.
Abschließend ist es hilfreich, konkrete Handlungsempfehlungen für Ärztinnen, Ärzte und Betroffene zu nennen: regelmäßige Blutdruck- und Stoffwechselkontrollen, geförderte körperliche Aktivität (mindestens 150 Minuten moderater Bewegung pro Woche), soziale Vernetzung, Schlafhygiene und bei anhaltenden psychischen Beschwerden zeitnahe fachärztliche oder psychotherapeutische Abklärung. Symptomorientierte Prävention kann sowohl biologische als auch verhaltensbezogene Risikofaktoren adressieren und so zur Förderung der kognitiven Reserve beitragen.
Quelle: sciencealert


Kommentar hinterlassen