6 Minuten
Eine neue genetische Analyse legt nahe, dass stärkere Blutzuckerspitzen in den ersten zwei Stunden nach einer Mahlzeit – oft als postprandiale oder 2-Stunden-Post-Load-Glukose-Spitzen bezeichnet – mit einem deutlich erhöhten Risiko für die Entwicklung von Alzheimer in Verbindung stehen könnten. Dieses Ergebnis ergänzt ein komplexes Bild, das Diabetes, Insulinfunktion und Demenz verknüpft, und lenkt die Aufmerksamkeit auf die postprandiale Blutzuckersteuerung als möglichen Zielpunkt der Prävention.
Was die Studie untersuchte und fand
Forschende im Vereinigten Königreich werteten genetische Daten von 357.883 Personen aus, um zu prüfen, ob genetische Varianten, die eine Neigung zu höheren 2-Stunden-Post-Load-Glukosewerten (2hPG) anzeigen, auch das spätere Risiko für eine Alzheimer-Krankheit erhöhen. Anstatt den Blutzucker direkt zu messen, nutzte das Team die Mendelianische Randomisierung, eine Methode, die vererbte genetische Varianten als Proxies für die lebenslange Exposition gegenüber einem Merkmal verwendet – hier die Neigung zu postprandialen Glukosespitzen. Weil genetische Variation bereits bei der Empfängnis zugeordnet wird und späteren Lebensstil oder Erkrankungen nicht rückwirkend beeinflusst, stärkt die Mendelianische Randomisierung kausale Schlussfolgerungen und reduziert Verzerrungen durch umgekehrte Kausalität oder konfunderende Lebensstilfaktoren.
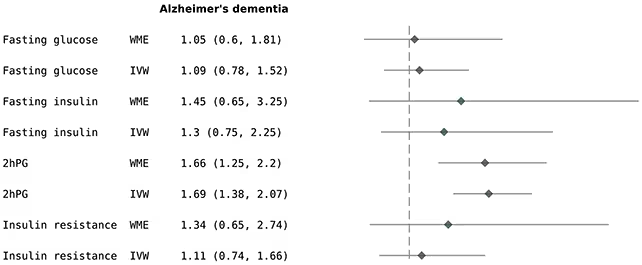
Die Analyse ergab, dass eine genetische Veranlagung für höhere 2hPG-Werte mit einem um etwa 69 % erhöhten Risiko für Alzheimer assoziiert war. Auffällig war dabei, dass die Studie keine vergleichbaren Zusammenhänge für Nüchtern-Glukose, Ausgangs-Insulinspiegel oder breit gefasste Maße der Insulinresistenz mit Alzheimer oder Demenz insgesamt fand. Dieses Muster deutet darauf hin, dass möglicherweise die kurzzeitigen, postprandialen Blutzuckerspitzen – und nicht dauerhafte erhöhte Nüchternwerte oder generelle Insulinresistenz per se – in diesem Datensatz besonders relevant für das Alzheimer-Risiko sind. Solche Befunde werfen neue Fragen zur Pathophysiologie auf und lenken die Forschung hin zu zeitlich begrenzten metabolischen Stressereignissen nach Mahlzeiten.
Methoden, Hirnbildgebung und offene Fragen
Im Rahmen der Studie standen für einen Teil der Teilnehmenden auch bildgebende Hirnaufnahmen zur Verfügung. Diese Bilddaten zeigten keine offensichtlichen Zusammenhänge zwischen Glukose- oder Insulinmerkmalen und klar messbaren strukturellen Veränderungen wie einer verringerten Hippocampus-Volumen oder ausgeprägteren weißen-matter-Läsionen. Das spricht dafür, dass der Zusammenhang zwischen postprandialem Blutzucker und Alzheimer eher über subtilere metabolische, inflammatorische oder funktionelle Mechanismen vermittelt werden könnte, die mit Standard-MRT nicht ohne Weiteres als großflächiger Gewebeverlust erkennbar sind.
Die Autoren betonen den Bedarf, die zugrunde liegenden Mechanismen besser zu verstehen: Das Gehirn ist auf Glukose als Energielieferant angewiesen, und wiederholter metabolischer Stress nach Mahlzeiten, verbunden mit Entzündungsreaktionen, oxidativem Stress oder neuronalem Energiestoffwechseldefizit, könnte sich über Jahre akkumulieren und schrittweise neuronale Funktionen beeinträchtigen. Mechanistisch denkbar sind außerdem Prozesse wie die Bildung von advanced glycation end products (AGEs), gestörte Insulinsignale im ZNS, Blut-Hirn-Schranken-Dysfunktion sowie Beeinflussung von Amyloid- und Tau-Metabolismus. Wie genau kurzzeitige Blutzuckerspitzen letztlich in die charakteristischen Plaques, Neurofibrillenbündel oder synaptische Dysfunktionen der Alzheimer-Krankheit münden, bleibt jedoch größtenteils unklar und erfordert molekulare sowie experimentelle Daten aus Tierstudien und menschlichen Biomarker-Analysen.
Warum Mendelianische Randomisierung relevant ist
- Mendelianische Randomisierung reduziert Verzerrungen durch Lebensstilfaktoren oder umgekehrte Kausalität, indem genetische Varianten als natürliche Experimente verwendet werden; so lassen sich Aussagen zur möglichen Kausalität eines Merkmals treffen.
- Wenn die genetische Veranlagung zu höherer 2hPG das Erkrankungsrisiko erhöht, stützt das die Hypothese, dass postprandiale Glukoseanstiege nicht nur Begleitmarker, sondern potenzielle Risikofaktoren sein könnten.
- Dennoch sind genetische Befunde allein nicht endgültig: Sie müssen in unterschiedlichen Kohorten und Populationen repliziert und durch mechanistische Laborstudien sowie Interventionsstudien ergänzt werden, um konkrete Präventionsmaßnahmen herzuleiten.
Der leitende Epidemiologe Andrew Mason (University of Liverpool) hebt die praktischen Implikationen hervor: Die Blutzuckersteuerung könnte eine Nuance über reine Nüchternwerte hinaus benötigen — das gezielte Management postprandialer Spitzen könnte für die langfristige Gehirngesundheit relevant sein. Die genetische Epidemiologin Vicky Garfield, ebenfalls in Liverpool tätig, warnt jedoch davor, Ergebnisse premature zu verallgemeinern: Replikationen sind essenziell, insbesondere in ethnisch vielfältigeren Populationen als der ursprünglich untersuchten Kohorte.
Beschränkungen und perspektive für die öffentliche Gesundheit
Der primäre Datensatz stammte aus der UK Biobank, einer Ressource, die tendenziell gesündere Personen mit höherem sozioökonomischem Status überrepräsentiert und in dieser Analyse überwiegend Teilnehmende weißer britischer Abstammung enthielt. Solche Selektionsbiases schränken die Generalisierbarkeit der Befunde ein. Darüber hinaus gelang der Nachweis in einem älteren, kleineren genetischen Datensatz mit 111.326 Personen nicht; Unterschiede in der Auswahl der Teilnehmenden, Messmethoden, statistischen Modellierung oder Stichprobengröße können diese Diskrepanz erklären. Deshalb ist der beobachtete Zusammenhang interessant und plausibel, aber vorläufig und nicht als definitiver Beweis für eine kausale Wirkung zu werten.
Für Ärztinnen und Ärzte sowie die breite Öffentlichkeit unterstreicht die Studie jedoch eine bereits etablierte Empfehlung: Das Reduzieren großer postprandialer Blutzuckerschwankungen fördert Herz-Kreislauf- und Stoffwechselgesundheit und könnte nach den neuen Daten auch für das Demenzrisiko relevant sein. Praktische Maßnahmen, die in der Primärversorgung und Gesundheitsberatung eine Rolle spielen, umfassen ausgewogene Mahlzeiten mit Ballaststoffen und Protein zur Abmilderung von Blutzuckerspitzen, die Auswahl von kohlenhydratärmeren oder niedrig-glykämischen Lebensmitteln, Portionenkontrolle, das zeitlich gezielte Einbauen von körperlicher Aktivität nach dem Essen sowie eine individuelle medizinische Therapie, wenn sie angezeigt ist (z. B. Anpassung von Diabetesmedikamenten unter ärztlicher Aufsicht). Zusätzlich können kontinuierliche Glukosemessung (CGM) und Ernährungsberatung helfen, postprandiale Muster zu erkennen und gezielt zu steuern.
Zukünftige Studien könnten klären, ob gezielte Interventionen zur Reduktion postprandialer Glukosespitzen tatsächlich die Inzidenz von Alzheimer senken. Solche Studien sollten randomisierte Interventionsdesigns, längere Nachbeobachtungszeiten und die Einbeziehung verschiedener Ethnien und Altersgruppen umfassen. Kombinierte Ansätze aus Lebensstilinterventionen (Ernährung, körperliche Aktivität), pharmakologischen Maßnahmen und Biomarker-Tracking (z. B. Amyloid-/Tau-PET, Liquor- und Blutmarker, neuroinflammatorische Marker) würden helfen, Kausalität und Wirkmechanismen belastbarer nachzuweisen.
Während das Forschungsfeld voranschreitet, sind drei empirische Schritte zentral: (1) Replikation der genetischen Signale in unterschiedlichen Abstammungsgruppen und Kohorten; (2) Aufklärung der zellulären und molekularen Mechanismen im zentralen Nervensystem, etwa durch Tiermodelle, zellbiologische Studien und menschliche Biomarker-Analysen; und (3) Durchführung klinischer Interventionsstudien, die gezielt postprandiale Glukoseanstiege reduzieren, um zu testen, ob sich das Demenzrisiko dadurch tatsächlich modulieren lässt. Nur durch diese mehrstufige Forschung wird sich zeigen, ob postprandiale Blutzuckerkontrolle künftig als gesicherte präventive Maßnahme gegen Alzheimer gilt.
Quelle: sciencealert


Kommentar hinterlassen