8 Minuten
Forscher berichten von einer ersten, am Menschen durchgeführten Stammzelltransplantation, die offenbar bei einigen älteren Menschen mit trockener altersbedingter Makuladegeneration (AMD) die Zentralvision wiederherstellen kann. Frühphasige klinische Daten zeigen, dass das Verfahren sicher ist und bei den am stärksten betroffenen Studienteilnehmern bedeutende Sehkraftgewinne erzeugte, was die Forscher veranlasste, weitere Untersuchungen mit höheren Dosen durchzuführen.
Warum die Zentralvision bei trockener AMD nachlässt — und warum das wichtig ist
Die altersbedingte Makuladegeneration ist die häufigste Ursache für irreversible zentrale Sehbeeinträchtigungen bei älteren Erwachsenen. Die „Makula“ ist der kleine zentrale Bereich der Netzhaut, der Aufgaben erlaubt, die scharfes Sehen erfordern — Lesen, Gesichtererkennung und sicheres Autofahren. Bei der trockenen Form der AMD, die etwa 80 % der Fälle ausmacht, lagern sich winzige Ablagerungen aus Fetten und Proteinen, sogenannte Drusen, unter dem retinalen Pigmentepithel (RPE) ab. Im Lauf der Zeit schädigen diese Ablagerungen die RPE-Zellen — das stützende Gewebe, das die lichtempfindlichen Photorezeptoren ernährt — und der fortschreitende Zellenverlust führt zu einer zunehmenden Unschärfe im zentralen Gesichtsfeld.
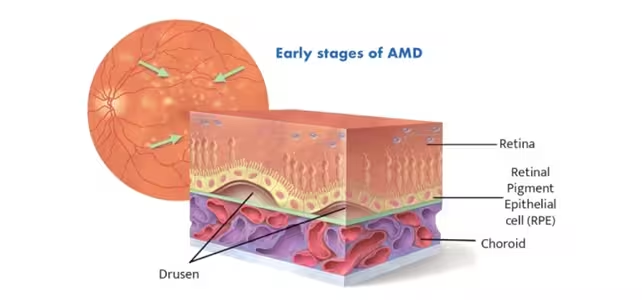
Diagramm, das frühe Stadien der trockenen Makuladegeneration zeigt, verursacht durch Ablagerungen aus Fetten und Proteinen (Drusen) unter dem RPE.
Was die neue Studie testete und wie das Verfahren funktioniert
Die veröffentlichte Phase‑1/2a-Studie untersuchte eine Transplantation von RPE-Zellen, die aus adulten Stammzellen gewonnen und von einer Augenbank bereitgestellt wurden. Ziel dieser frühen Studie war in erster Linie die Prüfung der Sicherheit und eine vorläufige Bewertung der Wirksamkeit — noch keine direkte Vergleichsstudie mit etablierten Therapien. Die Forscher screenten 18 potenzielle Teilnehmende und rekrutierten sechs Freiwillige im Alter von 71 bis 86 Jahren, die in einem Auge eine fortgeschrittene trockene AMD aufwiesen.
Applikation und Dosierung
Jede Teilnehmerin bzw. jeder Teilnehmer erhielt eine einmalige, vergleichsweise niedrige Dosis von 50.000 RPE-Stammzellen, die unter die Netzhaut in die oberen, seitlichen Anteile der Makula des schlechter sehenden Auges injiziert wurden. Die transplantierten Zellen sollen zerstörtes RPE-Gewebe ersetzen und das Mikro‑Milieu wiederherstellen, das die Photorezeptoren gesund hält. Die technische Durchführung erfordert mikrochirurgische Präzision, um die Zellen genau in die Subretinalzone zu platzieren, ohne die umliegenden Strukturen übermäßig zu belasten.
Voruntersuchungen im Labor und Sicherheitsprüfungen
Präklinische Laborexperimente hatten gezeigt, dass die transplantierten Zellen ihre retinale Identität bewahren und keine Tumorbildung oder systemische Toxizität verursachen — Befunde, die den Weg für Studien am Menschen ebneten. Während der klinischen Studie überwachten die Forschenden die Teilnehmenden engmaschig auf immunologische Reaktionen, Anzeichen tumoröser Veränderungen und die typischen Komplikationen, die mit Netzhautchirurgie verbunden sein können, wie z. B. Netzhautablösung oder Entzündungsreaktionen. Zusätzlich wurden Routine-Untersuchungen wie OCT (Optische Kohärenztomographie), Fundusfotografie und Sehschärfe-Tests eingesetzt, um strukturelle und funktionelle Veränderungen zu dokumentieren.
Zentrale Ergebnisse: Sicherheit zuerst — und überraschende Sehverbesserungen
Die Studie erreichte ihre primären Sicherheitsendpunkte. Es traten keine unerwünschten Ereignisse auf, die direkt auf die implantierten Stammzellen zurückgeführt werden konnten — keine Tumorbildung und keine eindeutigen Hinweise auf eine zellbezogene, immunvermittelte Abstoßungsreaktion. Einige Teilnehmende erfuhren typische, chirurgisch bedingte Komplikationen, die jedoch behandelbar blieben und nicht mit dem Zellprodukt selbst in Zusammenhang standen. Solche Komplikationen wurden in klinischen Protokollen vorab antizipiert und konnten in den meisten Fällen konservativ oder chirurgisch beherrscht werden.
Was die Wirksamkeit angeht, überraschten Verbesserungen der Sehleistung, die ausschließlich im behandelten Auge auftraten, die Untersuchenden. Drei Teilnehmende mit der schlechtesten Ausgangssehschärfe (ungefähr 20/200 bis 20/800) gewannen durchschnittlich 21 Buchstaben auf dem Sehprobentafeltest ein Jahr nach der Injektion. Die anderen drei Teilnehmenden, die mit einer besseren Ausgangssehschärfe starteten (etwa 20/70 bis 20/200), zeigten kleinere Verbesserungen. Die einseitige Verbesserung — also nur im Auge mit der Zelltransplantation — stärkt die Annahme, dass das Transplantat selbst zu den beobachteten visuellen Zugewinnen beigetragen hat, statt dass generelle systemische oder placeboartige Effekte zugrunde lagen.
„Obwohl uns die Sicherheitsdaten erfreut haben, war der spannende Teil, dass sich auch ihre Sehfähigkeit verbesserte“, sagte Rajesh Rao, Arzt-Wissenschaftler und Augenarzt bei Michigan Medicine. „Wir waren überrascht über das Ausmaß der Sehverbesserung bei den am stärksten betroffenen Patienten, die die aus adulten Stammzellen abgeleiteten RPE-Transplantate erhielten. Ein derartiger Sehzuwachs wurde in dieser Gruppe von Patienten mit fortgeschrittener trockener AMD bislang nicht beobachtet.“
Was das für Patientinnen und Patienten bedeutet und welche nächsten Forschungsschritte geplant sind
Diese Ergebnisse sind vielversprechend, aber vorläufig. Die kleine Stichprobengröße (sechs Teilnehmende bei einer niedrigen Dosis) bedeutet, dass größere randomisierte Studien erforderlich sind, um den Nutzen zu bestätigen, die Haltbarkeit der Effekte zu messen und die Ergebnisse mit bestehenden oder aufkommenden Behandlungsoptionen zu vergleichen. Die laufende Studie verfolgt weiterhin Kohorten, die höhere Dosen erhalten — 150.000 und 250.000 Zellen — um zu klären, ob eine Skalierung der Dosis die Sicherheit erhält und die Wirksamkeit verbessert. Solche Dosis-Eskalationsphasen sind entscheidend, um ein therapeutisches Fenster zu definieren: die Dosis, bei der der maximale Nutzen bei akzeptablem Risiko erreicht wird.
Falls höhere Dosen sicher sind und gleichwertige oder größere Sehverbesserungen erzeugen, würden die Forschenden Phase‑3-Studien entwerfen, um die Behandlung gegen den aktuellen Versorgungsstandard zu testen. Selbst dann werden Zulassungsverfahren, die Hochskalierung der Herstellung und die Sicherstellung eines breiten Zugangs für Patientinnen und Patienten mehrere Jahre in Anspruch nehmen. Hinzu kommen regulatorische Anforderungen für GMP‑konforme Zellprodukte, Langzeitüberwachungen zur Sicherheit und Kostenfragen, die für Gesundheitsbehörden und Kostenträger relevant sind.
Zugehörige Technologien und klinischer Kontext
Aus Stammzellen gewonnene RPE-Transplantate gehören zu einem wachsenden Arsenal regenerativer Ansätze, die auf Netzhauterkrankungen abzielen — von Gentherapien, die molekulare Defekte korrigieren, über Zellschicht-Implantate bis hin zu innovativen Medikamentenabgabesystemen, die das Fortschreiten der Degeneration verlangsamen sollen. Gemeinsam verfolgen diese Strategien das Ziel, verbliebene Sehfunktionen zu erhalten oder verlorene Funktion wiederherzustellen, sobald essentielle Zellpopulationen geschädigt sind. Forschungsteams weltweit kombinieren dabei Grundlagenforschung, präklinische Modelle und klinische Studien, um Therapiekonzepte zu optimieren.
Für Menschen mit trockener AMD — die derzeit nur begrenzte therapeutische Optionen über Lebensstiländerungen, Nahrungsergänzungen und Hilfsmittel für geringere Sehvermögen verfügen — könnte ein sicheres, wirksames RPE-Transplantat eine Verschiebung vom rein symptomatischen Management hin zu einer teilweisen Wiederherstellung darstellen. Entscheidend werden technische Aspekte der Zellintegration, Immunmodulation, die Standardisierung des Produkts und Daten zur Langzeitfunktionalität sein.
Fachliche Einschätzung
„Eine gezielte RPE-Transplantation adressiert einen konkreten Ausfallpunkt bei der trockenen AMD: den Verlust der unterstützenden Pigmentepithelzellen“, erklärt Dr. Elena Morales, Netzhautchirurgin und Translationalwissenschaftlerin. „Wenn wir diese Zellen zuverlässig ersetzen können, ohne Immunprobleme oder Tumorrisiken auszulösen, könnte der nachgeschaltete Nutzen für die Photorezeptoren erheblich sein. Die nächsten Hürden sind die Reproduzierbarkeit der Ergebnisse und die langfristige Integration der transplantierten Zellen in die komplexe Architektur der Netzhaut.“
Aus wissenschaftlicher Sicht sind mehrere offene Fragen weiterhin relevant: Wie stabil bleibt die Integration der RPE-Zellen über Jahre? Verbessert sich die Netzhautfunktion auch in anderen Messparametern wie Kontrastempfindlichkeit oder der Lesegeschwindigkeit? Lässt sich das Verfahren so standardisieren, dass Herstellungs- und Qualitätskontrollen auf Breitenmaßstab möglich sind? Antworten auf diese Fragen werden nicht nur klinisch, sondern auch industriell und regulatorisch von großer Bedeutung sein.
Für Patientinnen und Patienten ist zudem die Frage nach Zugänglichkeit bedeutsam: Welche Zentren können die Operationen durchführen, welche Voraussetzungen müssen gegeben sein und welche Kosten kommen auf Betroffene und Gesundheitssysteme zu? Klinische Studien dieser Art legen oft den Grundstein für spätere, zentral verfügbare Behandlungsangebote, erfordern aber gleichzeitig erhebliche Investitionen in Ausbildung und Infrastruktur.
Zusammenfassend lässt sich sagen, dass die berichteten Befunde einen bedeutenden Schritt in der regenerativen Netzhautchirurgie markieren. Sie liefern erste Hinweise darauf, dass eine therapeutische Wiederherstellung von RPE‑Funktionen möglich ist und in ausgewählten Fällen zu messbaren visuellen Verbesserungen führt. Die Forschungsgemeinschaft wird diese Signale in größeren, kontrollierten Studien validieren müssen, um die potenzielle Rolle der RPE‑Stammzelltransplantation in der AMD‑Versorgung endgültig zu bestimmen.
Quelle: sciencealert

Kommentar hinterlassen